Cuando se interpreta una canción conocer y leer las notas musicales es tan importante como hacerlo con el ritmo adecuado. En la partitura, las notas musicales se colocan de forma secuencial y diferentes marcas informan sobre el registro, la velocidad o la intensidad con que se deben hacer sonar. La epigenética estudia marcas similares, situadas en el genoma.

El genoma humano funciona de forma similar a una partitura, en la que la secuencia de ADN contiene las instrucciones para producir las proteínas y otros elementos funcionales, y los mecanismos epigenéticos regulan cómo y en qué grado tienen que expresarse.
Así, si el genoma incluye la secuencia completa del ADN, el epigenoma, se refiere al conjunto de elementos que regulan la expresión de los genes sin alterar la secuencia de ADN. Y si el genoma constituye las instrucciones de nuestro organismo, el epigenoma permite interpretarlas. La epigenética es la disciplina que estudia el epigenoma y los mecanismos epigenéticos.
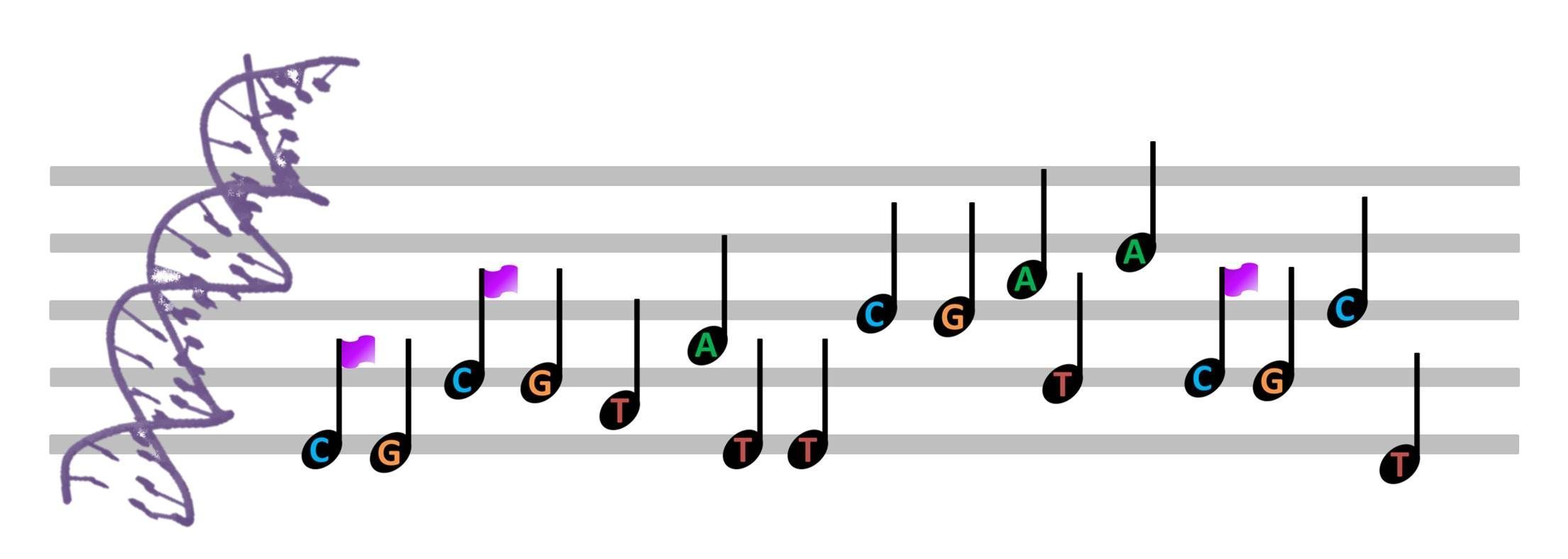
¿Qué hace la epigenética?
En esencia, todas las células del cuerpo humano contienen el mismo material genético (o la misma partitura, si seguimos comparando genética y música). Sin embargo, todas ellas no expresan los mismos genes.
Cada tipo celular, dentro de cada tejido, tiene un programa genético diferente, de modo que únicamente se expresan los genes que necesitan. Por ejemplo, además de los genes encargados de las funciones básicas, las neuronas necesitan expresar todos aquellos genes relacionados con emisión y recepción de señales nerviosas. Estos genes, por el contrario, no son necesarios en otros tipos celulares, como las células encargadas de almacenar grasa.
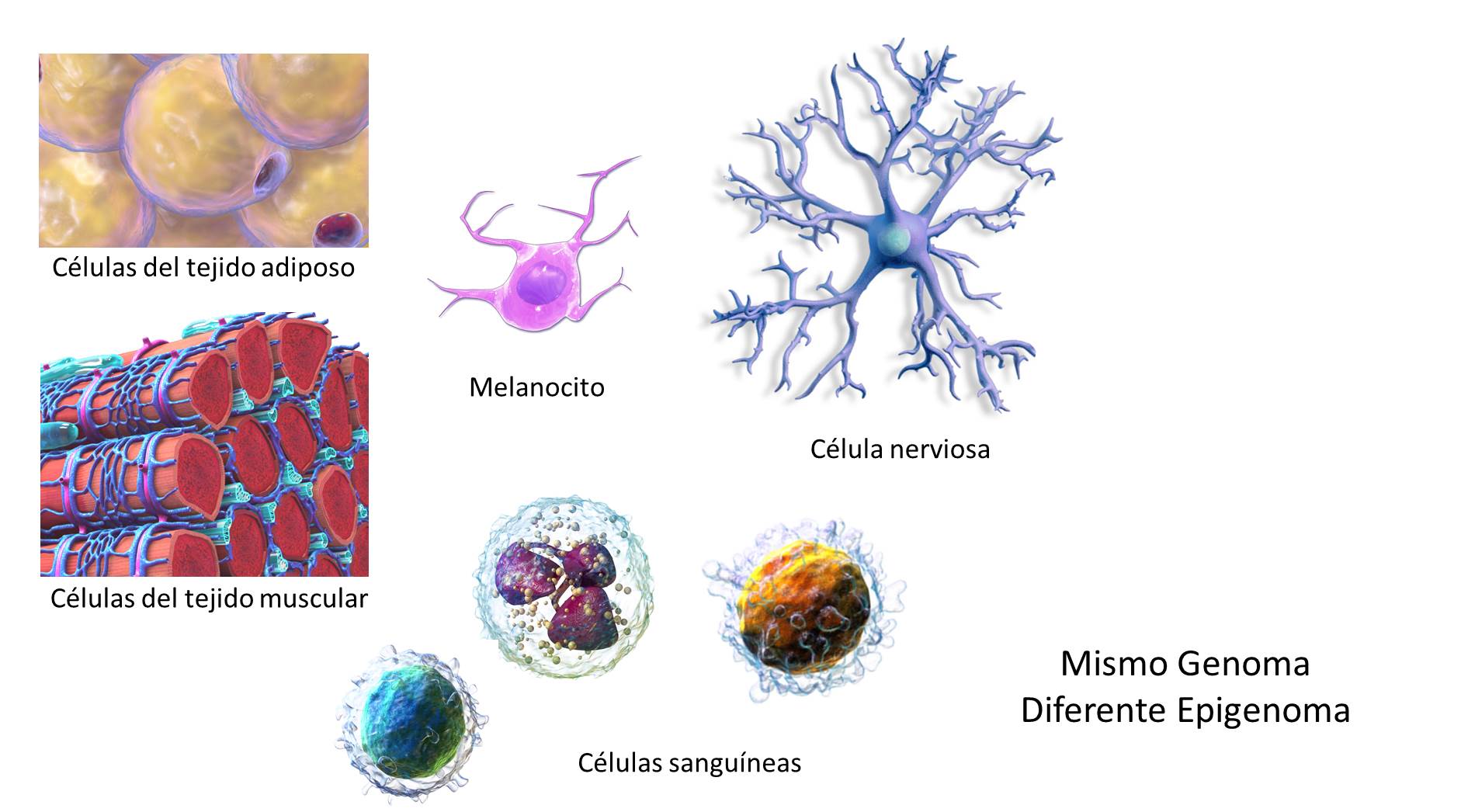
Además, cuando las células expresan los genes, necesitan hacerlo en el momento y cantidad adecuada. ¿Cómo? Uno de los métodos por los que lo consiguen es a través de los mecanismos epigenéticos.
Las marcas epigenéticas actúan como una memoria para la célula y son reversibles
Una de las características del epigenoma es que no es estático y puede modificarse. A lo largo de nuestra vida, el epigenoma registra las experiencias de la célula, así como la influencia del ambiente sobre las mismas.
Por lo tanto, el epigenoma es diferente en los distintos tejidos y tipos celulares del organismo, cambia a lo largo de la vida o momento del desarrollo e incluso en los distintos estados de salud.
¿Qué tipos de mecanismos epigenéticos existen?
A continuación presentamos los principales mecanismos epigenéticos. Todos ellos son reversibles, lo que significa que son susceptibles de poder ser modificados.
- Metilación del ADN
La metilación del ADN es uno de los mecanismos epigenéticos más estudiados. Consiste en la adición de un grupo bioquímico denominado metilo a una de las unidades o nucleótidos que conforman el ADN, la citosina.

Los grupos metilo situados sobre el ADN actúan como señales de reconocimiento para ciertas enzimas que actúan sobre la expresión génica. Normalmente la metilación se asocia a una represión de la expresión génica.
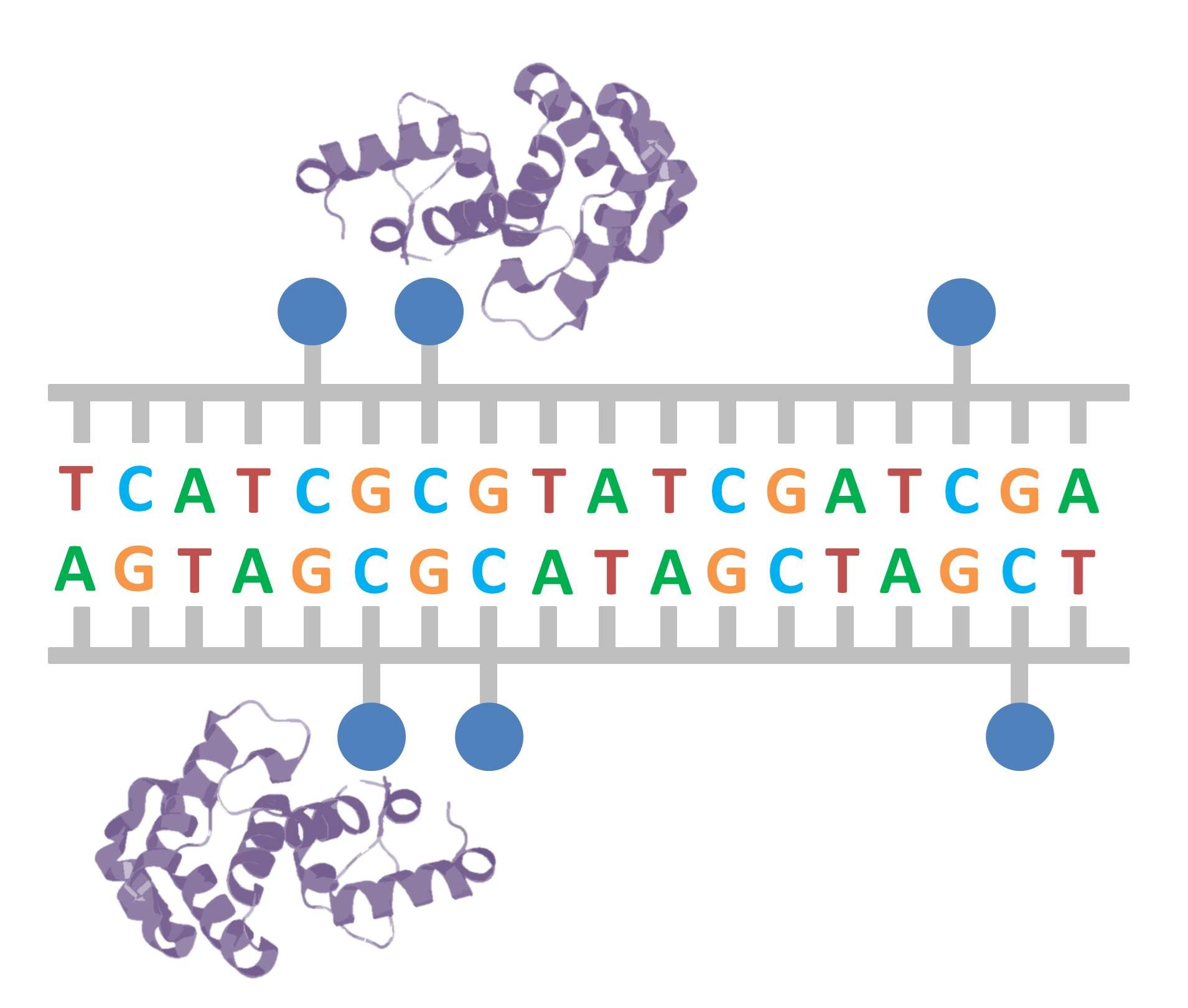
- Modificaciones de la cromatina
En el interior del núcleo celular el ADN no se presenta aislado, sino que está organizado con proteínas y otras moléculas, formando la cromatina. La unidad fundamental de la cromatina, es el nucleosoma, formado por ADN enrollado alrededor de ocho unidades de proteínas histonas.
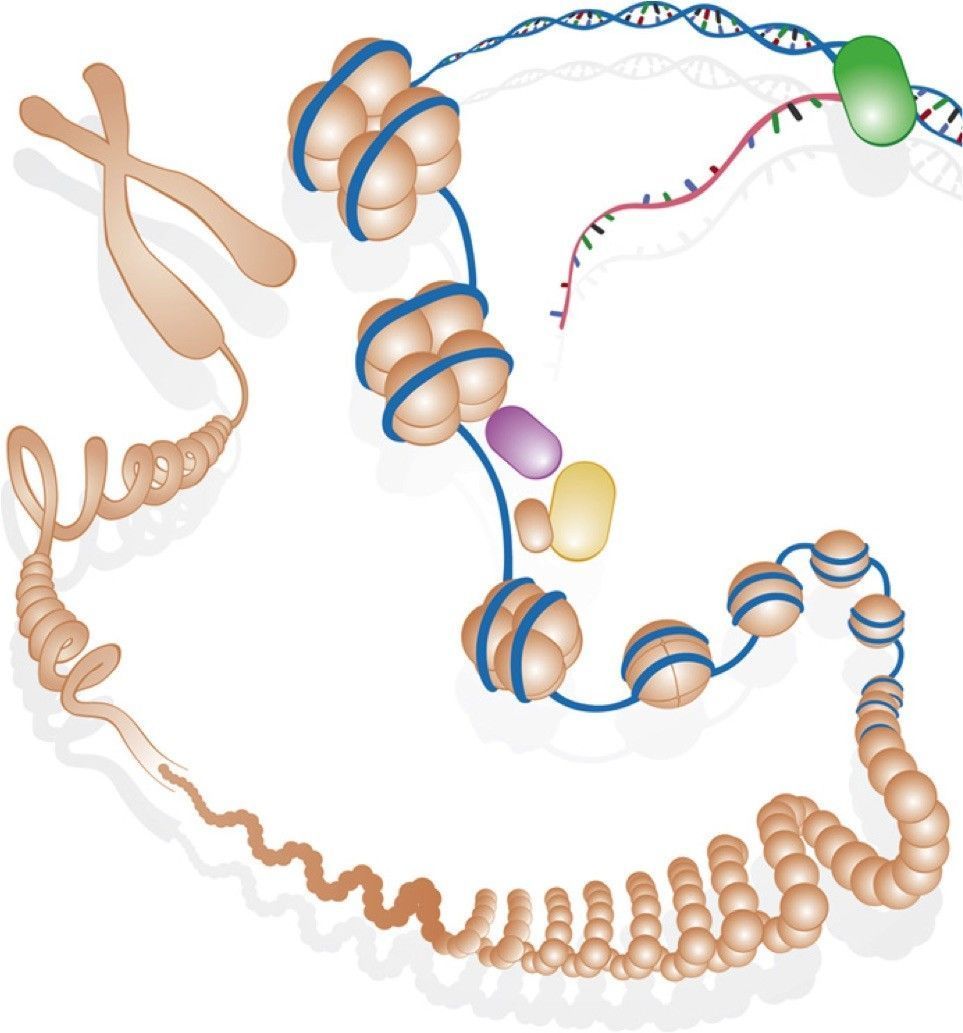
Las histonas pueden ser modificadas bioquímicamente en algunas posiciones concretas (modificaciones epigenéticas reversibles), lo que afecta al grado de compactación del ADN en el nucleosoma, y a cómo de accesibles son los genes a toda la maquinaria enzimática responsable de la expresión génica. Cuanto más compactado está el ADN en un nucleosoma menos accesibles son los genes de esa región. Por el contrario si el ADN está menos compactado, hay más espacio para que las proteínas relacionadas con la expresión génica se unan al ADN.
Las combinaciones de las modificaciones de las histonas definen el estado de la cromatina y la actividad del ADN que lo conforma.
Además, la localización de los nucleosomas también determina la accesibilidad de los factores de transcripción al ADN.
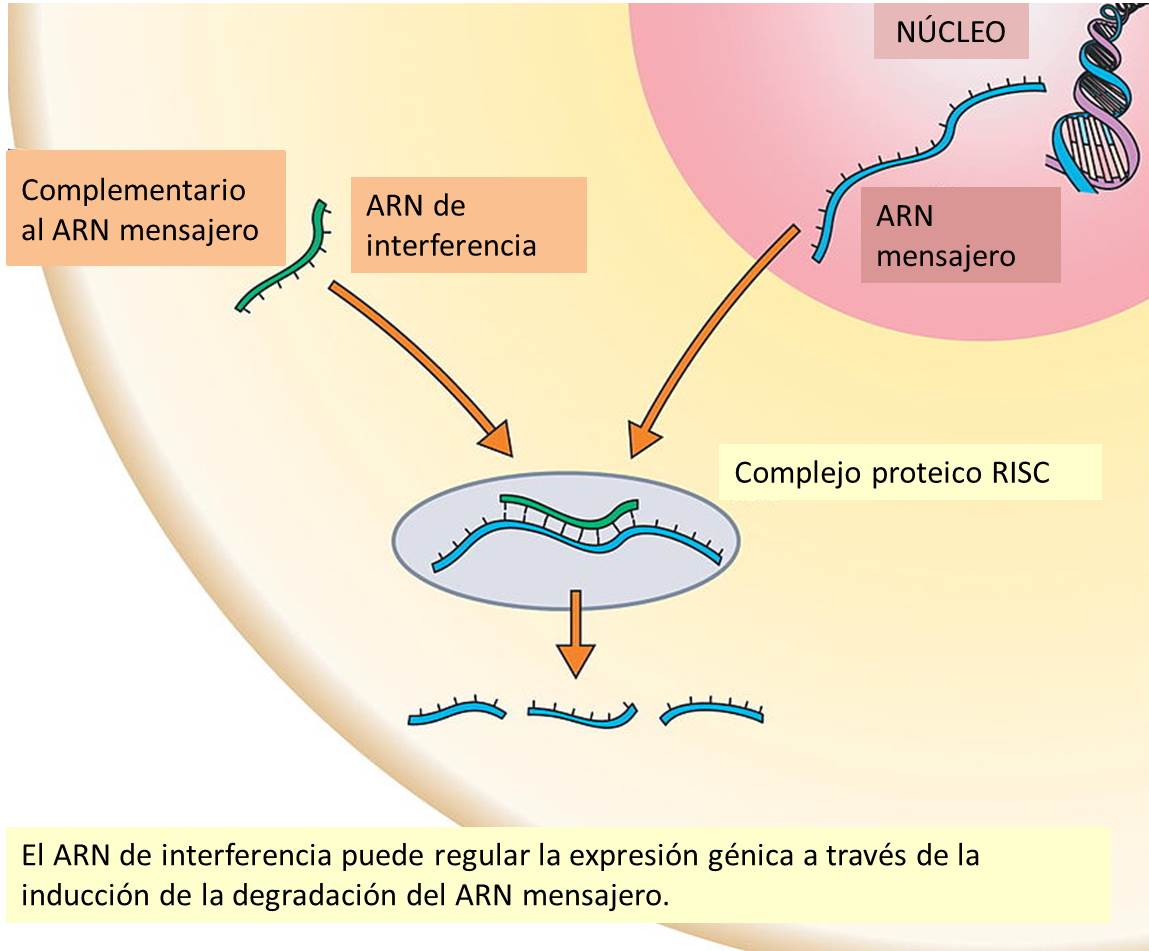
- ARN de interferencia
Ciertas moléculas pequeñas de ARNs pueden silenciar la expresión de los genes, uniéndose al ADN e interfiriendo con la transcripción o proceso en el que el que se transfiere la información del ADN al ARN o uniéndose a complejos proteicos de silenciamiento génico.
Los diferentes mecanismos epigenéticos interaccionan entre sí. Por ejemplo, la maquinaria celular encargada de remodelar los nucleosomas es influida por la metilación de ADN y por las modificaciones en las histonas. Igualmente la metilación del ADN supone una señal para reclutar complejos proteicos que incluyen proteínas modificadoras de las histonas.
Cuando los mecanismos epigenéticos no funcionan de forma correcta pueden desarrollarse enfermedades. Un ejemplo es el Síndrome de Rett, producido en la mayoría de los casos por mutaciones en el gen MECP2 que codifica para una proteína de unión a ADN metilado.
Epigenética y ambiente
La epigenética actúa como puente entre los genes y el ambiente. Algunos factores ambientales, como el tabaco, o la nutrición pueden iniciar procesos químicos que lleven a cambios en el epigenoma.
Epigenética y envejecimiento
Como mencionábamos antes, el epigenoma es dinámico y va cambiando a lo largo de la vida de una persona. Por ejemplo, al comparar la metilación del genoma en personas recién nacidas, adultos y ancianos se ha observado que a medida que se envejece se van perdiendo grupos metilo, lo que podría estar asociado con la expresión inadecuada de los genes al envejecer.
Además, aquellos pacientes con enfermedades en las que se produce un envejecimiento prematuro presentan epigenomas propios de edades mucho más avanzadas.
Algunos estudios indican que se pueden usar marcadores epigenéticos, concretamente metilación, para estimar la edad biológica de una persona, frente a su edad cronológica en años. Así, el epigenoma podría dar una medida de cómo de bien se envejece.
Epigenoma y cáncer
Las células tumorales tienen su epigenoma alterado. Cambios en el epigenoma pueden llevar a que se expresen genes que no deberían hacerlo, como por ejemplo aquellos relacionados con el crecimiento celular y la proliferación o evitar que se expresen genes cuya actividad es necesaria, como aquellos relacionados con la reparación del ADN.
Dado que las modificaciones epigenéticas son reversibles, diferentes equipos de investigación han planteado desarrollar fármacos epigenéticos para tratar el cáncer. A nivel clínico algunos de estos fármacos ya han sido aprobados, mientras que otros siguen siendo investigados.
Si te ha gustado este blog y quieres aprender más sobre Genética en Medicina, te interesa nuestra formación, como el “Máster de Medicina de Precisión y Genética Clínica“, o el curso “Epigenética en Medicina“.



