Hola de nuevo, seguidores de nuestro blog. Hoy, queremos hablaros acerca de una de las enfermedades genéticas más estudiadas: la anemia falciforme. Esta enfermedad genética, que afecta a entre 1 y 5 personas por cada 10.000 habitantes, fue la primera en tener aprobada una terapia génica basada en CRISPR ¿Te interesa? ¡Sigue leyendo!
¿En qué consiste la anemia falciforme?
La anemia falciforme, también conocida como drepanocitosis, es un trastorno sanguíneo que afecta a los glóbulos rojos de la sangre, también conocidos como eritrocitos. Normalmente, estas células tienen una forma redonda y son flexibles, lo que les permite moverse fácilmente a través de los vasos sanguíneos. Sin embargo, en las personas con anemia falciforme, los glóbulos rojos tienen una forma anormal de media luna o «hoz». Esta forma irregular los hace rígidos, provoca que se muevan con dificultad en los capilares sanguíneos y hace que se rompan con una mayor facilidad.
Los síntomas de la anemia falciforme varían entre unas personas. Entre ellos se incluyen: dolor intenso (conocido como crisis de dolor), fatiga, hinchazón en las manos y pies, infecciones frecuentes y problemas de crecimiento en niños. La gravedad de estos síntomas también puede variar de una persona a otra.

Modo de herencia y causa genética
Desde hace tiempo se sabe que la causa genética de la anemia falciforme se encuentra en mutaciones específicas del gen HBB. Este gen codifica para la beta globina una de las subunidades que conforman la hemoglobina, proteína que se encuentra en el interior de los glóbulos rojos que se encarga de transportar el oxígeno y ayuda a mantener la estructura redondeada y flexible de estas células.
En cuanto al modo de herencia, la anemia falciforme es una enfermedad autosómica recesiva. Es decir, para que una persona desarrolle la enfermedad, debe heredar dos copias mutadas del gen HBB, una de cada uno de sus progenitores.
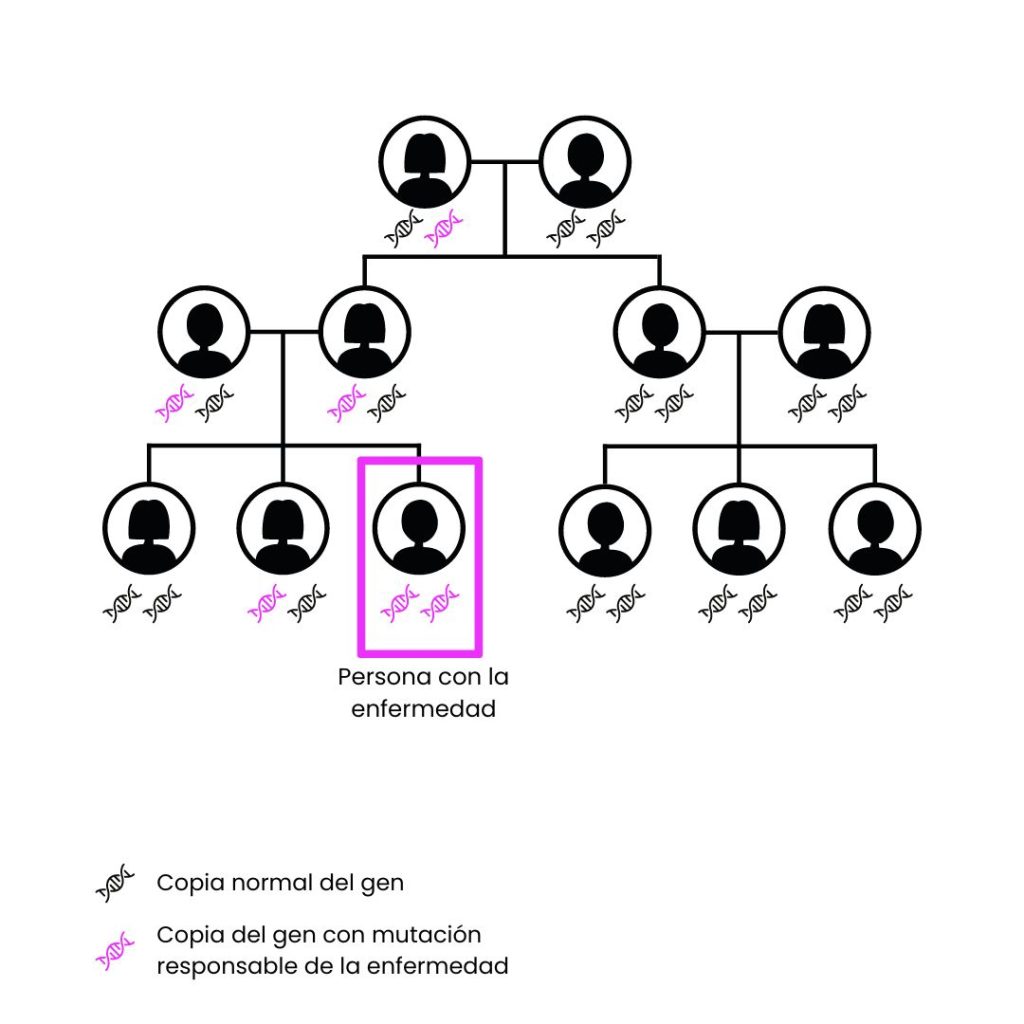
Cuando una persona presenta una copia del gen defectuoso y una copia normal, se dice que es portadora de la enfermedad, pero generalmente no presenta síntomas significativos. Lo que sí puede ocurrir es que transmita una copia alterada de HBB a su descendencia. En este caso, si los hijos o hijas reciben otra copia alterada del otro progenitor, es cuando se manifiesta la enfermedad.
Tratamientos para la anemia falciforme
A diferencia de otras enfermedades genéticas, la anemia falciforme dispone de opciones terapéuticas curativas. Entre ellas, se encuentran el trasplante de médula ósea y la administración de Casgevy, la primera terapia génica basada en CRISPR aprobada para su utilización en humanos. Esta última, aprobada en 2023 por la agencia reguladora de medicamentos de Reino Unido, ha supuesto un salto grandísimo en el tratamiento de la anemia falciforme.
Hasta ahora, el tratamiento se había centrado, principalmente, en el manejo de los síntomas y la prevención de complicaciones. Algunas de las opciones son:
- Analgésicos para el tratamiento del dolor, ya que las crisis de dolor son una de las manifestaciones más comunes y dolorosas de la anemia falciforme.
- Hidroxiurea. Este medicamento puede ayudar a reducir la frecuencia de las crisis de dolor y la necesidad de transfusiones de sangre. Funciona aumentando la producción de hemoglobina fetal, una forma de hemoglobina que no se deforma como la hemoglobina S.
- Transfusiones de sangre. Las transfusiones regulares pueden ayudar a tratar la anemia severa.
- Antibióticos y vacunas. Debido a que las personas con anemia falciforme son más propensas a las infecciones, las vacunas son fundamentales para prevenir enfermedades graves.
¿Cómo funciona la terapia génica aprobada para la anemia falciforme?
La terapia génica aprobada en noviembre de 2023 se basa en la introducción de células madre responsables de producir las células de la sangre cuyas copias del gen HBB han sido sustituidas por copias funcionales. Para ello, se extraen estas células madre del paciente y se modifica su genoma mediante la herramienta CRISPR. Luego, se amplifica el número de células y se reintroducen en el paciente, permitiendo que el paciente genere eritrocitos con hemoglobinas funcionales.
Hasta aquí nuestro post de hoy. Si te interesan las terapias génicas y quieres aprender un poco más acerca de estas aproximaciones terapéuticas, puedes aprender más en nuestro programa “Introducción a la Terapia Génica y Edición del Genoma”. En él, aprenderás los aspectos básicos de este tipo de terapias, así como sus aplicaciones clínicas en diferentes enfermedades, como la hemofilia o el cáncer.
Enlaces de interés
Enfermedad de células falciformes. MedlinePlus: https://medlineplus.gov/spanish/sicklecelldisease.html
¿Qué es la enfermedad de células falciformes? National Institutes of Health: https://www.nhlbi.nih.gov/es/salud/enfermedad-de-celulas-falciformes
Anemia de células falciformes: hoja informativa. FDA. https://www.fda.gov/consumers/minority-health-and-health-equity-resources/anemia-de-celulas-falciformes-hoja-informativa