A finales del siglo XX, un descubrimiento acerca de unos pequeños microorganismos sembraría la semilla de la herramienta molecular que revolucionó (y continúa revolucionando) la edición genética. Así es, me refiero a CRISPR, una “nanoherramienta” que, hasta la fecha, ha demostrado ser de utilidad en una gran batería de situaciones diferentes. ¿Quieres saber más sobre ella? ¡Continúa leyendo!
¿Qué es CRISPR y cómo funciona?
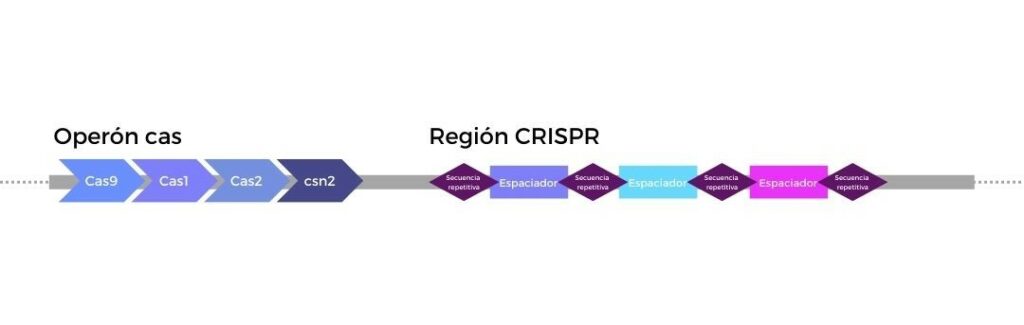
Los locus CRISPR son una serie de regiones altamente repetitivas que se encuentran presentes en el genoma de diferentes especies de bacterias y arqueas. Están formadas por dos partes diferenciadas, el operón cas y la región CRISPR. Por un lado, el operón cas contiene la información genética para codificar las endonucleasas Cas y otras proteínas relevantes para la función de CRISPR-cas. Por el otro lado, la región CRISPR está formada por secuencias repetidas intercaladas con pequeñas secuencias espaciadoras, de origen exógeno.
Origen y descubrimiento de CRISPR
La historia de CRISPR comienza a finales de los años 80 en el laboratorio de Yoshizumi Ishino de la Universidad de Osaka. Ishino y su equipo describieron por primera vez unas secuencias repetidas muy características (los locus CRISPR) en el genoma de Escherichia coli. Poco después, en 1993, el equipo de investigadores dirigido por el microbiólogo alicantino Francisco Juan Martínez Mojica identificó (de forma independiente) estas secuencias repetidas en una arquea, Haloferax mediterranei. En ese momento los dos equipos desconocían la función de estas secuencias y, por tanto, no se podían ni imaginar su gran potencial en biología molecular.
Diferentes grupos de investigadores, incluido el equipo de Mojica, continuaron investigando las secuencias repetidas y las identificaron en múltiples grupos de bacterias y arqueas, además de en el genoma mitocondrial. Fue entonces cuando el alicantino acuñó, por primera vez, el término CRISPR (siglas en inglés de “Repeticiones Palindrómicas Cortas Agrupadas Regularmente Interespaciadas”).
Poco después del descubrimiento de las secuencias CRISPR, diferentes equipos de investigadores encontraron que ciertos espaciadores de estas secuencias derivan de virus bacteriófagos o plásmidos. En ese momento, el grupo de Mojica sugirió que las secuencias CRISPR podían formar parte de algún tipo de “sistema inmunitario adaptativo” propio de los organismos unicelulares, como bacterias y arqueas. Y no se equivocaba, aunque esto no se confirmaría hasta años más tarde.
A principios del siglo XXI, múltiples equipos de investigadores intentaron descifrar los mecanismos moleculares relacionados con las secuencias CRISPR, con el objetivo de determinar cuál era realmente su función. Finalmente, en 2007, el equipo del francés Rodolphe Barrangou publicó un artículo en el que se detallaba cómo las secuencias CRISPR, junto a unas proteínas llamadas “cas”, proporcionan resistencia adquirida a infecciones pasadas en bacterias procariotas.
¿Cómo actúa el CRISPR-Cas original sobre el ADN?
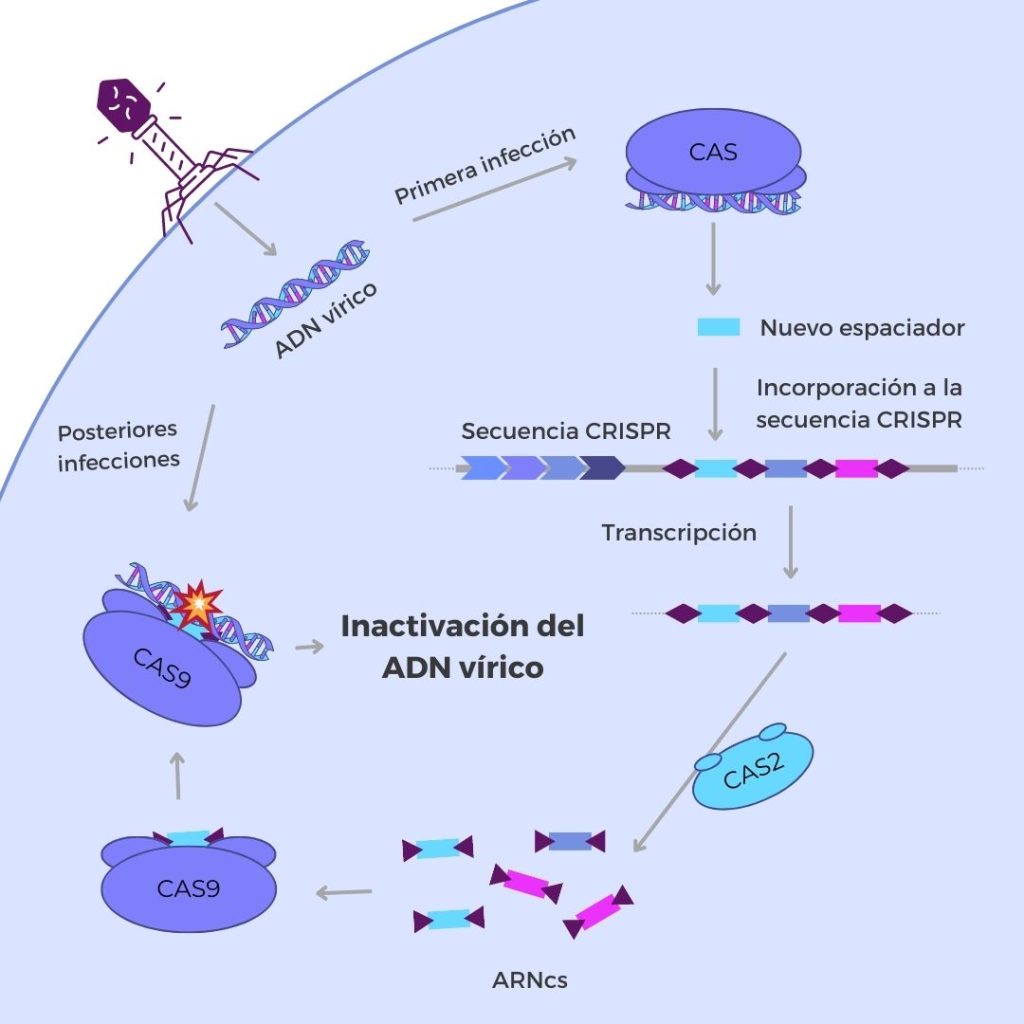
En cuanto a su funcionamiento, el sistema CRISPR-Cas es una especie de “sistema inmunitario adaptativo” presente en ciertos microorganismos que consta de varias etapas.
En primer lugar, el sistema identifica el ADN exógeno y lo incluye en su “batería” de espaciadores. Las proteínas encargadas de este primer paso son Cas1 y Cas2, proteínas capaces de identificar las secuencia de ADN exógeno, normalmente provenientes de virus bacteriófagos. Estas proteínas, además, cortan el ADN exógeno, generando un “protoespaciador”, que posteriormente será modificado e insertado en una secuencia CRISPR.
En segundo lugar, el sistema CRISPR identifica el ADN de un virus que ya ha infectado previamente un organismo unicelular y lo corta mediante una endonucleasa, para evitar una nueva infección. Para ello, el organismo sintetiza múltiples cadenas de ARN a partir del locus CRISPR y las proteínas cas lo separan en pequeñas moléculas de ARN con la información de un espaciador (denominadas ARNcr). Estos ARNcr se asocian a diferentes proteínas Cas y se unen al ADN del fago, interfiriendo en su ciclo de replicación. Posteriormente, las proteínas Cas cortan la secuencia de ADN exógeno, evitando la infección vírica por completo.
CRISPR como técnica de edición genómica
La verdadera “revolución CRISPR” comenzó en el inicio del siglo XXI. Y es que el nuevo sistema de inmunidad adquirida que se había identificado en microorganismos se convirtió en una herramienta con un potencial inimaginable en biología molecular. Esto se lo debemos a una gran multitud de investigadores de todo el mundo, entre los que se encuentran las bioquímicas Emmanuelle Charpentier y Jennifer Doudna, pioneras en el campo de las tecnologías CRISPR. Juntos, sus equipos se basaron en el sistema CRISPR de las bacterias para diseñar una herramienta molecular capaz de editar las moléculas de ADN a placer, CRISPR-Cas9. Por ello, se les otorgó el Premio Nobel de Química del año 2020.
Diferencias entre CRISPR-Cas9 y otras técnicas de edición genética
Antes de la aparición de CRISPR-Cas9 ya existían otras herramientas de edición genómica, como las meganucleasas, las nucleasas de dedos de zinc (ZFNs) o las nucleasas tipo TALEN. Estas tecnologías permitían modificar el ADN en regiones específicas del genoma, pero presentaban importantes limitaciones. Por ejemplo, el diseño de estas nucleasas era complejo, costoso y requería una gran optimización para cada nueva secuencia objetivo.
CRISPR-Cas9 supuso un cambio radical porque su especificidad depende principalmente de una pequeña molécula de ARN guía. Esto significa que modificar el lugar del genoma que se quiere editar es tan sencillo como diseñar un nuevo ARN guía, lo que hace que la técnica sea mucho más rápida, versátil y económica que las anteriores
Tecnología CRISPR: historia y tipos
Actualmente, se han diseñado múltiples herramientas CRISPR, que pueden ser utilizadas en diferentes ámbitos de la Biología Molecular y la Genómica para lograr diferentes resultados. Las tecnologías CRISPR más conocidas en el ámbito de la Salud son:
Edición genómica por nucleasa estándar (CRISPR-Cas9):
Se trata de un método de edición del genoma basado en CRISPR que se fundamenta en la acción de Cas9 como nucleasa. Se puede utilizar para corregir mutaciones, suprimir e insertar secuencias de ADN e incluso para inactivar genes concretos.
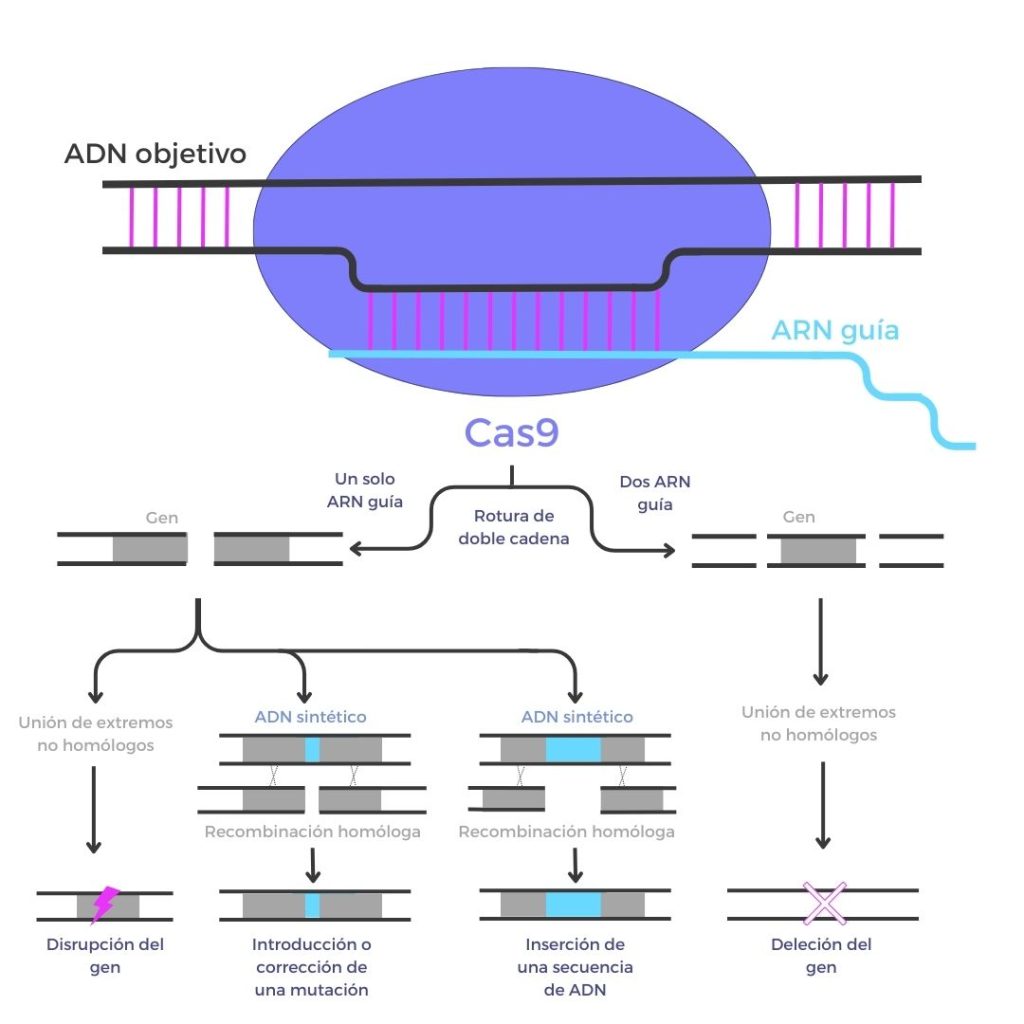
Tal y como se muestra en la figura, en primer lugar, el ARN guía posiciona la proteína Cas9 en el sitio de la secuencia que se haya elegido para el corte. Cas9 corta la doble cadena y, posteriormente, los mecanismos de reparación del ADN se encargan de reparar el corte. En este punto justo está la clave de las diferentes modificaciones que pueden realizarse con CRISPR-Cas9:
- Si no se proporciona un ADN molde con la secuencia que queremos, los mecanismos de reparación por extremos homólogos no siempre funcionan perfectamente, y es habitual que las cadenas de ADN pierdan alguna base. De esta forma, lo que se consigue es interrumpir un gen o secuencia de ADN.
- Si a los componentes del sistema CRISPR-Cas9 se añade un ADN molde sintético, los mecanismos de reparación pueden utilizarlo y por lo tanto introducir cambios concretos.
- Si se utilizan dos ARNs guía, pueden introducirse dos cortes y eliminar una región de interés.
Edición de bases
Esta tecnología CRISPR permite modificar una única base nitrogenada de una molécula de ADN. Para ello, este sistema utiliza una proteína Cas9 con la función de nucleasa desactivada (no puede cortar cadenas de ADN) y un dominio adicional capaz de modificar las bases nitrogenadas.
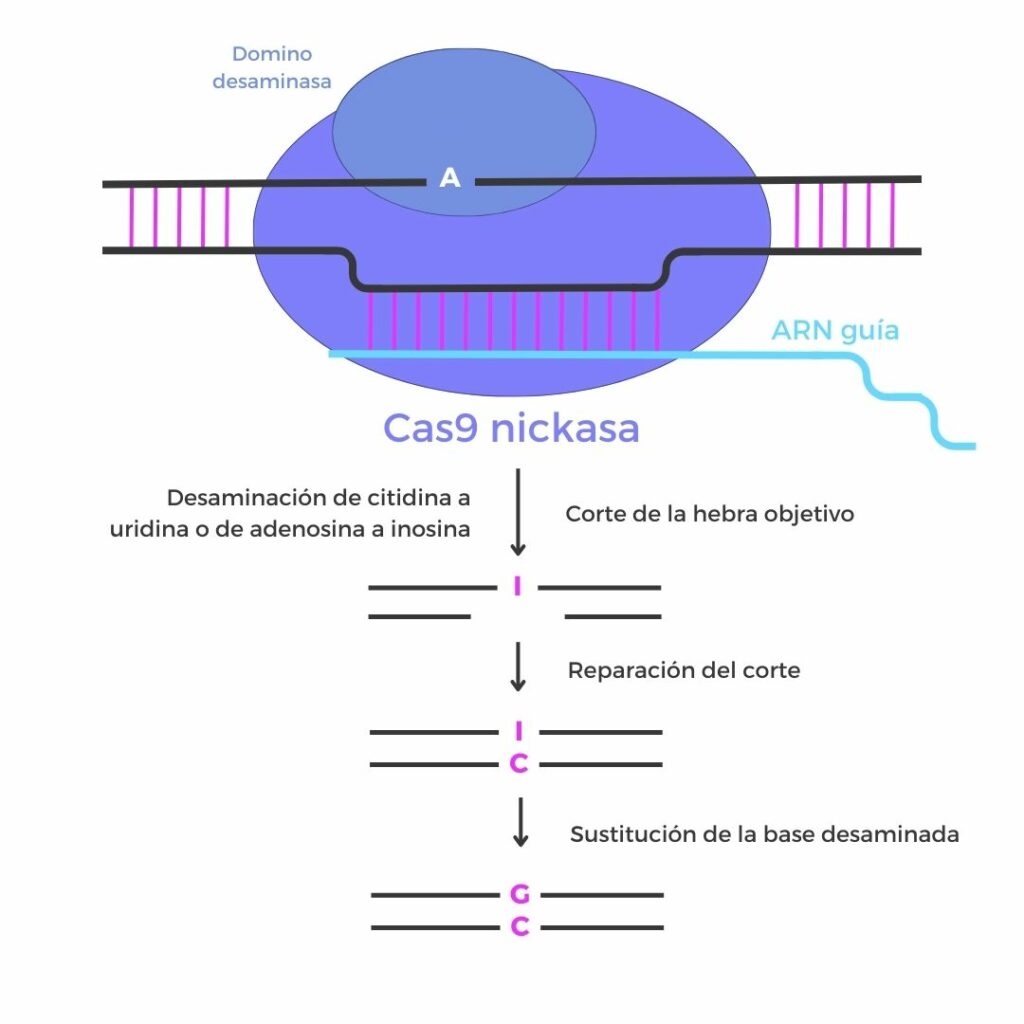
Las tecnologías de edición de bases son una herramienta prometedora, aunque tienen ciertas limitaciones. En primer lugar, solamente pueden realizar modificaciones concretas de nucleótidos (de Citosina a Timina, de Adenina a Guanina y de Citosina a Guanina). Por otro lado,su actividad está restringida a determinadas regiones del genoma debido a la dependencia de secuencias PAM (protospacer adjacent motif) cercanas, lo que impide, por el momento, su aplicación en cualquier posición de forma arbitraria.
Prime editing
Esta tecnología CRISPR mantiene la precisión y la eficiencia de los editores de bases, al tiempo que soluciona algunas de sus limitaciones, como la dependencia de secuencias PAM Se trata de una herramienta extremadamente versátil, gracias a la que es posible tanto realizar cambios de una sola base como provocar inserciones y deleciones de diferentes tamaños.
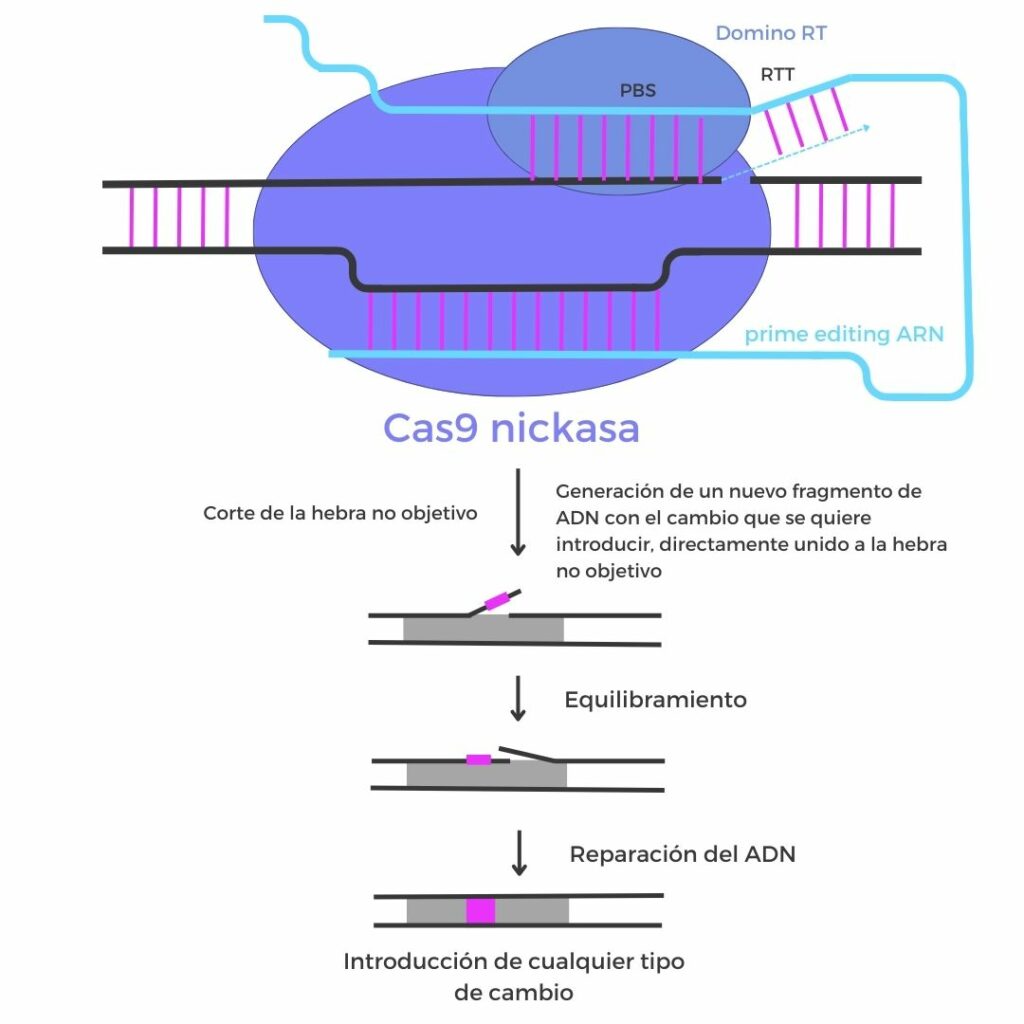
Como se aprecia en la figura anterior, en el prime editing, se utiliza una proteína Cas9 modificada (nickasa) fusionada a una transcriptasa inversa y un ARN guía especializado (pegRNA):
- El pegRNA dirige el complejo nickasa-transcriptasa inversa hasta la secuencia diana, a la vez que contiene la información del cambio genético que se quiere introducir en la secuencia.
- La nickasa realiza el corte en la secuencia de ADN objetivo.
- La transcriptasa inversa utiliza el pegRNA como molde para sintetizar la nueva secuencia directamente en la molécula de ADN objetivo.
Después de la actuación de estos tres componentes, los mecanismos celulares de reparación del ADN incorporan el cambio de forma estable.
PERT (Programmable Editing with Reverse Transcriptase)
PERT es una estrategia de edición genética basada en prime editing dirigida a la reprogramación de la traducción del ARN. Esto es interesante de cara a evitar las paradas prematuras en la traducción del ARNm características de ciertas enfermedades genéticas (p.e. la fibrosis quística o la enfermedad de Tay-Sachs) o a introducir aminoácidos alternativos.
Funciona de forma similar al prime editing, pero, en lugar de editar regiones codificantes del genoma, se edita la región correspondiente al anticodón de los ARN de transferencia. De este modo, las células, en lugar de detener la traducción al encontrarse un codón de parada prematuro, introducen un aminoácido alternativo.
Aunque todavía se encuentra en fases tempranas de desarrollo, representa una de las líneas más prometedoras dentro de la evolución de las herramientas CRISPR.
Edición del epigenoma
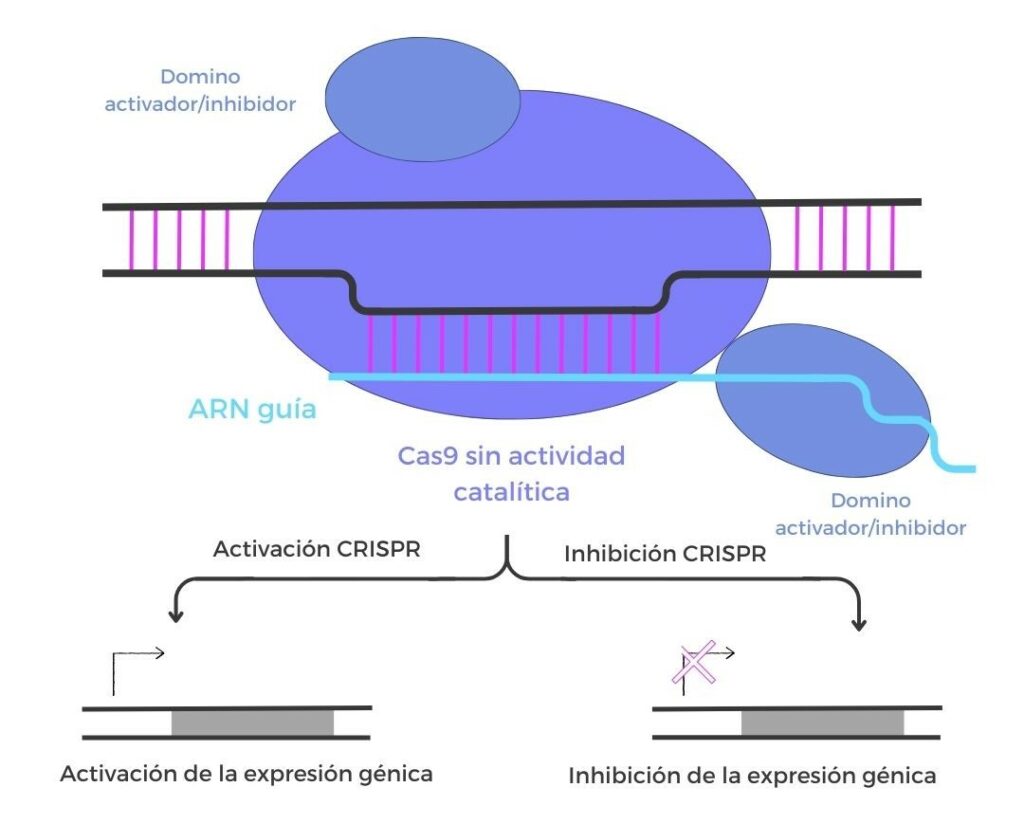
La tecnología CRISPR no solamente se ha aplicado a la edición genómica, sino que ha dado un paso más hacia la edición del epigenoma. Las herramientas CRISPR de edición epigenética utilizan una versión catalíticamente inactiva de Cas9 (dCas9), que conserva su capacidad de unirse a secuencias específicas del genoma guiada por un ARN, pero carece de actividad nucleasa. Esta proteína se fusiona a dominios efectores epigenéticos, como metilasas, desmetilasas, acetilasas o desacetilasas, capaces de modificar marcas epigenéticas en el ADN o en las histonas. De este modo, el sistema puede activar o silenciar genes de forma dirigida, dependiendo del tipo de modificación inducida.
Aplicaciones del CRISPR-Cas9 en medicina
Las herramientas CRISPR-Cas se han convertido en una tecnología muy prometedora para la edición genética capaz de editar, corregir y alterar el genoma y el epigenoma de una manera fácil, rápida, barata y altamente precisa. En la actualidad diferentes laboratorios trabajan para perfeccionar las herramientas CRISPR y adaptarlas a su utilización en la terapia e investigación de enfermedades.
CRISPR y terapias génicas: ejemplos reales
Durante los últimos años, las terapias génicas basadas en CRISPR han pasado de ser una idea prometedora a convertirse en una realidad clínica.
Uno de los hitos más importantes fue la aprobación de la primera terapia basada en CRISPR en 2023, para el tratamiento de enfermedades hematológicas como la anemia falciforme y la beta-talasemia. Esta terapia se basa en la edición genética de células madre hematopoyéticas del propio paciente para restaurar la producción de hemoglobina fetal.
Otro avance destacado ha sido el desarrollo exitoso de una terapia CRISPR personalizada para tratar a un niño con una enfermedad genética rara. Esto, sumado a los resultados prometedores de los primeros estudios clínicos con prime editing demuestra el gran potencial del tratamiento con terapias CRISPR en casos de enfermedades raras.
Actualmente existen muchísimos otros ensayos clínicos basados en tecnologías CRISPR en marcha para tratar diferentes patologías, incluyendo enfermedades hematológicas, cáncer, trastornos metabólicos o enfermedades raras.
CRISPR en detección de ácidos nucleicos
Otra de las aplicaciones más interesantes de CRISPR en medicina es su uso como herramienta de detección de secuencias específicas de ácidos nucleícos.
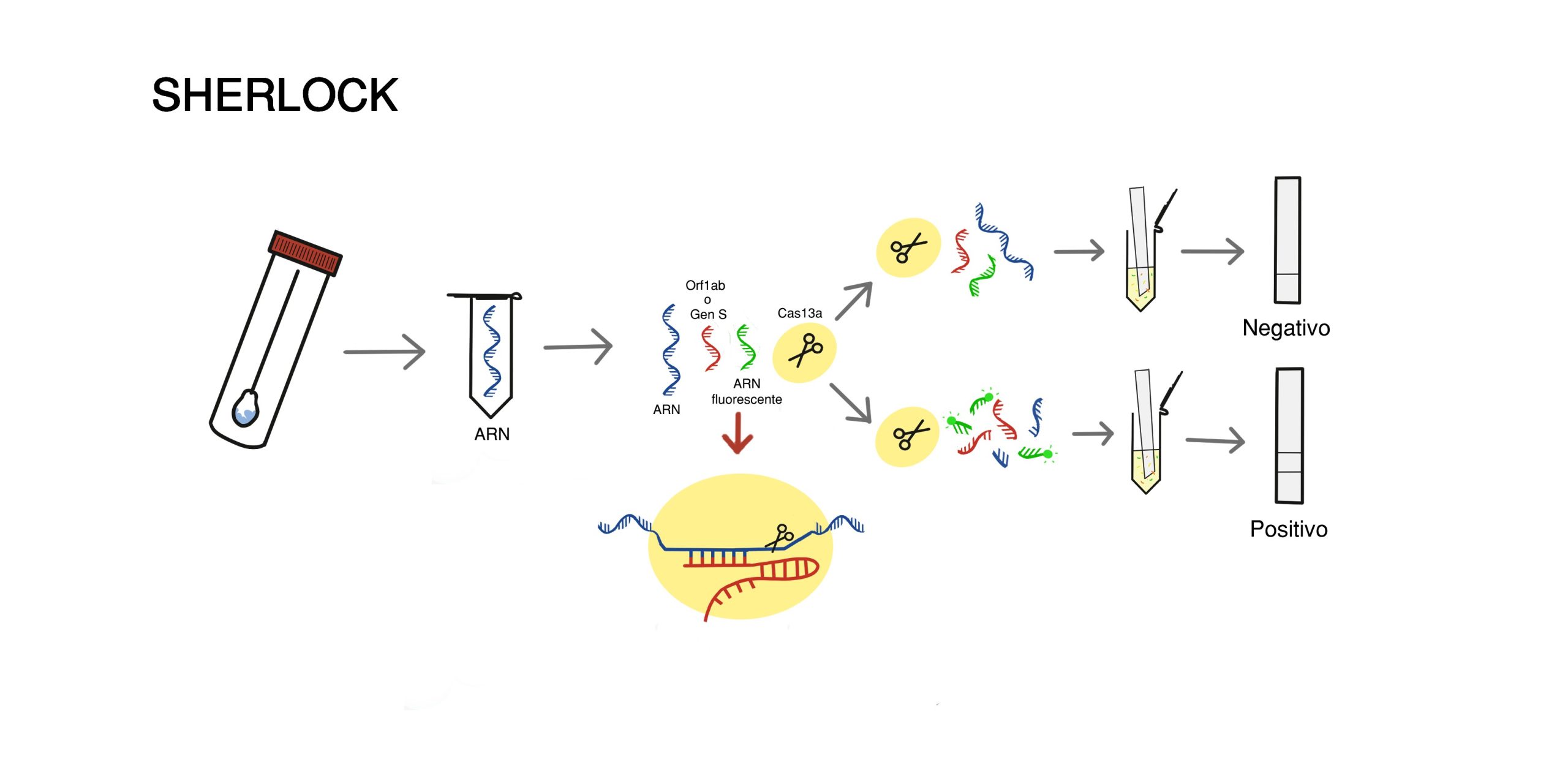
Algunas proteínas Cas, como Cas12a o Cas13a, pueden reconocer secuencias específicas de ADN o ARN y, una vez activadas, cortar otras moléculas cercanas de forma indiscriminada. Este fenómeno se ha aprovechado para desarrollar sistemas de detección molecular extremadamente sensibles.
Tecnologías como SHERLOCK o DETECTR permiten detectar patógenos, virus o mutaciones genéticas con una gran precisión y rapidez. Estas herramientas han demostrado ser especialmente útiles en el desarrollo de test diagnósticos rápidos para enfermedades infecciosas.
CRISPR en investigación biomédica
CRISPR también se ha convertido en una herramienta fundamental para la investigación biomédica. Gracias a su facilidad de uso y su elevada eficiencia, los investigadores pueden estudiar la función de genes concretos, modelar enfermedades humanas en el laboratorio o identificar nuevas dianas terapéuticas.
Por ejemplo, en el contexto de la generación de modelos celulares, es posible introducir, mediante CRISPR, mutaciones asociadas a enfermedades en células madre pluripotentes inducidas (iPSCs) y posteriormente diferenciarlas en diferentes tipos celulares para estudiar cómo afecta la mutación a cada tejido.
Otra aplicación emergente es el uso de CRISPR para modificar el genoma de animales (especialmente en cerdos) con el objetivo de generar órganos compatibles para xenotrasplantes. Mediante edición genómica es posible inactivar genes porcinos que desencadenan rechazo inmunológico en humanos o introducir genes humanos para mejorar la aceptación del órgano.
Desafíos actuales y perspectivas futuras de CRISPR en salud
A pesar de su enorme potencial, las tecnologías CRISPR todavía presentan algunos desafíos importantes. Uno de los principales retos es mejorar la especificidad de la edición genética, ya que en algunos casos pueden producirse modificaciones no deseadas en regiones del genoma distintas a la secuencia objetivo (los llamados efectos off-target).
Otro desafío clave es el desarrollo de sistemas de entrega eficientes y seguros, capaces de transportar los componentes CRISPR hasta las células y tejidos adecuados dentro del organismo.
Además, el uso de tecnologías de edición genética plantea importantes cuestiones éticas, especialmente en lo que respecta a la edición de la línea germinal humana.
A pesar de estas limitaciones, todo apunta a que las tecnologías CRISPR seguirán evolucionando rápidamente durante los próximos años, consolidándose como una de las herramientas más potentes de la medicina molecular y la biotecnología.
Si os interesa la edición genómica y queréis profundizar más en su utilización en salud, te recomendamos el programa “Introducción a la Terapia Génica y Edición del Genoma”. Y si quieres algo más aplicado, entonces te interesa nuestro curso “Edición del Genoma mediante CRISPR y células madre pluripotentes inducidas en la investigación de enfermedades genéticas”. ¡Nos leemos en el siguiente post!
Artículos de interés:
Musunuru K. CRISPR and cardiovascular diseases. Cardiovasc Res. 2023 Mar 17;119(1):79-93. doi: 10.1093/cvr/cvac048
Nicosia L, Harrison PT. CRISPR for cystic fibrosis: Advances and insights from a systematic review. Mol Ther. 2025 Sep 3;33(9):4091-4112. doi: 10.1016/j.ymthe.2025.06.021
CRISPR en Medicina: https://innovativegenomics.org/es/crisprpedia/crispr-en-medicina/#Nucleic-acid-detection
