Vivimos en una sociedad donde se pueden desconocer muchas cosas, pero es raro que el alcohol sea una de ellas. Esta molécula orgánica de fórmula C2H6O, que lleva acompañando al hombre mas de 13.000 años, es el liquido incoloro, volátil e inflamable que más ha condicionado al ser humano en la historia. Subamos la apuesta, el líquido incoloro después del agua que más ha condicionado al ser humano. Se trata de una droga recreativa y psicoactiva tan popular que da nombre a un grupo entero de bebidas, las bebidas alcohólicas, y algunas teorías sostienen que fue uno de los condicionantes del desarrollo de la agricultura en las sociedades primitivas.
Se trata de una molécula pequeña, que solo es capaz de “relacionarse” mediante puentes de hidrogeno y débiles interacciones hidrofóbicas. Debido a esto, carece de auténticas dianas sobre las que actuar en el organismo humano.
Desgraciadamente, ese mismo organismo humano lo compensa en ocasiones con un consumo desorbitado, que, unido a la capacidad del alcohol de disolverse en el agua, le permite llegar a casi todas las regiones del cuerpo, incluyendo el interior celular. Una vez dentro de la célula, uno de sus efectos negativos es su capacidad de realizar cambios epigenéticos. Los cambios epigenéticos son formas de modificar la expresión génica sin modificar para ello la estructura del ADN. E incluso aquí el alcohol es capaz de meter mano.
La triada epigenética: metilación, histonas y microARNs
Uno de los cambios epigenéticos más interesantes provocados por el alcohol se encuentra en la metilación del ADN. Recientemente (en estos campos de estudio, 2015 cuenta como “reciente”) el grupo de Estelle Barbier comprobó que los niveles de la enzima ADN (citosina-5)-metiltransferasa 1 (DNMT1) estaban incrementados en la corteza prefrontal de ratas con historial de dependencia alcohólica, borrachas habituales en lenguaje coloquial, lo que conllevaba una hipermetilación del ADN y una reducción de su expresión génica. Sin embargo, cuando inhibieron la actividad de la DNMT1 y restablecieron la expresión de los genes a sus valores normales, inhibieron también el aumento en el consumo de alcohol que ocurre por parte de animales dependientes.
Esta misma enzima DNMT1 se encontraba también aumentada en el núcleo accumbens de ratones con historial alcohólico. “Pero que ocurra en ratones no se puede extrapolar automáticamente al ser humano” podríamos pensar, y con razón. Pero son descubrimientos que deben verse en conjunto, con las alteraciones comprobadas en estudios previos en los niveles de metilación de diversos genes encontrados en personas con dependencia alcohólica, genes que transcriben proteínas tan importantes como el factor de crecimiento nervioso (NGF, cuyo hallazgo fue ganador de un Nobel, pero eso es otra historia) o el factor neurotrófico derivado del cerebro (BDNF).
Si el alcohol causa una metilación del ADN, de forma sencilla, en cambio con las histonas es complicado. Múltiples estudios, la mayoría en roedores, mártires de las ciencias naturales, han comprobado que los individuos a los que más les gusta darle a la bebida presentaban en regiones del cerebro un aumento de la actividad de algunas histonas deacetilasas (HDAC) y por ende niveles reducidos de acetilación en las histonas H3 y H4. Una baja acetilación de las histonas es sinónimo de un aumento de la carga eléctrica positiva en ellas, fortaleciendo su unión con el ADN, de carga negativa (debido a los grupos fosfato que posee), condensándolo y dificultando la transcripción de esas zonas de genoma.

Sin embargo, otros estudios han visto como otras regiones nerviosas (del Sistema Nervioso, no que fueran zonas en ese estado de ánimo) presentaban, al contrario, un aumento de la acetilación, aunque no por el alcohol propiamente. El acetato, producto final del metabolismo alcohólico, es bastante inofensivo por sí mismo, pero al convertirse en acetil-CoA aumenta la acetilación de las histonas; las histonas acetiltransferasas (HAT) acetilan lisinas en las histonas (tiene sentido, viene en su nombre) cogiendo los grupos acetilo de moléculas de acetil-CoA. Se teoriza que precisamente uno de los principales responsables de las conductas adictivas derivadas del alcohol, y la ansiedad que se sufre en la abstinencia, están relacionados a una excesiva acetilación en la amígdala, que es seguida por su opuesto, una descontrolada desacetilación cuando el consumo desaparece, por la actividad compensatoria de las HDAC.
Por supuesto los microARNs, actores clave en la epigenética, no escapan tampoco de los efectos del etanol. Si bien este tema requeriría su propio articulo (tiene reviews enteras dedicadas a ello), baste con decir que los perfiles de expresión de microARNs entre personas alcohólicas crónicas y no consumidores presentan diferencias, siendo un estudio de gran interés dentro del Sistema Nervioso Central por su relevancia en el comportamiento del consumidor y el desarrollo de la adicción. Teniendo en cuenta que un mismo microARN es capaz de interactuar con varios RNA mensajeros distintos, y que la interacción puede ser además distinta según el RNA al que se una, con solo cambiar la expresión de unos pocos microARNs, sus implicaciones celulares pueden ser enormes.
Los metabolitos del alcohol se unen a la fiesta
Por si el alcohol no fuera suficiente por si mismo, su propio metabolismo crea compuestos con capacidad epigenética, como la acetil-CoA mencionada anteriormente proveniente del acetato. La generación de especies reactivas del oxígeno durante la eliminación del alcohol induce alteraciones en los patrones de metilación del ADN. El acetaldehído, primer compuesto producido en la degradación del alcohol, es un carcinógeno tipo 1 que, entre otros daños, causa la acetilación de la histona H3 en la posición Lys9.
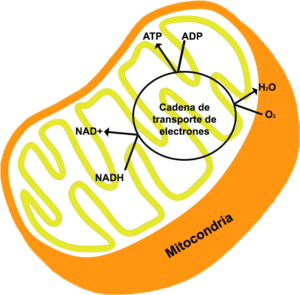
Incluso el aumento en la cantidad de NADH al descomponer el alcohol (es precisamente la producción de NADH en la degradación de alcohol lo que le otorga su alto valor calórico) tiene efectos epigenéticos. En un breve inciso, NADH es la forma reducida de la nicotinamida adenina dinucleótido (NAD), mientras que NAD+ es su forma oxidada. Dos caras de la misma moneda. NAD es una coenzima importante en muchas reacciones orgánicas, y conocida sobre todo por ser la molécula que transporta hidrógeno a la mitocondria en su forma reducida, the powerhouse of the cell, para que ella produzca energía y NAD pase a la forma oxidada. Un aumento de NADH conlleva un descenso en su forma oxidada, NAD+, que tiene repercusiones negativas en la actividad de SIRT1 y SIRT6, dos HDAC. Ambas enzimas tienen también menos rendimiento en personas envejecidas o con diabetes, por lo que estos datos no parecen buenos.
Las células trabajan en un equilibrio que intentan conservar, una homeostasis que cuando se rompe es poco probable que sea para mejor. Mejor no tocarlo entonces.
Si te ha gustado este post y te interesa la Epigenética , no puedes perderte nuestro programa formativo «Epigenética en Medicina». En él, aprenderás acerca de los mecanismos epigenéticos y su influencia en el desarrollo de enfermedades, además de otros factores ambientales que pueden modificar el epigenoma.
Bibliografía
Pandey, S. C., & Bohnsack, J. P. (2020). Alcohol Makes Its Epigenetic Marks. Cell Metabolism, 31(2), 213–214. https://doi.org/10.1016/j.cmet.2020.01.008
Pandey, S. C., Kyzar, E. J., & Zhang, H. (2017). Epigenetic basis of the dark side of alcohol addiction. Neuropharmacology (Vol. 122, pp. 74–84). https://doi.org/10.1016/j.neuropharm.2017.02.002
Ron, D., & Barak, S. (2016). Molecular mechanisms underlying alcohol-drinking behaviours. Nature Reviews Neuroscience (Vol. 17, Issue 9, pp. 576–591. https://doi.org/10.1038/nrn.2016.85
Etchegaray, J. P., & Mostoslavsky, R. (2016). Interplay between Metabolism and Epigenetics: A Nuclear Adaptation to Environmental Changes. Molecular Cell (Vol. 62, Issue 5, pp. 695–711). https://doi.org/10.1016/j.molcel.2016.05.029
Shukla, S.D., Lee, Y.J., Park, P.-h. and Aroor, A.R. (2006). Acetaldehyde Alters MAP Kinase Signalling and Epigenetic Histone Modifications in Hepatocytes. In Acetaldehyde-Related Pathology: Bridging the Trans-Disciplinary Divide (eds Novartis Foundation, D.J. Chadwick and J. Goode). https://doi.org/10.1002/9780470511848.ch16

