A lo largo de más de un siglo, los Premios Nobel han reconocido avances que hoy son la base de la medicina moderna: la estructura del ADN, el código genético, las técnicas de secuenciación o la edición génica. En este post repasamos los diferentes Nobel de Genética, lo que implica un paseo por la evolución de una disciplina que ha cambiado la forma en que entendemos la salud, la enfermedad y el futuro de la medicina.
Premios Nobel en las décadas de 1930-1950
La historia de los Nobeles de la Genética se inicia en 1933 con Thomas H Morgan, quien recibió el Premio Nobel de Fisiología o Medicina por sus descubrimientos en el papel de los cromosomas en la herencia. El trabajo de Morgan confirmó que los genes están ubicados a lo largo los cromosomas, en el interior del núcleo de las células. Además, Morgan fue el primero en descubrir el fenómeno de entrecruzamiento, por el cual cromosomas diferentes pueden intercambiar material hereditario.
El siguiente investigador galardonado con un premio Nobel en el campo de la Genética fue Hermann Muller, quien recibió el premio el Premio Nobel de Medicina en 1946 por su descubrimiento de la producción de mutaciones por medio de la radiación con rayos X. Muller observó que al exponer las moscas de la fruta, las famosas Drosophilas, a rayos X, presentaban un mayor número de mutaciones en su material hereditario. Además estimó que la cantidad de estas mutaciones era dependiente de la dosis ionizante utilizada.
Los trabajos de Muller serían clave para iniciar el estudio de los mecanismos, espontáneos o inducidos, que llevan a la aparición de mutaciones y su importancia en la evolución de las especies, así como los efectos biológicos de la radiación.
Premios Nobel en las décadas de 1950
En 1958 el Premio Nobel de Medicina fue para George Beadle y Edward Tatum, por su descubrimiento de que los genes actúan regulando reacciones químicas definidas y Joshua Lederberg, quien lo recibió por sus descubrimientos relacionados con la recombinación genética y organización del material hereditario en bacterias.
Beadle y Tatum describieron cómo los genes controlan las rutas bioquímicas en sus diferentes pasos, a través de la regulación de la expresión de las enzimas y sustancias que participan en dichas rutas. Los resultados de sus trabajos abrieron un nuevo camino hacia el estudio de la función de los genes y el metabolismo celular. El trabajo de Lederberg contribuyó a mejorar el conocimiento de la genética bacteriana, y reveló que las bacterias son susceptibles de aceptar material genético. Se abría por primera vez la posibilidad de introducir genes en un organismo.
En la parada de los Premios Nobel de la genética de 1959 encontramos la primera (y única) contribución de origen español. En ese año, Severo Ochoa compartió el deseado galardón con Arthur Kornberg por sus descubrimientos de los mecanismos de la síntesis biológica del ácido ribonucleico y el ácido desoxirribonucleico.
Dentro de su extensa vida investigadora Severo Ochoa estudió cómo se sintetiza el ácido ribonucleico (ARN) y el ácido desoxirribonucleico (ADN) y qué enzimas participan en este proceso. Su trabajo hizo posible la obtención de polinucleótidos sintéticos de distinta composición en bases nitrogenadas, que serían clave para desvelar el código genético. Kornberg, que había sido discípulo de Ochoa describió como se copia el ADN a partir de ADN. Además, aisló la enzima ADN polimerasa, encargada de sintetizar el ADN, esencial para su replicación y reparación.
Premio Nobel para la Estructura del ADN
Aunque la estructura del ADN fuera descrita en 1953, no fue hasta 1962 cuando Francis Crick, James Watson and Maurice Wilkins recibieron el Premio Nobel de Medicina por sus descubrimientos acerca de la estructura molecular de los ácidos nucleicos y su significado para la transferencia de la información en seres vivos.
Watson, Crick y Wilkins pasaron al Olimpo de la Ciencia por ser los primeros en obtener y describir la estructura en doble hélice del ADN. No podemos dejar de mencionar aquí a Rosalind Franklin, cuya contribución al descubrimiento fue clave y esencial para determinar que el ADN se compone de dos cadenas antiparalelas opuestas en una hélice, en la que las bases nitrogenadas quedan en el interior y los grupos fosfatos que las unen están expuestos hacia fuera.
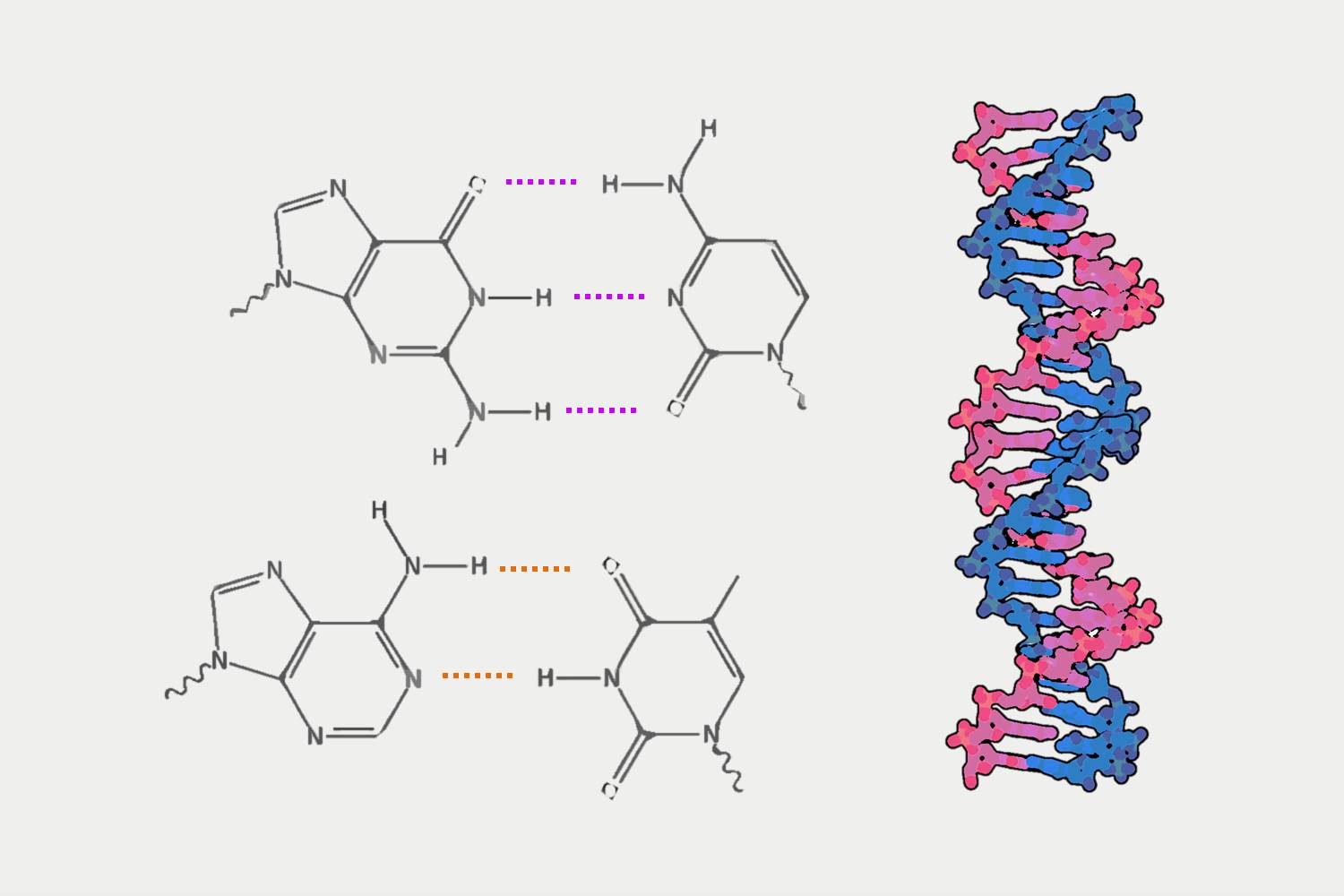
Lamentablemente, Franklin había fallecido en 1958, por lo que, teniendo en cuenta que los premios Nobel no se otorgan a título póstumo, su aportación no pudo siquiera ser considerada para el premio. Además de la gran importancia de la determinación de la estructura del ADN, los trabajos de Watson, Crick y Wilkins proporcionaron el concepto para entender el mecanismo por el cual el ADN puede copiarse y transmitirse a las células hijas: la doble hélice y la complementariedad de las bases.
Síntesis de proteínas, virus y código genético: Otros Premios Nobel de Genética de la Década de 1960
Los siguientes investigadores del área de la Genética en recibir un premio Nobel fueron François Jacob, André Lwoff y Jacques Monod, en 1965, por sus descubrimientos sobre el control genético de la síntesis de enzimas y virus.
Jacob y Monod describieron cómo la información contenida en el ADN es transferida a una molécula mensajera de ARN, como paso previo a la traducción a proteínas y cómo la expresión de los genes es regulada por la acción de los mismos en diferentes células. Por su parte André Lwoff describió cómo los genes de los bacteriófagos pueden incorporarse al material genético de las bacterias que infectan y permanecer latentes hasta que un agente activador induce la formación de un nuevo fago.
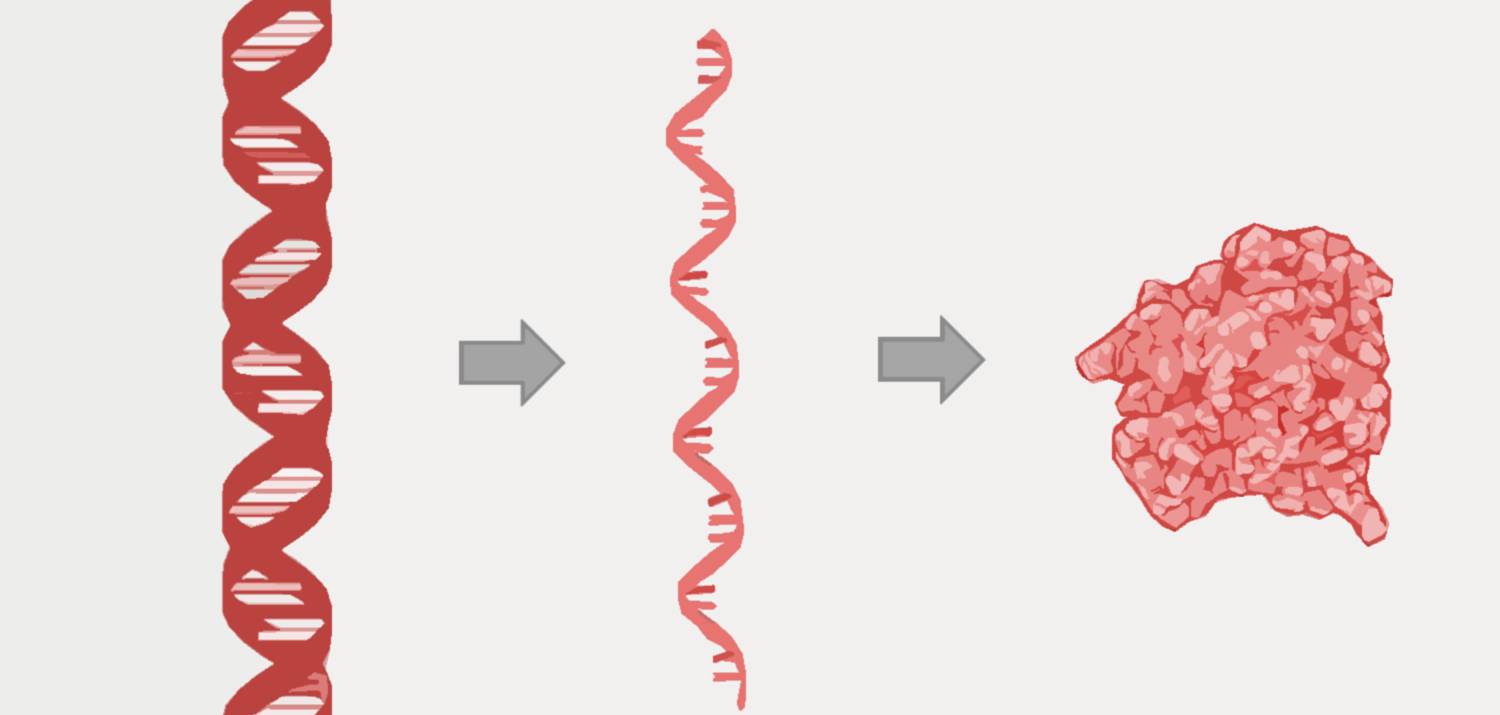
Robert Holley, Har Khorana y Marshal W. Nirenber recibieron el Premio Nobel de Medicina en 1968 por su interpretación del código genético y su función en la síntesis proteica. Los investigadores llevaron a cabo importantes descubrimientos sobre cómo se transportan los aminoácidos hacia el ribosoma, que es la máquina celular donde se sintetizan las proteínas.
Holley fue la primera persona en aislar el ARN de transferencia y posteriormente, su equipo contribuyó a caracterizar su estructura. Nirenber fue pionero en desvelar el lenguaje del código genético, al obtener un péptido formado por repeticiones del mismo aminoácido de una cadena de ARN con la misma repetición de trinucleótidos. Más tarde, el equipo de Khorana, asumió la intensa labor de caracterizar de forma sistemática el resto del código genético.
Un año más tarde, en 1969, Max Delbrück, Alfred D. Hershey y Salvador E. Luria recibieron el Premio Nobel de Medicina por sus descubrimientos sobre el mecanismo de replicación y estructura genética de los virus. A través de múltiples trabajos en colaboración, los investigadores respondieron a diversas cuestiones pendientes sobre el funcionamiento de los bacteriófagos, como por ejemplo la introducción de únicamente su material hereditario en la célula infectada y la capacidad de éste para la reproducción del bacteriófago. También destacan los experimentos de Hershey, junto con Martha Chase que fueron claves para confirmar al ADN como molécula portadora de la información hereditaria.
Nobel de Genética en la década de 1970
En 1975, los galardonados David Baltimore, Renato Dulbecco y Howard Temin descubrieron que algunos virus pueden integrar su material genético en el ADN de las células anfitrionas.
El Premio Nobel de Medicina de 1975, que fue otorgado a David Baltimore, Renato Dulbecco y Howard Temin, por sus descubrimientos sobre la interacción entre los virus que causan tumores y el material genético de la célula.
El equipo de Renato Dulbecco probó en los años cincuenta que el material genético del virus pasa a formar parte de los genes del organismo hospedador. También demostró que los genes integrados en las células infectadas, así como la presencia de mutaciones somáticas pueden inducir crecimiento anormal.
Por su parte, David Baltimore y Howar Temin descubrieron, de forma independiente, que los virus de ARN también pueden introducir su material hereditario en el ADN de las células, gracias a la acción de una enzima denominada transcriptasa reversa, que tiene la capacidad de crear una copia de ADN a partir de una molécula de ARN. Estos resultados desafiaron el dogma central de la biología molecular, según el cual la información genética fluye únicamente en una dirección, desde el ADN al ARN y de ahí a las proteínas. En conjunto, las aportaciones de Dulbecco, Baltimore y Temin abrieron un nuevo camino, no sólo hacia una de las causas del cáncer, sino también hacia su prevención.
El Premio Nobel de Medicina de 1978 fue otorgado a Werner Arber, Daniel Nathans y Hamilton O. Smith, por el descubrimiento de las enzimas de restricción y sus aplicaciones a los problemas de la genética molecular.
A principios de los años 60, Arber había descubierto las enzimas de restricción, enzimas que cortan el ADN en posiciones concretas, determinadas por la secuencia de nucleótidos que reconocen. Smith confirmó los resultados de Arber y demostró que las enzimas de restricción cortan el ADN en el centro de secuencias simétricas de nucleótidos. Posteriormente, Nathans fue el primero en utilizar las enzimas de restricción para resolver un problema genético, la caracterización del genoma del virus SV40. El descubrimiento de las enzimas de restricción supuso la posibilidad de cortar el ADN en posiciones concretas y abrió la puerta al campo de la Ingeniería Genética y el desarrollo de la Biotecnología.
Nobel de Genética en la década de 1980
Nobel para el ADN Recombinante, secuenciación y genética del sistema inmunitario
En 1980 tanto el premio Nobel de Química como el Medicina fueron otorgados a investigadores del área de la genética. Paul Berg recibió el premio Nobel de Química por sus estudios fundamentales de la bioquímica de los ácidos nucleicos, en particular al ADN recombinante. El premio fue compartido con Walter Gilbert y Frederic Sanger por sus contribuciones a la determinación de la secuencia de bases en los ácidos nucleicos, lo que se conoce ahora como “secuenciación del ADN”. Berg fue el primer investigador en realizar manipulación genética y obtener una molécula de ADN recombinante constituida por fragmentos de ADN de diferentes especies. Por su parte Gilbert y Sanger desarrollaron los primeros métodos de secuenciación del ADN.
En cuanto al Premio Nobel de Medicina de 1980, éste fue otorgado a Baruj Benacerraf, Jean Dausset y George D. Snell, por sus descubrimientos sobre las estructuras determinadas genéticamente que se localizan sobre la superficie celular y regulan las reacciones inmunológicas, los genes responsables del complejo mayor de histocompatibilidad.
En 1982, el premio Nobel de Química fue otorgado a Aaron Klug por su desarrollo de la microscopía de electrones en cristalografía y su determinación de la estructura de complejos de proteína y ácidos nucleicos con importancia biológica. Las imágenes obtenidas mediante el método desarrollado por el investigador mejoraron el conocimiento de algunas de las estructuras con función biológica necesarias para el correcto funcionamiento de la célula.
Nobel para elementos transponibles, la genética de los anticuerpos, las propiedades catalíticas del ARN y los oncogenes
No es hasta 1983 que encontramos una mujer en la lista de premios Nobel en genética. Ese año Barbara McClintock recibió el Premio Nobel de Fisiología o Medicina por su descubrimiento de los elementos genéticos móviles, que solemos llamar transposones. La investigadora fue la primera en probar la existencia de elementos genéticos que modifican su posición en un cromosoma y que pueden provocar la activación de genes en su nueva localización.
Tres años después, en 1987, Susum Tonegawa, recibió el Premio Nobel de Fisiología o Medicina por su descubrimiento del principio genético para la generación de diversidad de anticuerpos. El investigador describió cómo se pueden obtener cientos de millones de anticuerpos diferentes a partir de la redistribución de un pequeño conjunto de genes durante el desarrollo de los linfocitos productores de anticuerpos.
El premio Nobel de Química de 1989 que fue otorgado a Sidney Altman y Thomas R. Cech por su descubrimiento de las propiedades catalíticas del ARN. Los investigadores demostraron que el ARN, hasta entonces considerado únicamente como una molécula portadora de información hereditaria, también podía ejercer funciones como enzima y cortar otras moléculas de ARN.
Ese mismo año, el Premio Nobel de Medicina fue recibido por J. Michael Bishop y Harold E. Varmus, por su descubrimiento del origen celular de los oncogenes retrovirales. Los investigadores fueron los primeros en describir los oncogenes y señalar que el cáncer puede ser producido tanto por virus como por la activación de los propios genes (oncogenes) del organismo.
Década de 1990
El año 1993 el premio Premio Nobel de Medicina fue otorgado a Richard J. Roberts y Phillip A. Sharp por sus descubrimientos sobre el procesamiento de los genes. Los investigadores mostraron que los genes están interrumpidos y formados por exones e intrones y que la molécula de ARN mensajero sufre un proceso de eliminación de intrones y unión de exones durante su maduración. Una consecuencia de este proceso es la existencia de procesamiento alternativo, mecanismo por el que de un mismo gen pueden obtenerse diferentes productos proteicos, según se utilizan unos exones u otros.
Ese mismo año Kary B Mullis y Michael Smith compartían el premio Nobel de Química por sus contribuciones al desarrollo de métodos basados en el ADN. Mullis recibió el premio por la invención de la Reacción en Cadena de la Polimerasa, técnica de amplificación del ADN conocida en todo laboratorio de Genética. Smith lo recibió por sus contribuciones al establecimiento de la mutagénesis dirigida de oligonucleótidos y su desarrollo en estudios de proteínas.
Dos años después, en 1995, Edward B. Lewis, Christiane Nüsslein-Volhard y Eric F. Wieschaus recibieron el Premio Nobel de Medicina, por sus descubrimientos en el control genético del desarrollo embrionario temprano. Los tres investigadores realizaron diferentes aportaciones sobre los genes que dirigen el desarrollo de diferentes órganos en Drosophila.
Década del 2000
Nobel para la regulación genética del desarrollo, receptores olfativos y ARN de interferencia
La década de los 2000 fue fructífera en cuanto a desarrollo de investigaciones sobre genética. En 2002 Sydney Brenner, John Sulston y Robert Horvitz recibieron el Premio Nobel de Fisiología o Medicina por sus descubrimientos sobre la regulación genética del desarrollo de los órganos y la muerte celular programada. Los trabajos de los tres investigadores estudiando un gusano de laboratorio (Caernohabditis elegans) permitieron determinar que la muerte celular programada forma parte del proceso normal de diferenciación, así como identificar qué genes clave interaccionan en la muerte celular programada.
En 2004, Richard Axel y Linda Buck compartieron el Premio Nobel de Medicina por sus descubrimientos de los receptores olfativos y la organización del sistema olfativo. Los investigadores mostraron cómo cientos de genes codifican para los sensores olfativos situados en las neuronas olfativas sensoriales de la nariz. También resolvieron cómo la recepción de estímulos olfativos por los diferentes sensores provoca señales eléctricas que son enviadas e interpretadas en el cerebro.
Dos años después, en 2006 Andrew Z. Fire y Craig C. Mello recibieron el Premio Nobel de Medicina por su descubrimiento del ARN de interferencia y silenciamiento génico mediante ARN de doble cadena. Fire y Mello describieron un nuevo mecanismo de degradación de los ARN mensajeros de genes concretos basado en la unión de ARN complementario al ARN mensajero. El trabajo de Fire y Mello sería crucial para el desarrollo de una nueva herramienta para silenciar genes en biología y medicina.
Ese mismo año Roger D. Kornberg recibió el premio Nobel de la Química por sus estudios sobre las bases moleculares de la transcripción eucariótica. Kornberg fue el primero en caracterizar el proceso de transcripción (transferencia de la información del ADN al ARN) en eucariotas, determinó la estructura de la enzima responsable, la ARN polimerasa, y obtuvo imágenes detalladas de la síntesis de ARN a partir de ADN. Curiosamente, Roger D Kornberg había estado presente en la ceremonia en la que su padre, Arthur Kornberg, recibió el mismo premio por sus trabajos con la ADN polimerasa.
Nobel para la creación de animales modificados genéticamente y los telómeros
En 2007 el Premio Nobel de Medicina fue otorgado a Mario R. Capecchi, Martin J. Evans y Oliver Smithies, por sus descubrimientos de los principios para introducir modificaciones genéticas específicas en ratones mediante la utilización de células madre embrionarias. Fruto del trabajo de los tres investigadores fue posible generar múltiples modelos de enfermedades genéticas en ratón, así como determinar la función de otros genes.

Dos años después, en 2009, Elizabeth H. Blackburn, Carol W. Greider y Jack W. Szostak recibieron el Premio Nobel de Medicina por el descubrimiento de cómo son protegidos los cromosomas por los telómeros y la enzima telomerasa. Los resultados de los tres investigadores fueron clave para conocer uno de los mecanismos fundamentales de la célula, cómo se dividen los cromosomas y como se mantiene su integridad. Estudios posteriores de estos y otros investigadores revelaron el papel de los telómeros en el envejecimiento y su potencial como diana de tratamiento de diversas enfermedades humanas, incluido el cáncer.

Premios Nobel relacionados con la Genética en la década de los 2010
2012 – Nobel de Medicina para la reprogramación de células maduras en células pluripotentes
John B. Gurdon y Shinya Yamanaka demostraron que las células adultas pueden ser reprogramadas para convertirse en células madre pluripotentes. Este hallazgo abre la posibilidad de generar órganos para trasplantes sin el uso de células madre embrionarias.
2013 – Nobel de Medicina para la regulación del tráfico de vesículas en células
Randy W. Scheckman, James E. Rothman y Thomas C. Südhof descubrieron cómo las células regulan el tráfico de vesículas, que transportan sustancias dentro de la célula, demostrando que alteraciones en este proceso pueden causar enfermedades.
2015 – Nobel de Química para los mecanismos de reparación del ADN
Tomas Lindahl, Paul Modrich y Aziz Sancar descubrieron los mecanismos que utilizan las células para reparar el ADN dañado, lo que es esencial para mantener la estabilidad genética. Este descubrimiento ha sido clave para entender cómo las células previenen el cáncer y para el desarrollo de tratamientos de terapia génica. Puedes consultar nuestro artículo para conocer más aspectos sobre los Premios Nobel desde 1989 hasta 2015.
2017 – Nobel de Medicina para el Reloj Circadiano
En 2017, Jeffrey C. Hall, Michael Rosbash y Michael W. Young recibieron el Premio Nobel de Medicina por sus descubrimientos sobre los mecanismos moleculares que controlan los ritmos circadianos. El trabajo fue clave para entender cómo se sincroniza el reloj biológico interno con las diferentes fases del día.
2018 – Nobel de Medicina para la Inmunoterapia
En 2018, James P. Allison y Tasuku Honjo recibieron el Premio Nobel de Medicina por sus descubrimientos sobre la inmunoterapia, estrategia frente al cáncer basada en la regulación del sistema inmunitario. Además, supuso un punto de partida para el desarrollo de nuevos ensayos clínicos, algunos de los cuales ya son tratamientos aprobados.
2018 – Nobel de Química para la evolución aplicada a la biotecnología y medicina
Mediante diferentes estrategias, Frances H. Arnold, George P Smith y Sir Gregory P. Winter consiguieron reproducir la evolución en laboratorio para mejorar y generar nuevas proteínas con las que resolver diferentes problemas.
Arnold recibió el premio por sentar las bases de la evolución dirigida de enzimas. Smith y Winter desarrollaron una técnica conocida como “phage display” que ha permitido el desarrollo de anticuerpos con aplicaciones terapéuticas.
2019 – Nobel de Medicina para la respuesta celular a la disponibilidad de oxígeno
En 2019, William G. Kaelin Jr., Sir Peter J. Ratcliffe y Gregg L. Semenza descubrieron cómo se adaptan las células a la disponibilidad de oxígeno. Los tres investigadores contribuyeron a caracterizar la regulación de la expresión del gen EPO dependiente de los niveles de oxígeno y abrieron un camino para el desarrollo de tratamientos destinados a regularlo.
Premios Nobel relacionados con la Genética en la década de los 2020
2020 – Nobel de Medicina para el virus de la hepatitis C
Los investigadores Harvey J. Alter, Michael Houghton y Charles M. Rice recibieron el premio Nobel de Medicina de 2020 por el descubrimiento del virus de la Hepatitis C. Sus trabajos favorecieron el desarrollo de pruebas para detectar la hepatitis C y limitar la transmisión.
2020 – Nobel de Química para la edición del genoma
En 2020 el Nobel de Química fue para Emmanuelle Charpentier y Jennifer Doudna por el desarrollo de un método para modificar el genoma. Ambas investigadores tuvieron un papel importante en la tecnología CRISPR, que permite editar el genoma de forma más sencilla y versátil que los métodos anteriores.
2021 – Nobel de Medicina para los receptores de la temperatura y el tacto
David Julius y Ardem Patapoutian recibieron el Premio Nobel por sus descubrimientos de los receptores de temperatura y tacto. Su trabajo contribuyó a conocer cómo percibe nuestro organismo las señales físicas y la transmisión de estas señales para ser interpretadas por el cerebro.
2022 – Nobel de Medicina para la evolución humana
En 2022, el científico Svante Pääbo recibió el Premio Nobel de Fisiología y Medicina por sus descubrimientos sobre los genomas de homínidos extintos y la evolución humana.
2023 – Nobel de Medicina para Katalin Karikó y Drew Weissman
Katalin Karikó y Drew Weissman recibieron el Premio Nobel de Medicina de 2023 por sus descubrimientos sobre la interacción entre el ARN y el sistema inmunitario. Su trabajo fue clave para el desarrollo de las vacunas de ARN mensajero frente a COVID-19.
2024- Premio Nobel de Medicina para los descubridores de los microARNs
Victor Ambros y Gary Ruvkun fueron sido galardonados con el Premio Nobel de Fisiología o Medicina 2024 por su descubrimiento de los microARNs y su papel en la regulación de la expresión de los genes.
El trabajo de ambos investigadores reveló un nuevo nivel de regulación de la actividad de los genes, basado en microARNs. Este tipo de molécula pequeña de ARN actúa a nivel del ARN mensajero, inhibiendo su traducción en proteínas o promoviendo su degradación y tiene un papel esencial en el desarrollo y función de los organismos multicelulares. Además, su alteración está relacionada con la aparición de diferentes patologías en humanos.
2024 – Premio Nobel de Química para los avances en la resolución de la estructura de las proteínas
El Premio Nobel de Química de 2024 fue otorgado a David Baker, por el diseño computacional de proteínas, y a Demis Hassabis y John M. Jumper en reconocimiento a sus contribuciones pioneras en la predicción de estructuras proteicas mediante el uso de inteligencia artificial.
Ambos premios están relacionados con la predicción de estructuras a partir de la secuencia de aminoácidos (definida por la secuencia de ADN) y la predicción de secuencias a partir de estructuras. El trabajo de los investigadores galardonados ha permitido avances notables en la obtención de la estructura de miles de proteínas con alta precisión y generación de proteínas nuevas con estructuras deseadas, con aplicaciones en la biotecnología, la medicina y otros campos científicos.
Hasta aquí los últimos Premios Nobel de la Genética. Si queréis más detalles de cada uno podéis consultar las noticias específicas que os incluímos. Y si os apasiona el mundo de la Genética, recordad que siempre podéis ampliar vuestro conocimiento con Genotipia.
Bibliografía
2017 – Nobel de Medicina para el Reloj Circadiano. https://genotipia.com/genetica_medica_news/nobel-medicina-2017/
2018 – Nobel de Medicina para la Inmunoterapia. https://genotipia.com/genetica_medica_news/nobel-2018-inmunoterapia-cancer/
2018 – Nobel de Química para la evolución aplicada a la biotecnología y medicina. https://genotipia.com/genetica_medica_news/nobel-quimica-2018/
2019 – Nobel de Medicina para la respuesta celular a la disponibilidad de oxígeno. https://genotipia.com/genetica_medica_news/nobel-fisiologia-medicina-2019/
2020 – Nobel de Medicina para el virus de la hepatitis C. https://genotipia.com/genetica_medica_news/nobel-medicina-2020-hepatitis/
2020 – Nobel de Química para la edición del genoma. https://genotipia.com/genetica_medica_news/nobel-quimica-crispr/
2021 – Nobel de Medicina para los receptores de la temperatura y el tacto. https://genotipia.com/genetica_medica_news/premio-nobel-medicina-2021-receptores-de-la-temperatura-y-el-tacto/
2022- Nobel de Medicina para la evolución humana. https://genotipia.com/genetica_medica_news/nobel-de-medicina-2022-svante-paabo-evolucion-humana/
2023 – Nobel de Medicina para las vacunas de ARN mensajero. https://genotipia.com/genetica_medica_news/nobel-2023-vacunas-arn-mensajero/
2023 – Nobel de Medicina para las vacunas de ARN mensajero. https://genotipia.com/genetica_medica_news/nobel-2023-vacunas-arn-mensajero/
2024 – Premio Nobel de Medicina para los descubridores de los microARNs. https://genotipia.com/genetica_medica_news/nobel-medicina-2024-microarns/
NobelPrize https://www.nobelprize.org/



