INTRODUCCIÓN
El estudio de los ritmos circadianos comenzó con observaciones de los movimientos de las plantas y ahora abarca una amplia gama de organismos (desde las cianobacterias hasta los seres humanos), lo que pone de relieve el papel universal de los relojes biológicos. La regulación circadiana de procesos esenciales como la secreción de hormonas, el sueño, el metabolismo y la respuesta inmunitaria (Masri y Sassone-Corsi, 2018) es fundamental para la salud humana. Los ritmos circadianos se sincronizan mediante señales ambientales, como la luz y la ingesta de alimentos. En los mamíferos, el marcapasos circadiano central es el núcleo supraquiasmático, situado en el hipotálamo anterior. Recibe información luminosa de la retina (Moore y Lenn, 1972), transmite señales circadianas dentro del hipotálamo a través de la comunicación sináptica y paracrina y comunica la información circadiana a los tejidos periféricos de forma indirecta a través de hormonas, la temperatura corporal y los metabolitos.
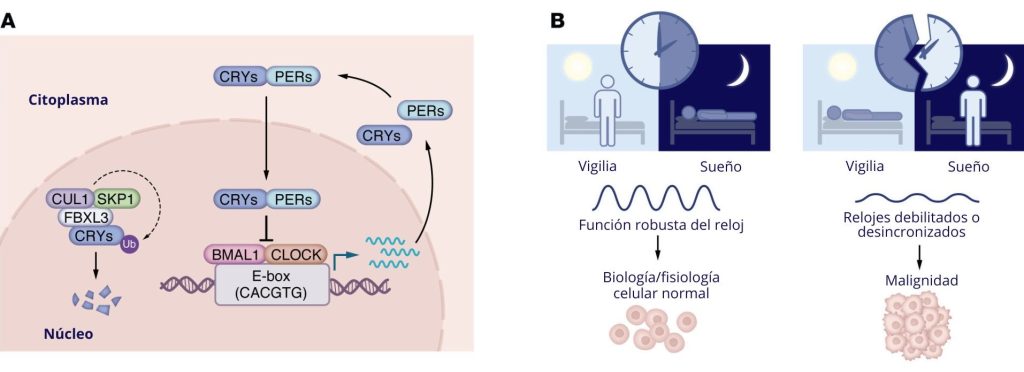
Los ritmos circadianos celulares implican un bucle de retroalimentación transcripción-traducción en el que el brazo positivo está impulsado por el heterodímero de la proteína básica hélice-bucle-hélice (bHLH-PAS) PER-ARNT-SIM (Fribourgh y Partch, 2012; Wu y Rasinejad, 2017) y los factores de transcripción BMAL1-CLOCK (Takahashi, 2017), que se unen a secuencias E-box (5´-CACGTG-3´) para iniciar la transcripción de genes controlados por el reloj, incluidos PER1/2/3 y CRY1/2, los cuales forman el brazo negativo del reloj circadiano reprimiendo a BMAL1-CLOCK (Kume et al., 1999). La degradación oportuna de CRY, mediada por una ubiquitina ligasa E3 Skp–Cullin–F-box (SCF) que contiene una proteína 3 con F-box y repeticiones ricas en leucina (que contiene FBXL3) (Busino et al., 2007), reinicia el ciclo (Figura 1A). Otros parálogos relacionados con BMAL1 (como BMAL2) y CLOCK (como NPAS2) contribuyen a los ritmos circadianos de forma selectiva según el tejido y son menos conocidos (DeBruyne et al., 2007; DeBruyne et al., 2007b; Dantas-Ferreira et al., 2024). Los receptores hormonales nucleares de las subfamilias 1D y 1F (también conocidos como REV-ERB y ROR) regulan la transcripción del gen que codifica BMAL1, lo que favorece los ritmos circadianos (Sato et al., 2004; Preitner et al., 2003; Yin y Lazar et al., 2005).
Los estudios epidemiológicos relacionan la alteración del ritmo circadiano con un mayor riesgo de cáncer (Bass y Lazar, 2016; Pariollaud y Lamia, 202) (Figura 1B), lo que ha llevado a la Agencia Internacional para la Investigación del Cáncer a clasificar el trabajo en turnos de noche como un probable carcinógeno humano (Erren et al., 2016). Estos estudios subrayan la relación entre la alteración del ritmo circadiano y el cáncer, pero ofrecen una visión limitada de los mecanismos implicados, lo que plantea la necesidad de seguir investigando para aclarar los procesos biológicos que contribuyen a este fenómeno. Términos como “jet lag crónico”, “desalineación circadiana” y “alteración del reloj biológico” se utilizan a menudo de forma intercambiable, aunque describen perturbaciones distintas: la desincronización inducida por el entorno, la desalineación entre las señales internas y externas, o la alteración molecular del reloj biológico, respectivamente. Esta heterogeneidad terminológica puede oscurecer el significado y complicar la interpretación entre los distintos estudios.
En esta revisión se analizan los últimos avances sobre la relación entre el reloj circadiano y el cáncer, centrándose en cómo este “marcapasos” biológico influye en la biología tumoral y en las respuestas terapéuticas en contextos específicos de cada tejido.
EFECTOS MULTIFACÉTICOS DE LA ALTERACIÓN DEL RITMO CIRCADIANO EN EL CRECIMIENTO TUMORAL
La desincronización circadiana ambiental (como la alteración de los ciclos de luz y oscuridad) agrava el crecimiento tumoral en modelos murinos, incluidos los tumores de xenoinjertos derivados de células de osteosarcoma o melanoma, el carcinoma hepatocelular espontáneo y los cánceres de colon, mama y pulmón modificados genéticamente (Filipski et al., 2004; Filipski et al., 2009; Kettner et al., 2016; Lee et al., 2010; Papagiannakopoulos et al., 2016; Pariollaud et al., 2022; Van Dyke et al., 2015; Chun et al., 2022; Stokes et al., 2021; Wang et al., 2023). Sin embargo, no afecta a la carga tumoral en un modelo de linfoma impulsado por la expresión transgénica de c-MYC (Mello et al., 2023). La mutación o deleción de componentes del reloj circadiano puede tener consecuencias oncogénicas o supresoras de tumores, dependiendo del tipo de perturbación utilizada, el tipo de cáncer y el modelo experimental. Dicha variabilidad puede deberse a funciones no canónicas y específicas de cada tejido de las proteínas del reloj, incluida la regulación mediada por CRY de los procesos metabólicos (Jordan et al., 2017; Kriebs et al., 2017; Zhang et al., 2010) y la integridad del genoma (Shafi et al., 2021; Papp et al., 2015; Chan et al., 2021) o la heterodimerización de BMAL1 con HIF2α (Mello et al., 2025; Ruan et al., 2025).
La deleción de BMAL1 en células de cáncer de páncreas humano aumenta el crecimiento de tumores de xenoinjertos en ratones (Kiang et al., 2016). Evidencias en células humanas y de ratón sugieren que esto puede implicar una apoptosis alterada y una progresión aumentada del ciclo celular (Kiang et al., 2016, Schwartz et al., 2023). En modelos de ratón modificados genéticamente con cáncer de colon, BMAL1 favorece la renovación epitelial y la regulación inmunitaria, mientras que su pérdida acelera la iniciación tumoral (Stokes et al., 2021), promueve el crecimiento tumoral (Chun et al., 2022) y altera el panorama inmunitario del tumor (Fortin et al., 2024). De manera similar, la pérdida de BMAL1 en el adenocarcinoma pulmonar murino da lugar a un aumento de c-MYC, una mayor proliferación y una desregulación metabólica (Papagiannakopoulos et al., 2016). Todos estos hallazgos sugieren un papel supresor de tumores para BMAL1 en el cáncer de páncreas, pulmón y colon.
La pérdida de el brazo positivo del reloj circadiano inhibe la tumorigénesis en otros tipos de tumores. En células de glioblastoma (GBM) derivadas de muestras clínicas, la deleción de BMAL1 o CLOCK induce la detención del ciclo celular y la apoptosis (Dong et al., 2019). Del mismo modo, la depleción de Bmal1 o Clock promueve la diferenciación de las células madre y dificulta el crecimiento tumoral en la leucemia mieloide aguda en ratones (Puram et al., 2016). La pérdida de BMAL1 también reduce el crecimiento de células humanas de carcinoma renal de células claras (carcinoma renal de células claras) y de tumores de xenoinjertos cultivados en ratones. En las células de carcinoma renal de células claras, BMAL1 promueve el crecimiento a través de la formación de dímeros con HIF2α, potenciando así la señalización oncogénica (Mello et al., 2025). La sobreexpresión de BMAL1 aumentó la migración de líneas celulares de cáncer de mama humano a través de la sobreregulación MMP9 (Wang et al., 2019), pero no se ha investigado el papel de BMAL1 en un modelo in vivo de cáncer de mama. Se ha descrito que la inhibición de BMAL1 reduce la migración, la invasión y la quimiorresistencia en células de cáncer colorrectal y muestras clínicas (Zhang et al., 2021), en contraste con los estudios que demuestran una mayor tumorigénesis tras la deleción de Bmal1 en modelos murinos de cáncer de colon con deficiencia de Apc (Chun et al., 2022; Stokes et al., 2021; Fortin et al., 2024). Hacen falta más investigaciones para determinar si la dosis de APC u otros factores influyen en el impacto de BMAL1 sobre el crecimiento de las células de cáncer colorrectal. La expresión de BMAL1 es menor en el adenocarcinoma de colon humano que en el colon normal, y es mayor en muestras de carcinoma renal de células claras que en el riñón normal (Mello et al., 2025). Todos estos datos sugieren que BMAL1 y CLOCK pueden actuar como impulsores de la malignidad específicos del contexto.
Aunque los mecanismos que subyacen a esta dualidad aún no se comprenden del todo, es probable que impliquen tanto una apropiación maligna de los procesos fisiológicos regulados por el reloj circadiano como interacciones directas entre los componentes del reloj circadiano y los efectores del cáncer. Es importante destacar que los efectos de la alteración circadiana pueden verse condicionados por la genética del huésped, de modo que un mismo factor del reloj podría desempeñar funciones opuestas en diferentes contextos. Revisiones recientes advierten contra afirmaciones universales sobre los genes circadianos en el cáncer, haciendo hincapié en los efectos específicos del locus, el tejido y el modelo (Sancar y Van Gelder, 2021).
REGULACIÓN CIRCADIANA DE LAS RUTAS CRÍTICAS PARA LA PROGRESIÓN TUMORAL
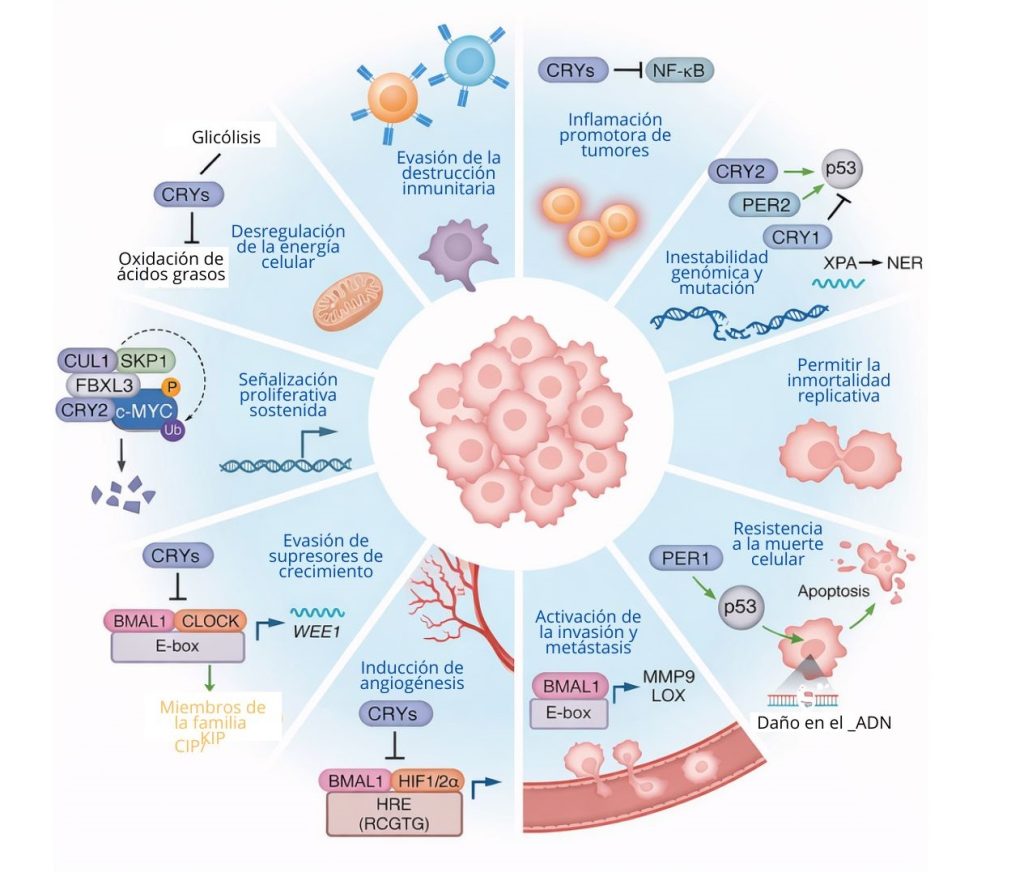
Los relojes circadianos coordinan los procesos celulares esenciales para responder a las fluctuaciones ambientales, incluidas las vías consideradas como características distintivas del cáncer (Swanton et al., 2024) (Figura 2), lo que pone de relieve cómo la alteración del ritmo circadiano puede contribuir a la malignidad o cómo las células transformadas pueden apropiarse de los relojes circadianos para impulsar el crecimiento maligno. En esta sección se analizan cuatro vías reguladas por el ritmo circadiano relevantes para el cáncer: la progresión del ciclo celular, la respuesta y reparación del daño en el ADN, la señalización de la hipoxia y la metástasis (Tabla 1).
| Vía | Gen/Proteína | Función | Mecanismo |
| Ciclo celular | p21, p27, p57 | Inhibidores de quinasas dependientes de ciclina | Expresión rítmica en múltiples tejidos (Gréchez-Cassiau et al. 2008; Soták et al., 2014) |
| WEE1 | Punto de control G₂/M | Expresión rítmica en múltiples tejidos (Matsuo et al., 2003; Gery et al., 2006; Zhang et al., 2014; Mure et al., 2018) | |
| c-MYC | Promueve la proliferación | Competencia por E-box (Shostak et al., 2016) Ubiquitinación mediada por CRY2 (Huber et al., 2016) | |
| Daño en el ADN | XPA | NER (enzima limitante de la velocidad) | La expresión está regulada por el reloj molecular (Kang et al., 2010; Gaddameedhi et al., 2011; Kang et al., 2011) |
| Guardián de la integridad genómica | Estabilizado por PER2 (Gotoh et al., 2014) PER1 favorece la localización nuclear (Gery et al., 2006) Mutantes de CRY2 inhiben la actividad (Chan et al., 2021) | ||
| Hipoxia | HIF1α, HIF2α | Factores de transcripción sensibles a hipoxia | Expresión rítmica (Wu et al., 2017) Heterodimerizan con BMAL1 (Mello et al., 2025; Ruan et al., 2025; Wu et al., 2017; Peek et al., 2017) Suprimidos por CRYs (Vaughan et al., 2020; Dimova et al., 2019) |
Ciclo celular
Los primeros estudios en ratones revelaron que el momento de la división celular en el hígado tras una hepatectomía parcial está regulado por el ritmo circadiano (Matsuo et al., 2003). Investigaciones posteriores exhaustivas han mostrado que, incluso en células individuales, los osciladores circadianos y del ciclo celular están acoplados; los detalles de este acoplamiento no se conocen bien y varían según el tipo de célula (Nagoshi et al., 2004; Droin et al., 2019; Bieler et al., 2014). Los reguladores clave del ciclo celular —incluidas las ciclinas (Zhou et al., 2014) y los miembros de la familia Cip/Kip de inhibidores de la quinasa dependiente de ciclina (p21, p27 y p57) (Gréchez-Cassiau et al., 2008; Soták et al., 2014)— muestran una expresión circadiana en múltiples tejidos.
Los repositorios públicos como The Cancer Genome Atlas (Cancer Genome Atlas Research Network, et al., 2013) son un recurso valioso para la biología del cáncer. De forma similar, herramientas como CircaDB (Pizarro et al., 2013) permiten a los investigadores visualizar los patrones de expresión circadiana de cualquier gen de interés en múltiples estudios. Estas herramientas proporcionan información valiosa, limitada únicamente por la calidad de los estudios subyacentes, que pueden no tener en cuenta las diferencias de sexo, las etapas de desarrollo o la variación entre especies, factores que pueden estar detrás de vínculos sin resolver entre los ritmos circadianos y el cáncer. Independientemente de los mecanismos subyacentes, la alteración de la influencia circadiana sobre la progresión del ciclo celular puede facilitar una proliferación descontrolada.
Uno de los primeros vínculos descritos entre el reloj circadiano y el ciclo celular es WEE1, una quinasa que controla la transición G2/M impidiendo la entrada prematura en la mitosis. En ratones sanos, BMAL1-CLOCK activa transcripcionalmente a Wee1, y la expresión de Wee1 aumenta en modelos con carencia de CRY (Matsuo et al., 2003). La expresión ectópica de PER1 suprime la de WEE1 independientemente de p53 en líneas celulares de cáncer de colon humano (Gery et al., 2006), lo que sugiere además una regulación opuesta por parte de las ramas positiva y negativa del reloj circadiano. De manera coherente, el transcrito que codifica WEE1 muestra ritmos circadianos robustos en muchos órganos de roedores y primates sanos (Parioullad et al., 2022; Koike et al., 2012; Zhang et al., 2014; Mure et al., 2018), en consonancia con la dinámica de genes controlados por el reloj. Notablemente, la expresión rítmica circadiana de Wee1 en los pulmones de ratón se ve alterada por la exposición a un jet lag crónico (Parioullad et al., 2022). La proteína WEE1 se potencia de forma transitoria durante varios días tras una hepatectomía parcial y muestra fluctuaciones diarias contrarias a las observadas para la proteína BMAL1 (Zou et al., 2012). Sin embargo, existe desacuerdo en la literatura sobre si la fosforilación de CDC2, diana de WEE1, presenta ritmos diarios correlacionados con los de la acumulación de la proteína WEE1 (Matsuo et al., 2003; Zou et al., 2012), y no está claro si la regulación circadiana de WEE1 es funcionalmente importante para vincular las oscilaciones circadianas y del ciclo celular. Aunque WEE1 se expresa en niveles elevados en muchos casos clínicos de cáncer, se ha descrito su ausencia en los cánceres de colon y de pulmón no microcítico (Matheson et al., 2016), lo que podría contribuir a los efectos específicos del contexto de la alteración circadiana sobre la progresión del cáncer.
Otro regulador clave del ciclo celular es c-MYC, que impulsa la proliferación en muchos tumores (Walton et al., 2018). c-MYC y el reloj circadiano muestran una regulación recíproca (Figura 3, A–C). Al igual que BMAL1-CLOCK, c-MYC se une a los motivos E-box, incluidos los que regulan NR1D1 (también conocido como Reverba), un represor de BMAL1 (Altman Brian et al., 2015). Por lo tanto, c-MYC puede interferir en la transcripción circadiana mediante una unión competitiva o una represión indirecta a través de la activación de NR1D1. De hecho, la sobreexpresión de c-MYC atenúa la oscilación circadiana de la expresión génica y de procesos fisiológicos celulares como la captación de glucosa, mediante una regulación positiva combinada de NR1D1 —que reprime la transcripción de BMAL1 (Altman Brian et al., 2015)— y una represión directa de BMAL1 a través de los complejos MYC-MIZ1 (Shostak et al., 2016). Aunque los primeros informes discrepaban sobre si NR1D1 media la alteración circadiana inducida por MYC, MYC aumenta de forma consistente la proteína NR1D1 (Shostak et al., 2016; Altman et al., 2017). En modelos murinos de cáncer colorrectal, la alteración circadiana activa la señalización mediada por Wnt, una vía clave que promueve la expresión de Myc en los intestinos (Chun et al., 2022), lo que podría ayudar a explicar los efectos específicos de cada tejido de la alteración circadiana sobre el crecimiento tumoral. La reducción de la coordinación de la expresión génica circadiana es una característica común de muchos cánceres (Shilts et al., 2018). Sin embargo, algunos tumores conservan ritmos circadianos robustos (Mello et al., 2025). Se desconoce qué determina el grado en que los ritmos circadianos se degradan en los tumores, pero la amplificación de MYC podría promover la desregulación circadiana. Se requieren más investigaciones para comprender por qué los tumores presentan una alteración variable de los ritmos circadianos y si esto tiene alguna implicación para la progresión de la enfermedad o el manejo clínico.
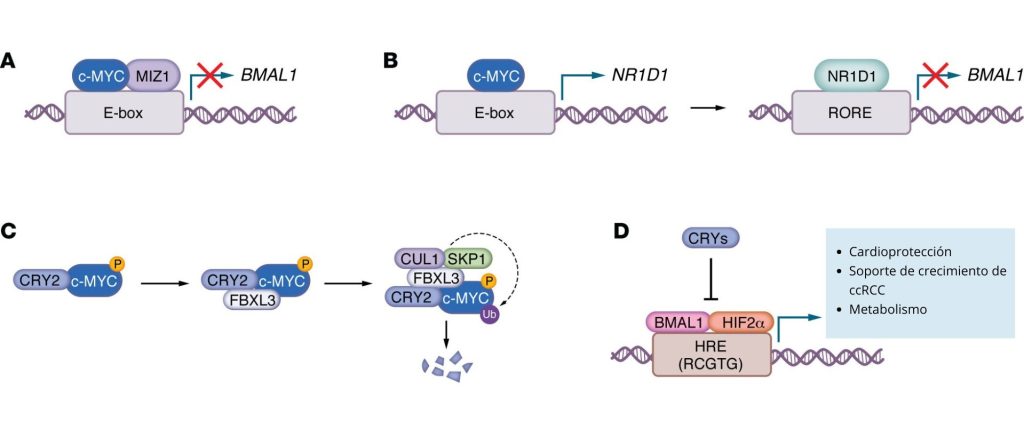
c-MYC suele tener una vida media corta. Su degradación está regulada por múltiples vías (Das et al., 2023), incluida una en la que interviene el represor circadiano CRY2. CRY2 recluta el c-MYC fosforilado al complejo SCF-FBXL3, lo que facilita su renovación en el linfoma impulsado por MYC (Huber et al., 2016). CRY2 salvaje o wildtype inhibe el crecimiento impulsado por MYC en fibroblastos embrionarios de ratón, mientras que los mutantes de CRY2 identificados en biopsias tumorales de pacientes que no interactúan con FBXL3 son notablemente menos eficaces (Chan et al., 2021). In vivo, cuando un transgén de MYC humano se expresa fuertemente en células linfoides de ratón, la deleción ubicua de Cry2 conduce a un aumento de MYC en bazo pretumoral y a un linfoma más agresivo (Huber et al., 2016). Por el contrario, MYC no se ve afectado en bazo sano en ratones que carecen de Cry1 o Cry2 en ausencia de sobreexpresión de MYC, y el MYC endógeno se reduce en bazo de ratones Cry1−/− Cry2−/− (Liu et al., 2020). Se requieren más estudios para comprender estos hallazgos algo contradictorios. La interacción de FBXL3 con el mecanismo de ubiquitinación se ve potenciada por el daño en el ADN (Reitsma et al., 2017), por lo que el recambio de MYC estimulado por FBXL3 y CRY2 podría ser relevante únicamente en células sometidas a estrés de replicación inducido por MYC u otras fuentes de daño en el ADN.
Por lo tanto, la abundancia de MYC podría influir en el grado en que está sujeta a la renovación dependiente de CRY2. Esta función no canónica de CRY2 en la regulación de la renovación de MYC —y la identificación de mutaciones clínicamente relevantes que alteran esta función— pone de manifiesto un vínculo mecánico entre la alteración del ritmo circadiano y la proliferación celular descontrolada, lo que refuerza el papel central del reloj circadiano en la fisiología del cáncer. En consonancia con esto, CRY2 se expresa a niveles más bajos en muchos casos clínicos de cáncer en comparación con el tejido normal emparejado (Huber et al., 2016), aunque sigue sin estar claro si la reducción de CRY2 contribuye a la malignidad o es consecuencia de un proceso tumorigénico desconocido. Se necesitan más investigaciones para estudiar si, y en caso afirmativo cómo, CRY2 influye en la formación de tumores en diversos contextos (Sancar et al., 2021).
Respuesta y reparación del daño en el ADN
Cada vez hay más pruebas que relacionan el reloj molecular con la respuesta y la reparación del daño en el ADN. La reparación por escisión de nucleótidos (NER) muestra un carácter rítmico (Kang et al., 2009; Kang et al., 2010; Gaddameedhi et al., 2011), impulsado por el control circadiano de XPA, el factor limitante de la velocidad en la NER Kang et al., 2009; Kang et al., 2010; Gaddameedhi et al., 2011; Kang et al., 2011). Aunque los criptocromos (CRY) de los mamíferos han perdido su actividad fotoliasa ancestral, la proteína CRY2 de los mamíferos interactúa preferentemente con fotoproductos (Özgür y Sancar, 2003), lo que podría respaldar funciones no canónicas en el reconocimiento o la reparación del daño en el ADN. De hecho, las células con deficiencia de CRY2 acumulan daño en el ADN (Papp et al., 2015) . Además, CLOCK se localiza en los sitios de daño en el ADN inducidos por la radiación ionizante, lo que sugiere que múltiples proteínas del reloj circadiano pueden contribuir a la respuesta al daño en el ADN. Por otra parte, el daño en el ADN estabiliza CRY1, desestabiliza CRY2 y puede reiniciar los relojes circadianos (Shafi et al., 2021; Papp et al., 2015). P53 —un mediador crítico de la respuesta al daño en el ADN— se une al promotor de Per2, induciendo su expresión y suprimiendo la actividad transcripcional de BMAL1-CLOCK (Miki et al., 2013). Además, FBXL3 muestra una mayor asociación con CUL1 tras el tratamiento con etopósido (Reitsma et al., 2017), y CRY2 muestra una mayor afinidad por FBXL3 en respuesta a la doxorrubicina (Papp et al., 2015), lo que apunta a un mecanismo de desestabilización de CRY2 por estrés genotóxico. Globalmente, estos resultados revelan una relación bidireccional entre la sincronización circadiana y la integridad genómica: la disfunción circadiana puede afectar a la eficacia de la reparación del ADN y aumentar el riesgo de cáncer, y el daño en el ADN puede alterar los ritmos circadianos en los tumores.
El daño en el ADN desencadena la apoptosis a través de p53, lo que impide la transmisión de material genético dañado. Como supresor tumoral clave, p53 protege la estabilidad genómica al detener la progresión del ciclo celular en presencia de lesiones en el ADN. PER2 estabiliza p53 al impedir su degradación mediada por ubiquitina (Gotoh et al., 2013; Gotoh et al., 2015), mientras que la sobreexpresión de PER1 potencia la localización nuclear de p53 y sensibiliza a las células cancerosas a la apoptosis inducida por el daño en el ADN (Gery et al., 2006). Curiosamente, las versiones mutantes de CRY2 identificadas en biopsias tumorales inhiben la actividad de p53 y, en células con p53 intacto, promueven una proliferación descontrolada (Chan et al., 2021). Estos hallazgos sugieren que la rama negativa del reloj circadiano promueve la estabilidad genómica, en parte mediante el apoyo a la función de p53, y que la alteración de estos componentes puede socavar este eje supresor de tumores. La activación de p53 por la luz UV presenta ritmos circadianos, lo cual depende de BMAL1 (Kawamura et al., 2018). En un modelo murino de adenocarcinoma de pulmón impulsado por KRAS, la alteración circadiana por exposición al jet lag crónico aumenta la carga tumoral (Pariollaud et al., 2022) de forma más marcada cuando P53 está intacto que cuando P53 está delecionado (Papagiannakopoulos et al., 2016; Pariollaud et al., 2022). Esto puede reflejar la naturaleza agresiva de los tumores con deficiencia de P53, que enmascara el efecto del jet lag crónico, o puede indicar que el impacto del jet lag crónico en la tumorigénesis implica la interferencia con una o más funciones supresoras de tumores de P53 (Papagiannakopoulos et al., 2016).
Cuando se induce carcinoma hepatocelular murino mediante radiación ionizante o se forma de forma espontánea, la deleción genética tanto de Cry1 como de Cry2 potencia la tumorigénesis (Kettner et al., 2016; Lee et al., 2010) y hace que los ratones sean más susceptibles a una mayor formación de tumores en respuesta al CJL (Kettner et al., 2016; Padilla et al., 2024) . Sin embargo, la deleción de Cry1 y Cry2 reduce la formación de tumores en ratones p53−/− al resensibilizar a las células a la apoptosis inducida por el daño en el ADN (Ozurk et al., 2009), lo que sugiere que la interacción entre P53 y los CRY podría influir en los efectos divergentes de los relojes circadianos sobre el crecimiento tumoral. En conjunto, estos estudios ponen de manifiesto la complejidad de la regulación circadiana en la respuesta al daño en el ADN y subrayan la importancia de tener en cuenta el trasfondo genético a la hora de evaluar el papel del reloj circadiano en la regulación de la estabilidad genómica.
Hipoxia
La hipoxia se produce en los tumores sólidos como consecuencia de la rápida proliferación celular y la consiguiente competencia por el oxígeno y otros nutrientes. A medida que los tumores crecen más allá de la capacidad de la vasculatura existente, desarrollan regiones con baja disponibilidad de oxígeno (denominadas zonas hipóxicas) dentro del microambiente tumoral. El estrés hipóxico desencadena una respuesta celular mediada principalmente por los HIF (Factores Inducibles por Hipoxia). Cuando el oxígeno es abundante, las enzimas con dominio prolil hidroxilasa hidroxilan las prolinas en HIF1α y HIF2α (también conocido como EPAS1), lo que promueve el reconocimiento de HIF1/2α por el supresor tumoral von Hippel–Lindau (VHL), facilitando la ubiquitinación y la degradación proteasómica de las subunidades HIFα (Ivan y Kaelin, 2017). En condiciones hipóxicas —o con la inactivación de VHL, frecuente en el carcinoma renal de células claras (Shen et al., 2013)—, esta vía se ve alterada, lo que conduce a la estabilización de HIF1α y HIF2α. Las subunidades HIFα estabilizadas entran en el núcleo, donde se dimerizan con ARNT (también conocido como HIF1β) y se unen a los elementos de respuesta a la hipoxia (HRE) en los promotores de los genes diana. Estos genes regulan procesos biológicos que favorecen la adaptación y la supervivencia del tumor, entre ellos la angiogénesis (por ejemplo, VEGFA), el metabolismo de la glucosa (como GLUT1 y LDHA) y la invasión (como MMP9, LOX) (Ivan y Kaelin, 2017; Majmundar et al., 2010; Gordan y Simon et al., 2007; Kaelin 2017).
Los HIF son factores de transcripción bHLH-PAS y comparten una estrecha relación evolutiva y estructural con BMAL1 y CLOCK (Fribourgh y Partch, 2012; Wu y Rasinejad, 2017). Cabe destacar que ARNT y BMAL1 presentan una alta conservación en sus dominios bHLH de unión al ADN y en los motivos de heterodimerización PAS en tándem (Mello et al., 2025; Maurer et al., 2025). Los primeros informes indicaban que BMAL1 podía formar heterodímeros transcripcionalmente activos con subunidades HIFα (Hogenesch et al., 1998), aunque inicialmente se creía que BMAL1 no era fundamental para la respuesta hipóxica. Esta opinión se basaba en gran medida en estudios que mostraban que BMAL1 no era esencial para la angiogénesis embrionaria (Cowden y Simon, 2002), un proceso impulsado por el complejo HIF-1 (ARNT-HIF1α). Esta visión tradicional ha cambiado a la luz de la evidencia acumulada que revela la interacción entre las rutas circadianas y las de la hipoxia (Figura 3D).
Los estudios iniciales sobre el eje circadiano-hipoxia revelaron que, en ratones, la respuesta transcripcional a los estímulos hipóxicos en el hígado, riñones, músculos esqueléticos y pulmones está muy influida por la hora del día en que se aplica el estímulo (Wu et al., 2017; Dandavate et al., 2024; Manella et al., 2020; Peek et al., 2017) . El efecto de la exposición a la hipoxia a gran altitud sobre el transcriptoma sanguíneo humano también depende de la hora del día, lo que sugiere que este fenómeno se conserva en todas las especies (Manella et al., 2022). Los fibroblastos y los músculos esqueléticos murinos con deficiencia de PER y CRY muestran una mayor inducción de la expresión génica dirigida a la hipoxia en comparación con los controles wildtype tras la exposición a estímulos activadores de HIF (Wu et al., 2017; Vaughan et al., 2020), incluidos los genes proapoptóticos Bnip3 y Noxa1, lo que sugiere un papel protector de los represores del reloj circadiano durante la apoptosis inducida por la hipoxia (Wu et al., 2017). Estos resultados indican que la regulación circadiana de la expresión génica hipóxica depende de la hora del día, es específica de cada tejido y es influida por el reloj molecular.
La expresión circadiana de Hif1a (Wu et al., 2017; Panda et al., 2002) y Hif2a (Hughes et al., 2009) podría contribuir a la regulación circadiana de la respuesta transcripcional a la hipoxia. Sin embargo, la homología secuencial y estructural entre los factores de transcripción circadianos y los de la hipoxia condujo al descubrimiento de que BMAL1 se dimeriza con las subunidades HIFα. Los heterodímeros BMAL1-HIFα permiten la activación transcripcional de genes que contienen elementos de respuesta a hipoxia (Mello et al., 2025; Vaughan et al., 2020), motivos que se asemejan mucho a las secuencias E-box a las que se une BMAL1-CLOCK (Figura 3D). BMAL1 colocaliza con HIF1α (Wu et al., 2017) y HIF2α (Mello et al., 2025) en las células en varios sitios de la cromatina endógena, lo que indica una amplia interacción entre las redes transcripcionales que responden a los ritmos circadianos y a la hipoxia. Es detacable que BMAL1 contribuye a la expresión génica impulsada por HIF en contextos de enfermedad, incluyendo la obesidad inducida por la dieta (Chaikin et al., 2025) y el cáncer de riñón (Mello et al., 2025). Más recientemente, el heterodímero BMAL1-HIF2α se ha relacionado con la cardioprotección durante el infarto de miocardio (Ruan et al., 2025) y con la promoción del crecimiento del carcinoma renal de células claras (Mello et al., 2025). Al parecer, BMAL2 contribuye a la expresión génica inducida por la hipoxia y a la reprogramación metabólica en el cáncer de páncreas, posiblemente a través de interacciones con HIF1α (Maurer et al., 2025), lo que destaca más la convergencia de estas vías reguladoras en los procesos fisiopatológicos. Interesantemente, la expresión de BMAL2 es mayor en los tumores en comparación con las muestras normales adyacentes en muchos tipos de tumores (Liu et al., 2025). No está claro si BMAL2 contribuye a la tumorigénesis ni de qué manera lo hace.
Los represores del reloj circadiano pueden inhibir la transcripción mediada por HIF. Los criptocromos inhiben los genes diana de HIF1α (Vaughan et al., 2020; Dimova et al., 2019) y reprimen la transactivación de los heterodímeros BMAL1-HIF1α (Vaughan et al., 2020). La pérdida de los CRYs potencia la oxidación de ácidos grasos (Jordan et al., 2017) y la glucólisis (Vaughan et al., 2020) en los miotubos de ratón, probablemente debido al aumento de la actividad de los receptores hormonales nucleares y de HIF, respectivamente. Los fibroblastos embrionarios de ratón con deficiencia de CRY1 mostraron una mayor proliferación y migración en un estudio que atribuyó estos efectos al aumento de la actividad de HIF-1 (100). Sin embargo, existe desacuerdo en la literatura sobre el impacto de la depleción de CRY1 en la proliferación de los fibroblastos (Huber et al., 2016), y otros estudios han encontrado que CRY1 promueve el crecimiento en las células de cáncer de próstata (Shafi et al., 2021). En cualquier caso, la evidencia acumulada respalda la idea de que las proteínas CRY limitan la transcripción impulsada por HIF, incluidas las vías promotoras de tumores. Estos hallazgos sugieren que las CRY podrían desempeñar un papel protector en los tumores impulsados por la hipoxia, limitando potencialmente la progresión tumoral en condiciones de bajo nivel de oxígeno u otras condiciones de estabilización de HIF.
Los HIFs desempeñan un papel fundamental en la fisiología normal, especialmente en el riñón y el cerebro, órganos que están muy sensibles a las fluctuaciones de oxígeno. En tumores como el carcinoma renal de células claras y el glioma multiforme (GBM), los HIF no solo actúan como factores de respuesta al estrés, sino como impulsores fundamentales de la identidad tumoral, la progresión y la resistencia terapéutica. Estas neoplasias malignas dependen de manera específica de mecanismos genéticos (Shen et al., 2013; Kaelin et al., 2017; Wang et al., 2015; Ricketts et al., 2018; Linehan y Ricketts, 2019) y/o impulsados por señales oncogénicas (Wang et al., 2021) que estabilizan los HIF. Interesantemente, tanto el carcinoma renal de células claras como el glioma multiforme muestran una dependencia preferencial por HIF2α (Wang et al., 2021; Courtney et al., 2020; Kondo et al., 2002) frente al HIF1α, lo que los distingue de otros tipos de tumores en los que los HIF están inactivos, se estabilizan únicamente por la hipoxia del microambiente o dependen en mayor medida de la actividad del HIF1α. Esto podría ayudar a explicar por qué tumores como el carcinoma renal de células claras (Mello et al., 2025) y el GBM (Dong et al., 2019) presentan un crecimiento alterado tras la pérdida de BMAL1, mientras que otros cánceres no (Papagiannakopooulos et al., 2016; Chun et al., 2022). Esta hipótesis merece una investigación más profunda para dilucidar la interacción mecánica entre el reloj molecular y la tumorigénesis, y podría revelar nuevas oportunidades terapéuticas que aprovechen el eje circadiano-hipoxia en contextos oncológicos específicos.
Por el contrario, la estabilización de HIFα puede modular los ritmos circadianos. En los roedores, los niveles fisiológicos de oxígeno oscilan a lo largo del día; fluctuaciones similares pueden reajustar los relojes circadianos en células cultivadas de forma dependiente de HIF1α (Adamovich et al., 2017). Esto sugiere que la activación de HIF1α impulsada por el oxígeno puede actuar como un Zeitgeber —una señal temporal ambiental— para el sistema circadiano en algunos mamíferos. Sin embargo, la estabilización crónica de HIF1α altera los ritmos circadianos en múltiples modelos, incluyendo el músculo esquelético murino (Peek et al., 2017), las células de osteosarcoma humano U2OS (Wu et al., 2017) y los fibroblastos embrionarios de ratón NIH3T3 (Dimova et al., 2019) . Por el contrario, las células de carcinoma renal de células claras, en las que HIF2α se estabiliza debido a la inactivación de VHL, muestran ritmos circadianos robustos que se atenúan tras la reintroducción de VHL wildtype (Mello et al., 2025). Esta observación sugiere que, a diferencia de HIF1α, HIF2α puede promover, en lugar de alterar, la ritmicidad circadiana. En apoyo de esto, una variante natural de HIF2α de la meseta, adaptada a la altitud, atenúa los ritmos circadianos, mientras que en roedores que no habitan de forma nativa en entornos de gran altitud, HIF2α no muestra este efecto supresor (Liu et al., 2022). Estos hallazgos plantean la posibilidad de que HIF2α pueda favorecer las oscilaciones circadianas, en contraste con la influencia disruptiva de la actividad sostenida de HIF1α. Por lo tanto, HIF1α y HIF2α podrían ejercer efectos distintos, y potencialmente opuestos, sobre la regulación del ritmo circadiano. Por otra parte, las diferencias en el modo de estabilización de HIF —ya sea inducida por fármacos, la inactivación de VHL, el ejercicio o la hipoxia— pueden afectar de manera diferente a la función del reloj circadiano. Se necesitan más estudios mecánicos para aclarar cómo las isoformas específicas de los HIF y los contextos de estabilización modulan los ritmos circadianos y cómo estos efectos se relacionan con la progresión tumoral y las respuestas al tratamiento.
Metástasis
Varios hallazgos recientes sugieren que el momento en que se produce la metástasis podría estar regulado por los ritmos diarios. En modelos de cáncer de mama en humanos y ratones, la liberación espontánea de células tumorales circulantes alcanzó su punto máximo durante la fase de reposo del ciclo circadiano (es decir, el sueño), y las células tumorales liberadas durante esta fase mostraron una mayor expresión de genes mitóticos, lo que sugiere que no solo circulan más células tumorales durante el sueño, sino que las células liberadas también tienen una mayor capacidad metastásica (Diamantopoulou et al., 2022). En los tumores de mama luminal A, los ritmos circadianos marcados se correlacionaron con un aumento del ciclo génico epitelial-mesenquimal, un mayor potencial metastásico y una peor supervivencia de las pacientes (Li et al., 2024).
Si bien estos estudios señalan a ritmos interesantes para el comportamiento metastásico, todavía queda por distinguir las funciones específicas del sueño frente a la fase circadiana subyacente. El sueño en sí mismo podría contribuir mecánicamente a través de fluctuaciones hormonales, supresión inmunitaria o una permeabilidad vascular alterada durante el descanso. Por el contrario, la regulación circadiana independiente del sueño podría regular los programas transcripcionales que preparan a las células para la intravasación o la propagación. Desentrañar estos factores requerirá diseños controlados que analicen por separado el sueño y la fase del reloj endógeno, como el muestreo repetido basado en marcadores circadianos (como el inicio de la melatonina) y la monitorización simultánea del sueño y la vigilia.
CRONOTERAPIA
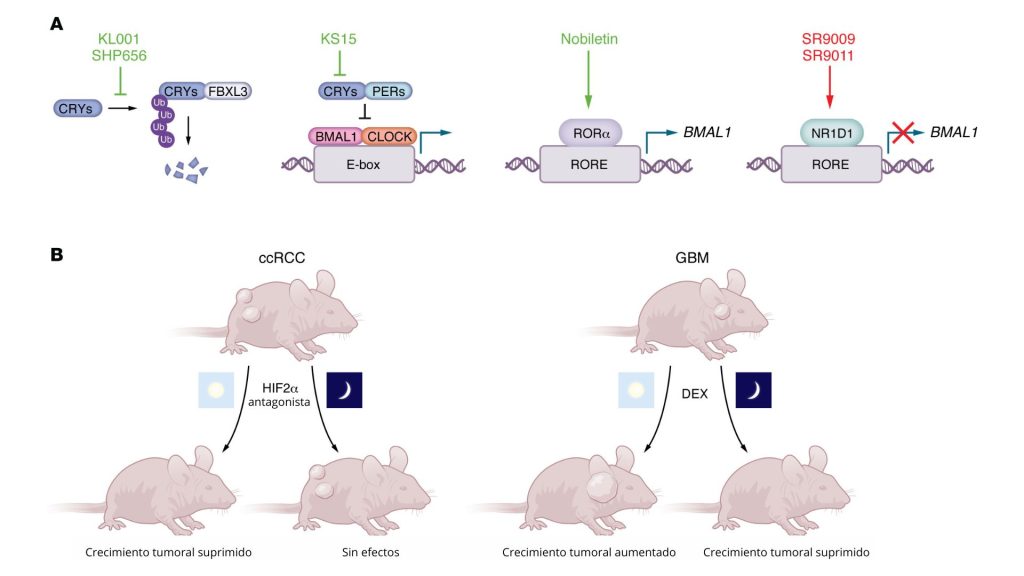
La cronoterapia aprovecha los ritmos circadianos para optimizar la eficacia terapéutica y minimizar los efectos adversos. Esta estrategia reconoce que el momento de la administración de los fármacos —en relación con la fase circadiana de cada persona— puede influir significativamente en los resultados del tratamiento. La cronoterapia puede dividirse, a grandes rasgos, en tres estrategias interrelacionadas: (a) el entrenamiento de los relojes biológicos, que consiste en reforzar los ritmos circadianos endógenos mediante intervenciones en el estilo de vida, como la regulación del sueño, la dieta y la actividad física; (b) la medicación de los relojes, que se centra en el uso de moléculas pequeñas para actuar sobre componentes del reloj molecular; y (c) la sincronización de la medicación, que determina el momento óptimo del día para la administración del fármaco con el fin de maximizar la eficacia y reducir la toxicidad (Lee et al., 2021). En este artículo nos centramos en las dos últimas estrategias: la medicación de los relojes y la medicina sincronizada (Figura 4).
Modulación farmacológica de los relojes biológicos: moléculas pequeñas dirigidas a componentes del reloj circadiano
El tratamiento del cáncer se enfrenta a retos persistentes, entre los que se incluyen la heterogeneidad tumoral, la inestabilidad genómica y la aparición de resistencias. Utilizar como diana el reloj circadiano ofrece una estrategia novedosa para superar algunos de estos obstáculos, aprovechando las vulnerabilidades específicas de los tumores en la regulación temporal de las proteínas del reloj molecular y los genes controlados por el reloj. Aunque los trabajos en este ámbito abarcan múltiples tipos de tumores, el GBM se ha convertido en un modelo clave, con aplicaciones prometedoras en otras neoplasias malignas, incluido el carcinoma renal de células claras.
El GBM es en gran medida resistente a las terapias convencionales. BMAL1 y CLOCK impulsan la progresión del ciclo celular, inhiben la apoptosis y mantienen la homeostasis metabólica en las células madre del GBM derivadas de muestras clínicas (Dong et al., 2019). Por lo tanto, actuar sobre estos factores podría constituir una estrategia terapéutica viable. Los agonistas de REV-ERBα SR9009 y SR9011 reducen la expresión de BMAL1 e inhiben la proliferación de las células madre del GBM (Dong et al., 2019) y el crecimiento de xenoinjertos de GBM in vivo (Sulli et al., 2018). SR9009 también reduce la expresión de BMAL1 e induce la autofagia en líneas celulares de cáncer de pulmón de células pequeñas, pero no en células epiteliales bronquiales humanas normales (Shen et al., 2020). Sin embargo, el tratamiento con SR9009 redujo la viabilidad y alteró la expresión génica en hepatocitos y células madre embrionarias, independientemente de la presencia o ausencia de REV-ERBα y REV-ERBβ, lo que sugiere que estas respuestas a SR9009 podrían no estar mediadas por los REV-ERB (Dierickx et al., 2019).
Otra estrategia prometedora consiste en estabilizar las proteínas CRY bloqueando su interacción con FBXL3, lo que impide su degradación proteasómica (Hirota et al., 2012; Lee et al., 2015; Oshima et al., 2015). Los compuestos estabilizadores de CRY KL001 y SHP656 tienen efectos antiproliferativos en las células madre del glioma en cultivos celulares (Dong et al., 2019). SHP656 también potencia la eficacia del bevacizumab, un anticuerpo anti-VEGFA, en xenoinjertos de cáncer colorrectal (Lo et al., 2024), y mejora la respuesta a la inmunoterapia anti-PD-1 al tiempo que ralentiza de forma independiente el crecimiento tumoral en modelos preclínicos (Soni et al., 2023). Los compuestos estabilizadores de CRY se han considerado seguros en ensayos clínicos de fase I, lo que resalta su potencial clínico (Chan et al., 2025). El inhibidor de CRY KS15, que interrumpe las interacciones CRY-BMAL1 (Jang et al., 2018), suprime el crecimiento y potencia la quimiosensibilidad en líneas celulares de cáncer de mama (Chun et al., 2014), lo que demuestra que tanto la inhibición como la estabilización de CRY pueden ser eficaces dependiendo del contexto tumoral.
La nobiletina (NOB), un compuesto natural derivado de Citrus reticulata y Citrus aurantium, activa el RORα y potencia la expresión de BMAL1 (He et al., 2016). NOB reduce la proliferación celular e induce la detención del ciclo celular en varias líneas celulares de cáncer de mama, mientras que el tratamiento con NOB de las células de cáncer de ovario OVCAR3 potenció la apoptosis in vitro y redujo la angiogénesis y el crecimiento tumoral en xenoinjertos basados en OVCAR3 en ratones atímicos (Chen et al., 2015; Morley et al., 2007; Chen et al., 2014). En las células de cáncer gástrico, NOB reduce la proliferación, detiene el ciclo celular e induce la apoptosis (Yshimizu et al., 2004). En dos líneas celulares derivadas de diferentes tipos de tumores renales (ACHN y Caki-2), NOB interrumpe la señalización oncogénica, suprime la proliferación e induce la detención del ciclo celular y la apoptosis (Wei et al., 2019). Además, el tratamiento con NOB in vivo redujo de forma significativa el crecimiento de tumores de xenoinjertos basados en ACHN en cepas de ratones sin timo (Wei et al., 2019). Estos estudios plantean que NOB puede ralentizar el crecimiento de varios tipos de tumores. Cabe destacar que ninguno de estos estudios investigó si BMAL1 es necesario para los efectos de NOB. Curiosamente, la supresión del crecimiento celular de ACHN y Caki-2 inducida por el NOB parece contrastar con el crecimiento reducido de las líneas celulares de CCRC en las que BMAL1 está agotado (Mello et al., 2025). Estas diferencias pueden explicarse por contextos genéticos distintos: las líneas celulares de RCC utilizadas en el estudio del NOB expresan VHL WT (ACHN) o carecen de HIF2α (Caki-2) (Wei et al., 2019), mientras que el estudio de dependencia de BMAL1 se centró en modelos de carcinoma renal de células claras deficientes en VHL e impulsados por HIF2α (Mello et al., 2025).
Estos hallazgos ponen de manifiesto los efectos de la modulación circadiana, que dependen del contexto, y respaldan el amplio potencial terapéutico de los compuestos que potencian el reloj circadiano, como el NOB, especialmente cuando se tienen en cuenta las conexiones circadianas específicas de los tumores y las dependencias oncogénicas.
Es importante notar que muchos de los estudios analizados comparan los compuestos que actúan sobre el reloj biológico únicamente con controles de placebo, en lugar de con las quimioterapias de referencia, y que pocos evalúan su potencial en el contexto de las terapias combinadas. Estas lagunas remarcan la necesidad de realizar estudios futuros para determinar cuál es la mejor forma en que estos compuestos pueden complementar los regímenes de tratamiento existentes.
Medicina basada en el reloj biológico: tiempos óptimos de tratamiento para las terapias dirigidas
En otras publicaciones se pueden consultar revisiones exhaustivas de ensayos clínicos que evalúan los efectos de la hora del día en los resultados de la quimioterapia, la radioterapia, los inhibidores de puntos de control inmunitario y los fármacos quimioterapéuticos dirigidos de primera línea (Tellinga et al., 2025; Singh et al., 2025; El-Tanani et al., 2024; Zhang et al., 2025). Interesantemente, algunos estudios presentan resultados contradictorios, por ejemplo, con la temozolomida en el GBM (Geurts et al., 2025; Damato et al., 2022; Damato et al., 2021), lo que probablemente refleje diferencias en el diseño del estudio, la referencia a la hora del reloj frente al cronotipo, los subtipos moleculares y los criterios de valoración seleccionados. A pesar del creciente reconocimiento de que el momento del tratamiento puede influir en los resultados, siguen existiendo importantes retos para permitir la aplicación clínica de los conocimientos de la biología circadiana con el fin de mejorar el tratamiento del cáncer. En este artículo, analizamos los resultados de investigaciones preclínicas recientes que revelan explicaciones mecánicas de las respuestas divergentes a los tratamientos dirigidos en función de la hora del día en que se administra el fármaco.
Los glucocorticoides se utilizan habitualmente como terapia complementaria en pacientes con GBM para aliviar los síntomas del edema cerebral (Kostaras et al., 2014; Salvador et al., 2014). Se prefiere la dexametasona (DEX) debido a sus potentes efectos antiinflamatorios y a su capacidad para atravesar la barrera hematoencefálica (Salvador et al., 2014). Curiosamente, algunos estudios han informado de que la DEX inhibe el crecimiento tumoral, mientras que otros han demostrado que puede potenciar la proliferación del glioma (Afshari et al., 2022). Esta variabilidad podría explicarse en parte por las interacciones entre la señalización del receptor de glucocorticoides y el reloj circadiano. El receptor de glucocorticoides está regulado por componentes fundamentales del reloj circadiano (Lamia et al., 2011), lo que sugiere que el momento de la administración de la DEX podría influir en los resultados terapéuticos. En apoyo de esto, en modelos de xenoinjertos de GBM, la administración de DEX por la mañana (cuando los niveles de Per2 son bajos) potencia el crecimiento tumoral, mientras que la administración por la tarde (cuando los niveles de Per2 son altos) lo inhibe (Gonzalez-Aponte et al., 2025). De manera similar, en el cáncer de mama, donde se utiliza DEX para mitigar los efectos secundarios inducidos por la quimioterapia, DEX tiene actividad antitumoral en algunos contextos, pero otros estudios hallan que promueve la proliferación y la metástasis de las células de cáncer de mama (Zhidkova et al., 2020). Estos efectos divergentes, al igual que en el GBM, pueden verse influidos por el momento circadiano. En conjunto, estos estudios resaltan la relevancia de tener en cuenta la fase circadiana en la administración de glucocorticoides, especialmente cuando se utilizan como terapia complementaria en el cáncer. Optimizar el momento de la administración de DEX podría mejorar la eficacia terapéutica y minimizar los efectos protumorales no deseados.
Resultados recientes indican que el momento de la administración también podría influir en los resultados del belzutifán, un tratamiento relativamente nuevo para el carcinoma de células renales. Este tipo de cáncer se caracteriza por la pérdida de VHL (Sato et al., 2013), que marca a HIF1α y HIF2α para su degradación. VHL frena el crecimiento del carcinoma de células renales mediante la inhibición de la actividad de HIF2α (Courtney et al., 2020; Kondo et al., 2002), lo que subraya la función oncogénica de HIF2α en él. Dado su papel central en la progresión tumoral, se han dedicado grandes esfuerzos al desarrollo de un compuesto que inhiba la dimerización de HIF2α-ARNT. Esto condujo a la aprobación por parte de la FDA en 2021 de belzutifán (anteriormente denominado PT2977) para el carcinoma renal de células claras sin VHL (Deeks, 2021). Sin embargo, la resistencia sigue siendo un reto importante, ya que casi un tercio de los xenoinjertos derivados de pacientes con carcinoma renal de células claras no responden a los antagonistas de HIF2α como el PT2399, que está estrechamente relacionado con el belzutifán (Courtney et al., 2020; Chen et al., 2016). BMAL1 se expresa en niveles elevados en muestras clínicas de carcinoma renal de células claras, y los heterodímeros BMAL1-HIF2α favorecen el crecimiento tumoral en modelos de xenoinjertos (Mello et al., 2025). Los xenoinjertos derivados de pacientes sensibles a la inhibición del crecimiento por el PT2399 expresan niveles más altos de BMAL1 en comparación con los injertos tumorales resistentes (Chen et al., 2016), y los modelos de xenoinjertos derivados de líneas celulares son sensibles a la supresión por el PT2399 cuando el fármaco se administra al inicio de la fase de luz —cuando la expresión de BMAL1 es alta— y resistentes cuando se administra a los ratones al inicio de la fase de oscuridad (Mello et al., 2025).
Esto sugiere que los resultados de los pacientes tratados con belzutifán podrían mejorar si se les trata cuando la expresión de BMAL1 es elevada en sus tumores. Si el tratamiento con NOB aumenta la expresión de BMAL1 en el carcinoma renal con células claras, la terapia combinada con un antagonista de HIF2α y NOB podría dar lugar a mejores resultados. Son necesarias más investigaciones para explorar estas posibilidades.
Aprovechar la capacidad destructora del sistema inmunitario constituye una potente estrategia terapéutica para diversos tipos de cáncer, que a menudo genera respuestas duraderas (Mellman et al., 2011). Los ritmos circadianos regulan las funciones inmunitarias, provocando oscilaciones en los niveles de leucocitos, el reclutamiento tisular y la actividad inflamatoria —factores que determinan tanto el curso de las enfermedades agudas como de las crónicas y que resaltan la importancia del momento de la intervención (Scheiermann et al., 2013).
Los ritmos endógenos de los leucocitos, las oscilaciones en la infiltración inmunitaria del tumor y los relojes circadianos de las células endoteliales del microambiente tumoral influyen en el crecimiento tumoral y en las respuestas a las inmunoterapias, incluidas los inhibidores de punto de control inmunitario y la terapia con células CAR-T, en modelos preclínicos (Wang et al., 2024). En modelos de melanoma, cáncer de pulmón y cáncer colorrectal, las terapias anti-PD-1 y anti-PD-L1 son más eficaces cuando se administran a ratones en la fase activa temprana (Fortin et al., 2024; Wang et al., 2024). En consonancia con la investigación preclínica, los pacientes con cánceres avanzados de estómago (Tankaka et al., 2024), riñón (Rizzo et al., 2025) o melanoma (Qian et al., 2021) presentan mejores resultados con la administración matutina de inhibidores de punto de control inmunitario en comparación con los pacientes tratados más tarde durante el día. Se han descrito resultados inconsistentes en cuanto al momento óptimo de administración de los inhibidores de punto de control inmunitario en el cáncer de pulmón no microcítico: un estudio clínico retrospectivo mostró una mayor supervivencia con el tratamiento al final del día (Guo et al., 2025), mientras que otro informó de mejores resultados con la administración temprana en los pacientes (Zhang et al., 2025), lo que sugiere que factores como el cronotipo, los perfiles circadianos específicos del tumor o el estilo de vida del paciente pueden influir en la ventana terapéutica. Hacen falta más estudios para replicar estos hallazgos en otros centros y comprender cómo el tiempo circadiano influye en las respuestas a los inhibidores de punto de control inmunitario en pacientes con diversos tipos de tumores, con el fin de respaldar la integración de la cronoterapia en futuras estrategias de tratamiento del cáncer.
CONCLUSIONES Y PERSPECTIVAS FUTURAS
Los ritmos circadianos regulan procesos fisiológicos clave que influyen en el desarrollo y la progresión del cáncer, entre ellos la progresión del ciclo celular, la reparación del daño en el ADN, el metabolismo, la vigilancia inmunitaria, la adaptación a la hipoxia y la metástasis. La alteración de los ritmos circadianos puede modificar significativamente el crecimiento tumoral y las respuestas terapéuticas. Sin embargo, este impacto depende en gran medida del contexto, lo que subraya la necesidad de realizar estudios mecanísticos más exhaustivos que investiguen el papel del reloj circadiano en diversos tipos de cáncer.
La intervención directa sobre los componentes del reloj circadiano es una estrategia emergente y prometedora para frenar el crecimiento tumoral. Las moléculas pequeñas, como los agonistas de REV-ERB, los estabilizadores de CRY y NOB muestran efectos antitumorales. Sin embargo, dado que el reloj circadiano sustenta la homeostasis de los tejidos normales, la inhibición sistémica con estos agentes puede plantear riesgos de toxicidad. Dirigirse a proteínas del reloj molecular secuestradas selectivamente por los tumores (por ejemplo, BMAL1-HIF2α en el carcinoma renal con células claras o la degradación de MYC mediada por CRY2 en el linfoma) podría ofrecer una mayor seguridad y eficacia.
La traslación clínica de la medicina circadiana se enfrenta a obstáculos, entre los que se incluyen los retos logísticos de la terapia sincronizada, la variabilidad de los ritmos individuales y la necesidad de biomarcadores robustos, como el cronotipado basado en sangre. Los ensayos prospectivos que incorporen el cronotipo del paciente y los perfiles circadianos específicos del tumor serán clave para el avance de este campo. Estos esfuerzos podrían abrir el camino a un uso más seguro y eficaz de las terapias citotóxicas, dirigidas e inmunológicas en oncología.
El reloj circadiano es un potente modulador de la biología del cáncer, aunque depende del contexto. Sus complejas funciones exigen un enfoque específico para el cáncer a la hora de su aplicación clínica. Los esfuerzos futuros deberían centrarse en integrar el perfil circadiano en el diagnóstico, perfeccionar las cronoterapias selectivas y diseñar ensayos clínicos que tengan en cuenta los efectos de la hora del día. Estas estrategias son fundamentales para aprovechar todo el potencial de la medicina circadiana en la era de la oncología de precisión.
Financiación
Este trabajo es fruto de la financiación, total o parcial, de los NIH y está sujeto a la Política de Acceso Público de los NIH. Al aceptar esta financiación federal, se ha concedido a los NIH el derecho a poner el trabajo a disposición del público en PubMed Central.
Subvenciones del Instituto Nacional del Cáncer CA211187 y CA271500 (a KAL).
Subvenciones del Instituto Nacional del Cáncer R01CA244519 y R01CA259370 (a SM).
