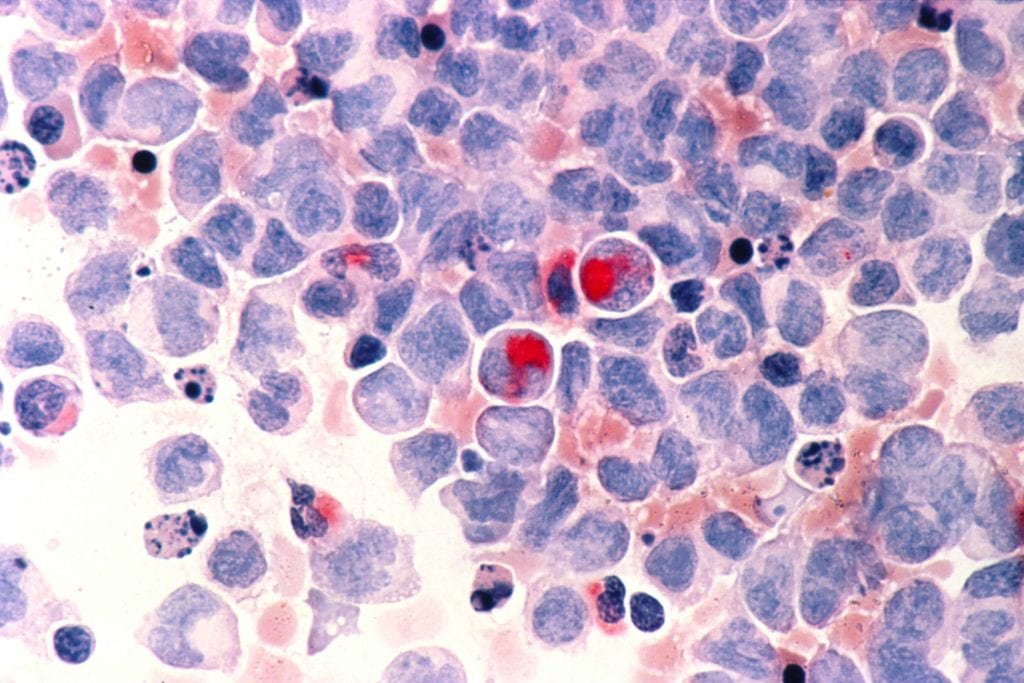
Un reciente estudio, publicado en el Journal of the American Medica Association, revela que los pacientes de leucemia mieloide aguda con mutaciones que han persistido en sus células tras la quimioterapia, tienen un mayor riesgo de recaída de la enfermedad.
La leucemia mieloide aguda (LMA) es un tipo de cáncer caracterizado por la proliferación anormal de los mieloblastos – células que tras diferenciarse dan lugar a algunos tipos de glóbulos blancos – en la médula ósea, lo que interfiere con la producción de las células sanguíneas normales y da lugar a que éstas no se generen en las cantidades necesarias para el organismo.
Leucemia mieloide aguda y recaídas
A pesar de las recientes mejoras en el tratamiento de la leucemia mieloide aguda, un 20% de los pacientes no logra alcanzar la remisión tras la quimioterapia, e incluso en los casos en los que si se consigue una completa remisión, un 50% sufren recaídas posteriormente. Ante esta situación, es vital el desarrollo de métodos que permitan diferenciar a los pacientes de mayor riesgo a sufrir recaídas, para así tener tiempo para tomar las medidas terapéuticas necesarias.
Bajo la forma de un estudio retrospectivo, los investigadores analizaron el perfil genómico de las muestras tomadas en el momento del diagnóstico de 71 pacientes con LMA que habían tratados con quimioterapia. El análisis del patrón de mutaciones no mostró diferencias entre los pacientes en los que la enfermedad había remitido y los pacientes que habían experimentado una recaída. A continuación, el equipo analizó 50 pacientes de los que se disponía tanto de material obtenido en el diagnóstico, como de muestras obtenidas 30 días tras la terapia de inducción de la remisión. La mitad de estos pacientes contenían, en el momento de la remisión, al menos un 5% de células de la médula ósea con mutaciones persistentes asociadas a la leucemia. Interesantemente, este grupo de pacientes había mostrado una tasa de supervivencia menor, con una mediana de tiempo de supervivencia de 10.5 meses, en comparación a la de los pacientes cuyas mutaciones habían sido eliminadas con la quimioterapia inicial, que alcanzaban los 42 meses de mediana.

Además, los investigadores observaron que no todas las mutaciones son eliminadas con la misma eficacia tras la quimioterapia convencional. Mutaciones en genes como DNMT3A, TET2, IDH1 e IDH2, relacionadas con el inicio de la enfermedad, no se eliminan de forma eficaz, al contrario de lo que sucede con mutaciones en los genes FLT3, NPM1 o KRAS.
Los resultados del trabajo indican que llevar a cabo el análisis genómico de los pacientes con LMA después de la quimioterapia e identificar si han resistido el tratamiento suficientes células con mutaciones asociadas a la enfermedad como para dar lugar a una recaída del paciente es eficiente para predecir la evolución de la enfermedad. También proporcionan información sobre la estructura clonal de los pacientes con LMA e indican que la eliminación de las células con mutaciones fundadoras, relacionadas con la inducción inicial de la enfermedad, es fundamental para el éxito del tratamiento.
Los investigadores resaltan que los resultados obtenidos en el trabajo están construidos a partir de los datos de hace más de una década, en los que se sugería que el aumento en el riesgo de recaídas de la LMA estaba asociado una eliminación ineficiente de las células de leucemia con anormalidades cromosómicas. Sin embargo, la imposibilidad de analizar el genoma para obtener una imagen más detallada había impedido profundizar más en la materia.
Aunque el estudio deberá confirmarse en una muestra de mayor tamaño, los datos indican que el análisis genómico de las células de la LMA tras obtener la remisión de los pacientes por quimioterapia puede mejorar la clasificación de los mismos en base al riesgo a desarrollar una recaída, llevando en definitiva, a un mejor manejo de los pacientes.
“Si nuestros resultados son confirmados en estudios prospectivos más amplios, el perfil genético tras la quimioterapia inicial podría ayudar a los oncólogos a predecir el pronóstico de forma temprana en la leucemia de un paciente, y determinar si el paciente ha respondido a la quimioterapia, sin tener que espera que el cáncer recurra,” manifiesta Jeffery M Klco, primer autor del trabajo. El investigador indica que esta aproximación de obtener perfiles genéticos a partir de la secuenciación del genoma tras el tratamiento inicial del paciente, podría resultar también útil para otros tipos de cáncer.
Amparo Tolosa, Genética Médica News
Referencias:
Klco JM, et al. Association Between Mutation Clearance After Induction Therapy and Outcomes in Acute Myeloid Leukemia. JAMA. 2015 Aug 25;314(8):811-22. doi: 10.1001/jama.2015.9643.
Pastore F, Levine RL. Next-Generation Sequencing and Detection of Minimal Residual Disease in Acute Myeloid Leukemia: Ready for Clinical Practice? JAMA. 2015 Aug 25;314(8):778-80. doi: 10.1001/jama.2015.9452.
Fuente:

