Amparo Tolosa, Genética Médica News
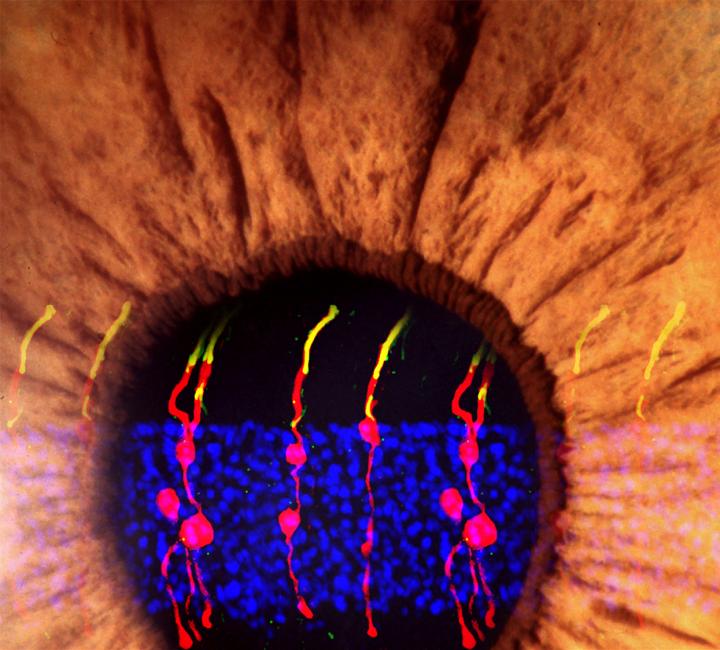
Investigadores de diversas instituciones internacionales han conseguido revertir la ceguera congénita en ratones mediante la reprogramación genética. Los resultados del trabajo plantean una nueva aproximación de tratamiento para los pacientes humanos afectados por esta enfermedad.
Los investigadores han conseguido generar células fotorreceptoras de la retina, aquellas que reciben la luz e inician la transmisión de esta información hacia el cerebro, a partir de células gliales, células de apoyo encargadas, entre otras funciones, del mantenimiento de las células de la retina. En mamíferos estos dos tipos de células no se regeneran. Sin embargo, en el caso del pez cebra se ha observado que cuando se producen daños en la retina las células de la glía de Müller son capaces de activar su proliferación de forma espontánea y generar células madre que se diferencian en neuronas de la retina para restaurar la visión.
Las características especiales de las células de la glía de Müller en pez cebra llevaron a pensar a los investigadores que, aunque en mamíferos estas células no se dividan en respuesta a los daños, quizás tengan todavía el potencial, la maquinaria molecular necesaria, para regenerar las células fotorreceptoras.
Así pues, los investigadores se plantearon como objetivo determinar si es posible activar la maquinaría y reprogramar las células de la glía de Müller de mamíferos para producir células fotorreceptoras.
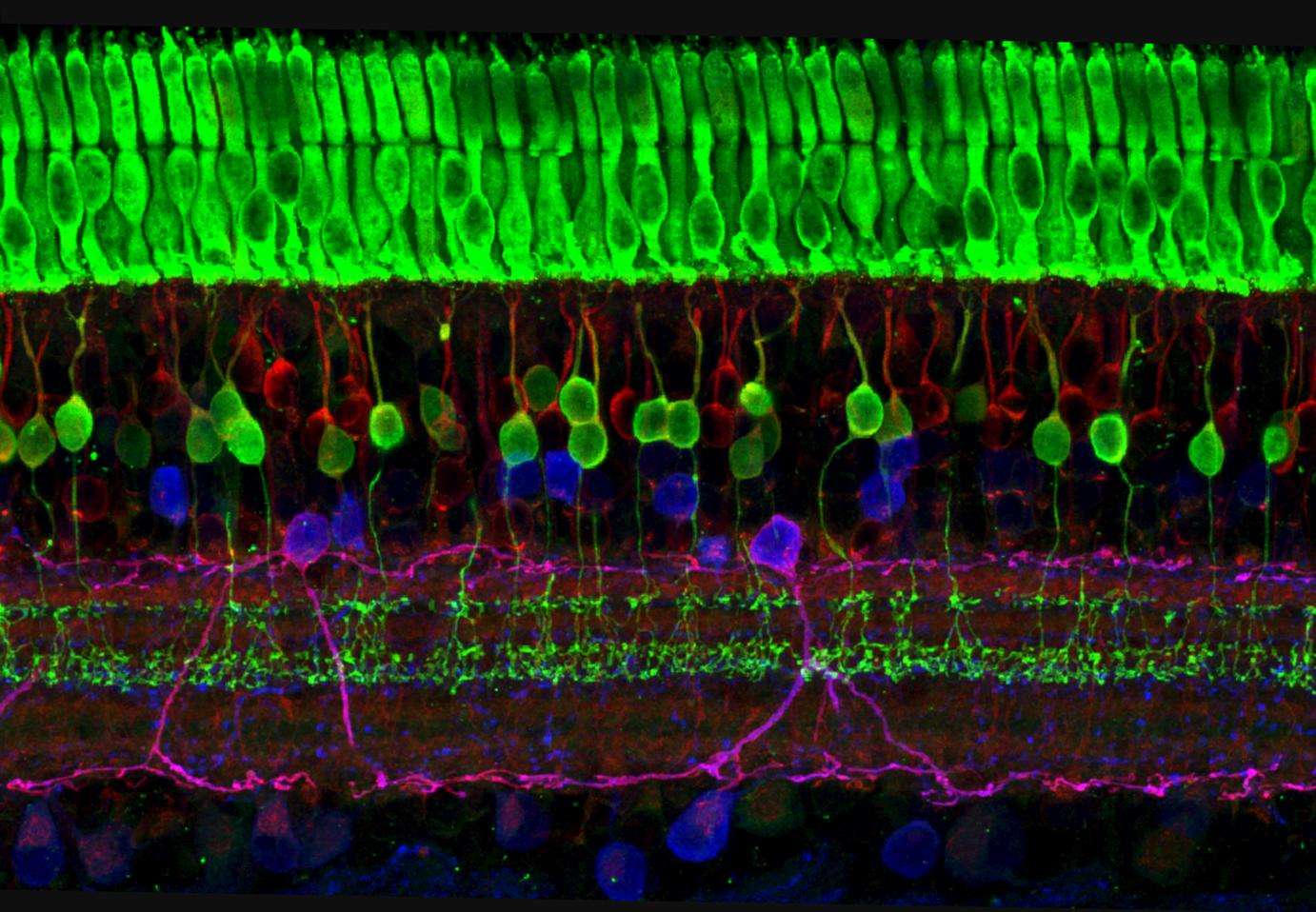
Para responder a esta pregunta utilizaron un modelo de ceguera congénita en ratón. En una primera fase, el equipo inyectó en los ojos de los ratones el gen que codifica para la beta-catenina, proteína que estimula la división de las células de la glía de Müller. Dos semanas después, los investigadores realizaron una segunda inyección, esta vez con un cóctel de genes dirigido exclusivamente a las células de la glía de Müller y destinado a hacer que las células generadas se diferenciaran en un tipo de células fotorreceptoras.
Los investigadores confirmaron que el tratamiento en dos fases generaba una población de células fotorreceptoras (concretamente, de un tipo denominado bastones) funcionales. Estas células eran capaces de comunicarse con otras células de la retina para, en última instancia, completar el circuito visual hasta el cerebro. Además, eran capaces de restaurar la visión de los ratones modelo con ceguera congénita.
Los resultados del trabajo sugieren que es posible reprogramar las células de la glía de Müller de la retina de los mamíferos para generar nuevos fotorreceptores.
En la actualidad los investigadores realizan estudios de comportamiento para evaluar si los animales tratados pueden realizar tareas visuales normales. Las pruebas muestran que los ratones ven, pero todavía será necesario evaluar cuánto o cómo de bien. El equipo también prepara diversos análisis para comprobar si las células de la glía de Müller humanas también pueden ser reprogramadas.
En el caso de confirmar que esta estrategia puede utilizarse también en humanos podría tener importantes aplicaciones. Por ejemplo, podría ser utilizada para regenerar las neuronas de la retina que se pierden durante algunas enfermedades neurodegenerativas, o reparar los daños en este tejido ocurridos en diversas enfermedades oculares.

“Este es el primer trabajo en el que los investigadores reprograman las células de la glía de Müller para convertirse en bastones fotorreceptores de la retina de mamíferos”, ha señalado Thomas N Greenwell, director del programa de neurociencia de la retina en el Instituto Nacional de la Visión de EE.UU., organismo que ha financiado las investigaciones. “Los bastones nos permiten ver con luz baja pero también nos ayudan a preservar los conos, que son importantes para la visión del color y la agudeza visual. Los conos tienden a morir en las últimas fases de las enfermedades oculares. Si los bastones pueden ser regenerados desde dentro del ojo, podría ser una estrategia para tratar las enfermedades del ojo que afectan a los fotorreceptores”.
No obstante, antes de que se pueda plantear si quiera su utilización en humanos, los investigadores deberán responder a diversas preguntas como si las células de la glía de Müller humanas serían capaces de regenerar los fotorreceptores en presencia de daños en la retina o si el reducido número de estas células sería capaz de regenerar suficientes bastones como para que se produzca una restauración completa o sustancial de la visión.
Referencia: Yao K, et al. Restoration of vision after de novo genesis of rod photoreceptors in mammalian retinas. Nature. 2018. Doi: https://doi.org/10.1038/s41586-018-0425-3
Fuente: NIH-funded researchers reverse congenital blindness in mice. https://nei.nih.gov/content/nih-funded-researchers-reverse-congenital-blindness-mice


