Amparo Tolosa, Genética Médica News
Investigadores de la Universidad de California San Francisco han desarrollado las primeras células madre pluripotentes universales, que podrían ser utilizadas en trasplantes sin ser detectadas por el sistema inmunitario y por lo tanto, sin provocar rechazo por parte de los receptores .
Desde hace unos años las células madre pluripotentes se han presentado como una prometedora herramienta para la medicina regenerativa y el tratamiento de algunas enfermedades humanas. El interés de estas células radica en dos características principales: se renuevan y son capaces de generar la mayor parte de los tejidos del cuerpo.

Dentro de los diferentes tipos de células madre pluripotentes, aquellas que pueden ser generadas a partir de células adultas han recibido una especial atención en el área de la terapia celular. Estas células, denominadas células madre pluripotentes inducidas o iPS, pueden obtenerse a partir de la reprogramación células de adultas del propio paciente para generar una fuente inagotable de células madre con las que tratar la enfermedad.
En teoría, utilizar células del propio paciente tiene la ventaja de evitar el posible rechazo del organismo al tratamiento celular, debido a que al ser reconocidas como propias, el sistema inmunitario no debería inducir una respuesta frente a las mismas. Sin embargo, en la práctica esta aproximación no ha resultado tan efectiva como se esperaba debido a que requiere generar células iPS de cada paciente, lo que resulta laborioso y requiere mucho tiempo y coste. En estas condiciones, los ensayos realizados sugieren que solo se obtendría un rendimiento adecuado en el caso de enfermedades crónicas ya que el tiempo necesario para generar las células solo permite producir células para condiciones crónicas y no para aquellas que se presentan de forma aguda.
Una solución a estas limitaciones sería utilizar células madre pluripotentes alogénicas, es decir, obtenidas de otra persona más o menos compatible. En este caso sería necesario recurrir a tratamientos complementarios destinados a suprimir al sistema inmunitario, estrategia que tiene sus riesgos, como un aumento en la susceptibilidad a otras enfermedades. Por lo tanto, la estrategia óptima sería disponer de células madre pluripotentes que pudieran ser utilizadas en cualquier paciente sin desencadenar una respuesta inmunitaria frente a ellas, esto es, células madre pluripotentes universales.
Con este objetivo, un equipo de investigadores de la Universidad de California San Francisco ha utilizado la herramienta de edición del genoma CRISPR para introducir cambios en células madre pluripotentes destinados a hacerlas “invisibles” para el sistema inmunitario.
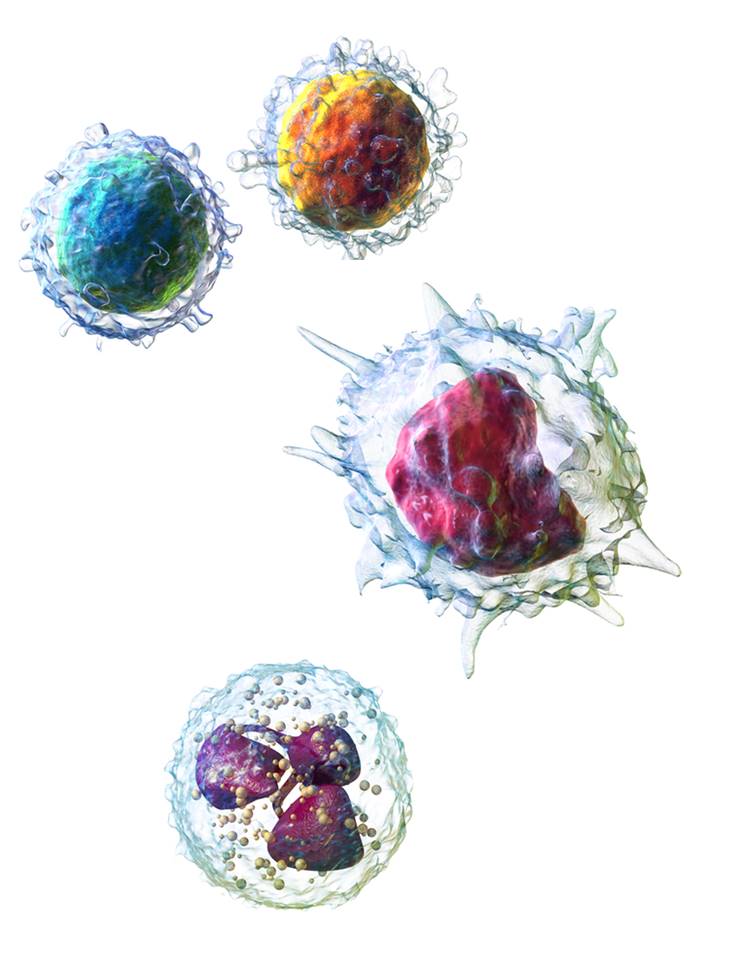
Los investigadores han conseguido reducir la inmunogenicidad de las células madre pluripotentes mediante tres modificaciones genéticas. En primer lugar el equipo utilizó la herramienta de edición del genoma CRISPR para eliminar secuencialmente la expresión de dos moléculas necesarias para la formación de los complejos de histocompatibilidad de clase I y clase II (MHCI y MHCII, respectivamente). Los MHC son estructuras de superficie celular que las células utilizan para presentar antígenos que serán reconocidos por los linfocitos T del sistema inmunitario. Ambos complejos intervienen en el desarrollo de la respuesta inmunitaria humoral y mediada por células. Además, debido a su importante variabilidad entre personas, tienen un papel importante en la diferente susceptibilidad a enfermedades o el rechazo de trasplantes.
Las células sin MHC no pueden exponer fragmentos de sus proteínas en la superficie para ser reconocidas por los linfocitos T del sistema inmunitario como propias o ajenas, por lo que en esencia se vuelven “invisibles” para estas células. Sin embargo, sí son reconocidas y eliminadas por otras células, las denominadas natural killer. Para evitar que esto suceda, los investigadores introdujeron una tercera modificación en las células, destinada a aumentar la expresión del gen CD47. Estudios previos indicaban que la proteína codificada por CD47 actúa como señal frente a algunas células del sistema inmunitario, como las células natural killer para impedir que estas células las ataquen. Por esta razón, los investigadores hipotetizaron que aumentar la expresión de CD47 en las células modificadas para no producir MHC podría hacer que evadieran no solo el reconocimiento por parte de linfocitos T, sino también por parte de las células natural killer.
El equipo desarrolló células madre pluripotentes inducidas con baja reactividad inmunológica tanto a partir de células madre pluripotentes inducidas de ratón como humanas. En todos los casos comprobaron, en primer lugar, que las carecían de MHC y expresaban CD47 en mayores cantidades que las células sin modificar. En segundo lugar, comprobaron que las células mantenían su capacidad de regeneración y de diferenciación en múltiples tipos celulares.
“Hay muchos problemas con la tecnología iPSC, pero las principales limitaciones son el control de calidad y la reproducibilidad”, manifiesta Tobias Deuse, jefe de Cirugía Cardiaca en la Universidad de California San Francisco y primer autor del estudio. “No sabemos qué hace que algunas células sean susceptibles a la reprogramación pero muchos científicos están de acuerdo en que todavía no puede hacerse de forma fiable. La mayoría de aproximaciones para las terapias iPSC individualizadas han sido abandonadas por esta razón”.
Los investigadores trasplantaron células pluripotentes modificadas de ratón en ratones no compatibles y observaron que no eran rechazadas ni atacadas por el sistema inmunitario de los ratones. De forma similar, trasplantaron las células pluripotentes modificadas humanas en ratones cuyo sistema inmunitario había sido modificado para parecerse lo máximo posible al humano y obtuvieron los mismos resultados. De este modo comprobaron que las células pluripotentes “universales” no inducían una respuesta inmunitaria.
“Esta es la primera vez que alguien diseña células que pueden ser trasplantadas de forma universal y pueden sobrevivir en receptores inmunocompetentes sin provocar una respuesta inmunitaria”, indica Tobias Deuse.
Por último, para evaluar el potencial de las células pluripotentes modificadas en una situación lo más parecida posible a un trasplante, los investigadores obtuvieron células endoteliales, musculares y cardiacas a partir de las células madre modificadas y las trasplantaron en ratones con un sistema inmunitario humanizado. Las células pluripotentes universales no provocaron rechazo por parte del sistema inmunitario, a pesar de no ser compatibles inmunológicamente con los receptores, y además, sobrevivieron durante un periodo prolongado de tiempo sin necesidad de recurrir a fármacos inmunosupresores.
Los resultados del trabajo plantean que es posible generar células madre pluripotentes universales para ser utilizadas en trasplantes sin importar la compatibilidad inmunitaria de los receptores.
“Nuestra técnica resuelve el problema de rechazo de las células madre y tejidos derivados de células madre, y representa un importante avance en el campo de la terapia con células madre”, señala Deuse. “Nuestra técnica puede beneficiar a un amplio rango de personas con costes de producción que son más bajos que cualquier aproximación individualizada. Solo necesitamos producir nuestras células una vez y tenemos un producto que puede ser aplicado de forma universal”.
Referencia: Deuse T, et al. Hypoimmunogenic derivatives of induced pluripotent stem cells evade immune rejection in fully immunocompetent allogeneic recipients. Nat biotech. 2019. Doi: https://doi.org/10.1038/s41587-019-0016-3
Fuente: CRISPR Gene Editing Makes Stem Cells ‘Invisible’ to Immune System. https://www.ucsf.edu/news/2019/02/413311/crispr-gene-editing-makes-stem-cells-invisible-immune-system


