Amparo Tolosa, Genética Médica News
Aunque el sistema CRISPR es conocido principalmente por su utilización en la edición del genoma, desde sus inicios ha sido presentado como una herramienta muy versátil, con capacidad para adaptarse a diferentes aproximaciones biotecnológicas. Dentro de las innovaciones en el área de CRISPR se encuentran la posibilidad de modificar el epigenoma o el reciente desarrollo de una amplificación del ADN sin ciclos de temperatura. A la creciente lista, ya podemos añadir una aplicación más: la detección de mutaciones en muestras de ADN.
Primero en la Universidad de California Berkely y después en el Instituto Keck de Postgrado de las Facultades Claremont, la investigadora Kiana Aran ha dirigido el diseño y puesta a punto de un dispositivo que combina las propiedades del grafeno y la tecnología CRISPR para detectar, en cuestión de minutos, mutaciones genéticas concretas en muestras de ADN.
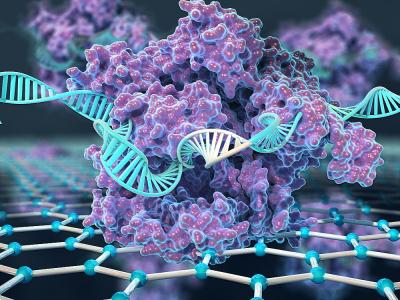
El dispositivo consiste en un transistor de grafeno sobre el que se han inmovilizado miles de complejos CRISPR. Cada complejo CRISPR está formado por una enzima Cas9 inactivada y un ARN guía diseñado para reconocer un fragmento específico del ADN.

Cuando se utiliza CRISPR como sistema de edición del genoma, ADN y complejos CRISPR están en solución y el ARN posiciona a la enzima nucleasa Cas9 en la región de interés a modificar. En el caso del nuevo dispositivo, el complejo CRISPR está inmovilizado sobre una superficie de grafeno, extremadamente sensible a moléculas cargadas, como el ADN. Cuando se añade la muestra de ADN al dispositivo, si la región del genoma que se quiere detectar no está presente en la misma, no es reconocido por los complejos CRISPR y por lo tanto, no se une a estos y el ADN permanece libre en la solución. Si la secuencia diana está presente en ADN, el ADN se unirá al complejo CRISPR correspondiente a través de la región de interés, lo que crea una carga adicional en la superficie de grafeno que es detectada por el dispositivo y puede ser registrada e identificada. Así, pues la diferencia de carga eléctrica es lo que marca la presencia del ADN diana.
“CRISPR proporcionó la selectividad y los transistores de grafeno la sensibilidad”, destaca Kiana Aran. “Combinar la nanoelectrónica actual con la biología actual abre una nueva puerta para acceder a nueva información biológica que no era accesible antes”.
Hasta el momento, los investigadores han utilizado con éxito CRISPR-Chip, como se denomina el dispositivo, para detectar la presencia de mutaciones responsables de la distrofia muscular de Duchenne, y están desarrollando nuevos complejos que reconozcan mutaciones responsables de otros trastornos genéticos. “CRISPR-Chip tiene la ventaja de marcar un punto en cuidado al paciente”, indica Niren Murthy profesora de ingeniería en la Universidad de California Berkeley y coautora del trabajo. “Es una de las pocas cosas que se podría realmente hacer en consulta si tienes una buena muestra de ADN. El último término solo hace falta tomar las células de una persona, extraer el ADN y mezclarlo con el chip de CRISPR para ser capaz de decir si una determinada secuencia de ADN está presente o no. Eso podría potencialmente llevar a una verdadera prueba de ADN inmediata”.
CRISPR-Chip presenta varias ventajas. En primer lugar, no requiere la amplificación de ADN, ya que el grafeno es lo suficientemente sensible como para detectar la secuencia de interés directamente de la muestra. En segundo lugar, el análisis de la muestra se produce en cuestión de minutos, en un dispositivo de mano, que puede estacionarse en cualquier localización.
El equipo de investigadores reconoce que todavía es pronto para utilizar el dispositivo en un contexto clínico y será necesario un periodo de optimización. No obstante, puede representar una herramienta de gran interés para el diseño y optimización de ARNs guía. Dado que CRISPR-Chip depende de la capacidad de los complejos CRISPR para reconocer la diana de interés, el dispositivo podría ser utilizado para seleccionar los ARNs guía que serán utilizados en otras aproximaciones CRISPR según su efectividad y precisión.
Referencia: Hajian R, et al. Detection of unamplified target genes via CRISPR–Cas9 immobilized on a graphene field-effect transistor. Nat Biom Eng. 2019. Doi: https://doi.org/10.1038/s41551-019-0371-x
Fuente: New CRISPR-powered device detects genetic mutations in minutes. https://news.berkeley.edu/2019/03/25/new-crispr-powered-device-detects-genetic-mutations-in-minutes/



