Amparo Tolosa, Genotipia
Investigadores del Instituto Broad del Instituto de Tecnología de Massachusetts y la Universidad de Harvard, la Universidad de Vanderbildt y el Instituto de Salud de EE.UU. han tratado con éxito la progeria en un modelo en ratón a través de la utilización de editores de bases para reparar la causa genética de la enfermedad. Los resultados del trabajo, uno de los primeros en abordar la efectividad de los editores de bases in vivo, han conseguido extender la vida de los animales modelo más allá de lo esperado y muestran potencial para que estas herramientas se conviertan, una vez optimizadas, en terapias reales.
“Cuando mi laboratorio de investigación identificó la causa de la progeria en 2003, esperábamos que algún día esto llevara a una forma de ayudar a estos niños”, señala Francis Collins, director del Instituto Nacional de Salud e investigador en el Instituto Nacional de Investigación del Genoma Humano y uno de los directores del trabajo. “A lo largo del camino hemos hecho algunos progresos con terapia farmacológica pero el potencial de realmente corregir la causa fundamental a nivel de ADN está más allá de cualquier cosa que hubiéramos imaginado entonces. Ver esta dramática respuesta en nuestro modelo en ratón de progeria es uno de los desarrollos terapéuticos más emocionantes en los que he participado en 40 años como médico científico” destaca el investigador.
Evaluación de los editores de bases como terapia para la progeria
La progeria o síndrome de progeria de Hutchinson-Gilford es una enfermedad genética caracterizada por el envejecimiento acelerado. Sus síntomas comienzan en la infancia y derivan en serias complicaciones, como la arteriosclerosis, que empeoran rápidamente y llevan a una muerte prematura. La causa de la enfermedad, desconocida hasta hace apenas 20 años, es la presencia de mutaciones en una de las copias del gen LMNA, que codifica para la proteína lamina A, esencial para la membrana nuclear. En la mayor parte de los pacientes con progeria, la mutación responsable es un cambio de citosina a timina que genera una proteína truncada llamada progerina que compromete la función de la proteína nuclear y lleva a la muerte celular.
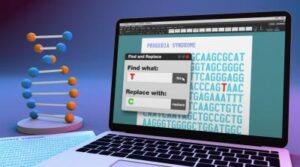
Para corregir la mutación, los investigadores han recurrido a los editores de bases, derivados del sistema CRISPR que permiten introducir cambios puntuales específicos en el ADN sin generar puntos de rotura en la doble cadena de la molécula hereditaria.
En una primera aproximación, los investigadores utilizaron una estrategia in vitro y trataron células derivadas de pacientes con progeria con lentivirus que contenían editores de bases. En este caso, observaron una reducción en la producción de progerina y una mejora en la morfología del núcleo celular, lo que indicaba efectos funcionales positivos.
A continuación, el equipo se planteó si la estrategia podría funcionar en un sistema in vivo. Para ello, el equipo empaquetó los componentes del sistema en virus adenoasociados y utilizó una inyección sistémica para hacerlos llegar a las células de ratones modelo para la progeria de tres o catorce días después de su nacimiento.
Los animales tratados crecieron de forma aparentemente sana y sobrevivieron una media de 510 días, más de dos veces que los ratones con progeria no tratados. Además de este efecto sobre la longevidad, los investigadores encontraron que varios meses tras el tratamiento único los ratones no presentaban los defectos característicos de deterioro de las arterias, sino que mostraban arterias similares a las de los ratones sanos.
A nivel molecular, el equipo detectó una corrección génica entre el 10 y el 60% en diferentes tejidos, así como una reducción de la proteína progerina, lo que explica las notables mejoras observadas respecto a los ratones control de la enfermedad.
“En nuestro conocimiento este trabajo es el que resulta en un mayor rescate de los síntomas de la progeria a través de múltiples medidas”, señala David Liu, director del Instituto Merkin de Tecnologías Transformativas en Sanidad del Instituto Broad, investigador en el Instituto Médico Howard Hughes y profesor en la Universidad de Harvard. “Hace cinco años estábamos terminando el desarrollo del primer editor de bases. Si me hubieran dicho que en cinco años una única dosis de un editor de bases podría dirigirse a la progeria en un animal, a nivel de ADN, ARN, proteína, patología vascular, patología y esperanza de vida, habría dicho que no era posible. Es un testamento real a la dedicación del equipo que ha hecho posible este trabajo”.
Tasa de edición eficiente y precisión
El éxito de cualquier estrategia de edición del genoma como terapia para una enfermedad genética depende de la tasa de edición genética y la precisión con que introduce los cambios deseados sin modificar otras regiones del ADN. A partir de los estudios en cultivo de células derivadas de pacientes y modelos in vivo en ratón, la tasa de edición del genoma reduce la producción de progerina lo suficiente como para inducir cambios en la fisiología de la célula e inducir cambios significativos. Respecto a la inducción de cambios en el genoma, los investigadores no han encontrado evidencias de que el editor de bases utilizado reconozca y modifique otras regiones del ADN.
Cuestiones por resolver para la terapia de la progeria con editores de bases
Si bien los resultados son muy prometedores, la estrategia todavía debe ser optimizada antes de plantear su posible utilización en humanos. Los investigadores han detectado la formación de tumores de hígado en algunos de los animales tratados más longevos, lo que es consistente con lo que muestran otros estudios donde se han utilizado virus adenoasociados en ratón. En este caso, sin embargo, la causa de la aparición de tumores no está clara. El equipo ha encontrado que los ratones modelo con progeria utilizados son portadores una duplicación del gen RAB25 humano. La sobreexpresión del gen está relacionada con el carcinoma hepatocelular humano, por lo que deberá investigarse si es esta la causa o si se trata de un efecto de la utilización de vectores víricos.
Artículo original: Koblan LW, et al. In vivo base editing rescues Hutchinson–Gilford progeria syndrome in mice. Nature. 2021. DOI: https://doi.org/10.1038/s41586-020-03086-7
Fuentes:
Vermeij WP y Hoeijmakers HHJ. Base editor repairs mutation found in the premature-ageing syndrome progeria. Nature. 2021. DOI: https://doi.org/10.1038/d41586-020-03573-x
Base editing successfully treats progeria in mice. https://www.broadinstitute.org/news/base-editing-successfully-treats-progeria-mice
Si te ha gustado esta noticia y quieres aprender más sobre Genética en Medicina, te interesan nuestros cursos y formación universitaria, así como nuestro canal audiovisual, Genotipia TV.