María Hernández Sánchez1,2,3 y Jesús María Hernández Rivas1,2,3
- Genética molecular en oncohematología. Instituto de Investigación Biomédica de Salamanca, Salamanca.
- Unidad de Citogenética Molecular. Centro de Investigación del Cáncer, Salamanca.
- Servicio de Hematología. Hospital Universitario de Salamanca, Salamanca.
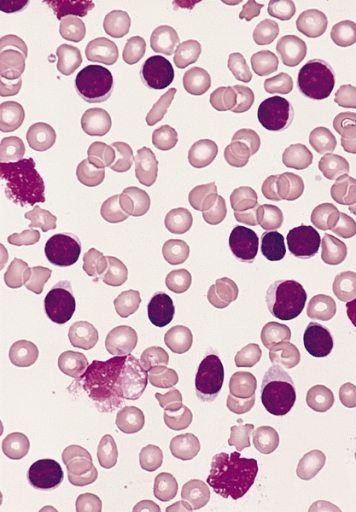
La evolución clonal es un proceso complejo que se caracteriza por los cambios genéticos que se van produciendo con el tiempo en las células cancerosas. Este fenómeno juega un papel fundamental en el desarrollo del cáncer en el que algunos clones tumorales van adquiriendo mutaciones proporcionándoles una mayor ventaja selectiva (mutaciones “drivers”). Su mejor comprensión nos podría ayudar a entender cómo evolucionan los enfermos con un estado inicialmente indolente a una forma más agresiva, así como a aplicar estrategias terapéuticas más eficaces para evitar las recaídas.
La leucemia linfática crónica (LLC) es una neoplasia hematológica que suele comenzar sin síntomas pero que puede progresar clínicamente con el paso del tiempo a una forma más activa con necesidad de tratamiento. Representa un modelo factible para analizar la evolución clonal debido a su gran prevalencia, el fácil acceso de las muestras en comparación a otros tipos de cáncer, y su lenta evolución. Durante los últimos años, la incorporación de la secuenciación masiva a gran escala ha permitido a los investigadores caracterizar las mutaciones genéticas más recurrentes en la LLC. Los análisis de secuenciación han revelado también la gran heterogeneidad de diferentes clones tumorales en un mismo paciente (heterogeneidad intra-tumoral) que podría contribuir a la variabilidad en el curso clínico entre enfermos. Hoy en día, se conoce que la evolución clonal es clave en la recaída de los pacientes de LLC, ya que se puede producir la expansión de los clones tumorales con ventaja proliferativa y resistentes al tratamiento. Sin embargo, aún se desconocen los patrones de evolución clonal que conducen la progresión clínica de la LLC sin intervención del tratamiento.
Secuenciación masiva de exoma completo y una novedosa herramienta bioinformática
En el contexto del proyecto europeo NGS-PTL, la colaboración internacional establecida entre el grupo de investigación del Dr. Jesús María Hernández Rivas (Centro de Investigación del Cáncer, Salamanca) y el de la Dra. Sarka Pospisilova (Central European Institute of Technology, Brno) ha permitido publicar recientemente un estudio en Leukemia, una de las revistas más prestigiosas en el campo de la hematología, que tenía por objetivo evaluar la dinámica clonal en pacientes con LLC durante la evolución de la enfermedad sin intervención del tratamiento. Mediante secuenciación masiva, se analizó el exoma completo de 70 muestras tumorales de un total de 35 pacientes con LLC, ya que se evaluaron dos momentos de la enfermedad por cada enfermo. Cabe destacar que en este estudio se incluyeron desde pacientes que terminaban progresando clínicamente a otros casos que presentaban una enfermedad indolente con un seguimiento largo.
Hoy en día, resulta esencial la aplicación de herramientas bioinformáticas que ayuden a los investigadores a interpretar la gran cantidad de datos que arrojan las técnicas de secuenciación masiva. Así, para el análisis de los exomas se usó el algoritmo bioinformático Cancer Genome Interpreter, desarrollado por el grupo de la Dra. Nuria López-Bigas (Institución Catalana de Investigación y Estudios Avanzados, Barcelona). Como su propio nombre indica, esta herramienta informática ayudó a los investigadores a interpretar qué mutaciones genéticas podían “conducir” el curso de la enfermedad de los enfermos (mutaciones “drivers”).
Identificación de nuevas mutaciones que conducen la leucemia
Del total de 392 mutaciones somáticas detectadas, se identificaron 57 como mutaciones drivers localizadas en 35 genes diferentes. Entre estos genes, 11 habían sido previamente reportados como “drivers” en otros estudios siendo los más frecuentes SF3B1, NOTCH1, NFKBIE, TP53, BIRC3, RPS15… De manera interesante, el algoritmo utilizado predijo también otras mutaciones relevantes en la LLC, dato que se desconocía hasta la fecha. Entre ellas, destacan las mutaciones en los genes HDAC2, DHX9, GATA3 o IDH1, que habían sido descritas en otras neoplasias hematológicas.
Al analizar qué mutaciones podrían ser responsables de la evolución clonal de estos enfermos, se evaluaron los cambios clonales comparando los dos momentos secuenciados de cada enfermo. Cabe destacar que la mitad de las mutaciones “drivers” mostraron un cambio significativo en el porcentaje de células tumorales. Aunque la mayoría de los pacientes que terminaban progresando clínicamente presentaban evolución clonal, llama la atención que algunos enfermos que presentaban una enfermedad indolente de larga duración también tenían cambios clonales significativos a nivel genético. Por tanto, con este estudio se confirma que la evolución clonal se puede producir no sólo en enfermos que recaen, como se habían descrito previamente, sino también en enfermos que no hayan recibido ninguna línea de tratamiento, y no sólo en pacientes que progresen clínicamente o que presentan alteraciones genéticas de mal pronóstico.
Las mutaciones asociadas previamente a cursos clínicos más agresivos como las de TP53, BIRC3 o RPS15 sólo se detectaron en pacientes que progresaban clínicamente entre los dos momentos analizados. Por otra parte, dos pacientes con una enfermedad inactiva hasta el último seguimiento presentaban una mutación en genes relevantes en la LLC desde el momento del diagnóstico, revelando que la simple presencia de estas mutaciones no conduce a una progresión clínica inmediata. Será necesario cuantificar el impacto de otras mutaciones subclonales que puedan favorecer el desarrollo de una forma de LLC más activa con necesidad de tratamiento. Además, la generación de modelos experimentales permitirá evaluar el impacto funcional de las observaciones obtenidas en los estudios de secuenciación de LLC. En este sentido, la tecnología de edición genómico CRISPR/Cas9 está jugando un papel fundamental. También será esencial integrar los conocimientos genéticos en cohortes de pacientes más grandes con datos de epigenética o microambiente para tener una mayor comprensión de la evolución en la LLC con la esperanza de que los clínicos puedan actuar anticipándose al potencial evolutivo de los enfermos.
Referencia
Hernández-Sánchez M, et al. 2018. CLL cells cumulate genetic aberrations prior to the first therapy even in outwardly inactive disease phase. Leukemia. 2018. Doi: https://doi.org/10.1038/s41375-018-0255-1


