Almudena Avila-Fernandez 1,2 , Raquel Perez-Carro1,2 , Marta Corton 1,2 ,Carmen Ayuso 1,2.
1 Servicio de Genética, Instituto de Investigacion Sanitaria- Hospital Universitario Fundación Jiménez Díaz (IIS-FJD, UAM), Madrid, España.
2 Centro de Investigación Biomédica en Red de Enfermedades Raras (CIBERER), ISCIII, Madrid, España
La retinosis pigmentaria (RP, MIM 268000) es la distrofia de retina (DR) más común. Se presenta con una prevalencia de 1 en 4000 individuos, perteneciendo por ello al grupo de las enfermedades raras. La RP se caracteriza por la degeneración primaria de los fotorreceptores produciendo ceguera nocturna, pérdida del campo visual así como una disminución lenta y progresiva de la agudeza visual. La edad de inicio y la progresión de la enfermedad varían mucho de unos individuos a otros, incluso dentro de la misma familia. Además, la RP, al igual que el resto de las DR presenta una elevada heterogeneidad genética. Es una enfermedad monogénica que puede heredarse siguiendo todos los patrones de herencia mendeliana. Hasta la fecha se han descrito mutaciones asociadas a la RP en más de 70 genes. Aún así, éstas sólo explican el 50% de los casos. Esta heterogeneidad dificulta enormemente el manejo de los pacientes, especialmente la confirmación precisa de su diagnóstico y el consejo genético.
La rápida evolución de las técnicas de secuenciación masiva permite el uso del análisis del exoma completo (WES) como la estrategia más adecuada para la identificación de nuevos genes en enfermedades Mendelianas raras. Así, en los últimos años esta técnica ha permitido la identificación de decenas de nuevos genes asociados a patologías raras como las DR y el establecimiento de nuevas asociaciones genotipo-fenotipo.
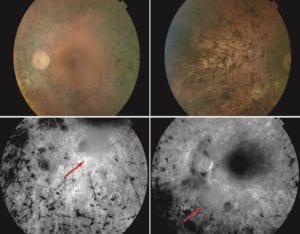
En el trabajo publicado en Human Molecular Genetics se reporta la identificación de un nuevo gen –ZNF408– asociado a RP en población española, mediante la secuenciación de exoma completo. Los pacientes con mutaciones en este gen presentan un fenotipo particular consistente en una RP con alteraciones vítreas.
Además del fenotipo clínico de los pacientes, los investigadores han descrito la localización de la proteína producto de este gen, a nivel subcelular y en los distintos tipos celulares de la retina, así como su posible función y el efecto de sus mutaciones en la retina. Tras este estudio, parece que ZNF408 tiene un papel importante en el desarrollo del ojo, cumpliendo funciones esenciales en el mantenimiento homeostático de la retina, así como en el desarrollo vascular. Las mutaciones en el gen ZNF408, asociado previamente a otra patología ocular en una familia holandesa, se vincula por primera vez a la RP, en familias de población española.
La identificación de este nuevo gen asociado a una clínica específica tiene una aplicabilidad clínica directa sobre los pacientes y sus familiares ya que el gen ZNF408 podrá incluirse en los paneles de diagnóstico genético para la RP. Dicha caracterización molecular permitirá proporcionar un pronóstico preciso y precoz de la evolución clínica de la enfermedad y un adecuado consejo genético a las familias. Además, el diagnostico genético de los pacientes hace que sea posible su futura inclusión de los mismos en ensayos clínicos basados en terapia génica con el fin de rescatar el daño producido en los fotorreceptores.
Referencia:
Avila-Fernandez A, Perez-Carro R, et al. Whole-exome sequencing reveals ZNF408 as a new gene associated with autosomal recessive retinitis pigmentosa with vitreal alterations. Hum Mol Genet. 2015 Apr 16. pii: ddv140
Fuentes:
http://www.fjd.es/es/sala-prensa/noticias/investigadores-fjd-identifican-dos-familias-espanolas-nuevo
http://www.ciberer.es/index.php?option=com_content&task=view&id=1376&Itemid=62
Bibliografía sobre la genética de la retinosis pigmentaria:
Hartong DT, et al. Retinitis pigmentosa. Lancet. 2006 Nov 18;368(9549):1795-809. Review.
Wright AF, et al. Photoreceptor degeneration: genetic and mechanistic dissection of a complex trait. Nat Rev Genet. 2010 Apr;11(4):273-84. doi: 10.1038/nrg2717
Berger W, et al. The molecular basis of human retinal and vitreoretinal diseases. Prog Retin Eye Res. 2010 Sep;29(5):335-75.doi: 10.1016/j.preteyeres.2010.03.004.
Audo I, et al. Development and application of a next-generation-sequencing (NGS) approach to detect known and novel gene defects underlying retinal diseases. Orphanet J Rare Dis. 2012 Jan 25;7:8. doi: 10.1186/1750-1172-7-8.
Webb TR, et al. Deep intronic mutation in OFD1, identified by targeted genomic next-generation sequencing, causes a severe form of X-linked retinitis pigmentosa (RP23). Hum Mol Genet. 2012 Aug 15;21(16):3647-54. doi: 10.1093/hmg/dds194.
Wang H, et al. Exome capture sequencing identifies a novel mutation in BBS4. Mol Vis. 2011;17:3529-40.
Daiger SP, et al. Targeted high-throughput DNA sequencing for gene discovery in retinitis pigmentosa. Adv Exp Med Biol. 2010;664:325-31. doi: 10.1007/978-1-4419-1399-9_37.
Nikopoulos K, et al. Next-generation sequencing of a 40 Mb linkage interval reveals TSPAN12 mutations in patients with familial exudative vitreoretinopathy. Am J Hum Genet. 2010 Feb 12;86(2):240-7. doi: 10.1016/j.ajhg.2009.12.016.
Peluso I, et al. The ADAMTS18 gene is responsible for autosomal recessive early onset severe retinal dystrophy. Orphanet J Rare Dis. 2013 Jan 28;8:16. doi: 10.1186/1750-1172-8-16
Khateb S, et al. Exome sequencing identifies a founder frameshift mutation in an alternative exon of USH1C as the cause of autosomal recessive retinitis pigmentosa with late-onset hearing loss. PLoS One. 2012;7(12):e51566.
Wang Y, et al. Exome sequencing identifies compound heterozygous mutations in CYP4V2 in a pedigree with retinitis pigmentosa. PLoS One. 2012;7(5):e33673.
Collin RW, et al. ZNF408 is mutated in familial exudative vitreoretinopathy and is crucial for the development of zebrafish retinal vasculature. Proc Natl Acad Sci U S A. 2013 Jun 11;110(24):9856-61. doi: 10.1073/pnas.1220864110.

