Amparo Tolosa, Genética Médica News

El sistema inmunitario de cada persona reacciona de forma diferente frente a un mismo estímulo. En algunas personas, la respuesta inmunitaria es insuficiente, lo que lleva a que sean más susceptibles a infecciones. En otras, por el contrario, el sistema inmunitario está sobreactivado y puede generar respuestas no necesarias, aumentando la predisposición a enfermedades autoinmunes como la artritis reumatoide.
¿Cómo se genera esta diversidad? Tanto factores genéticos como no genéticos influyen en la variabilidad que existe en la función o en el número de las células inmunitarias, así como en la concentración de moléculas mediadoras como las citoquinas. Sin embargo, debido a las complejas interacciones entre unos y otros, hasta el momento no se había abordado de forma sistemática el efecto de la variación genética humana o los otros aspectos que participan, ni tampoco sus relaciones sobre la respuesta inmune.
Creado hace tres años, el Proyecto de Genómica Funcional Humana (HFGP, en sus siglas en inglés) es una iniciativa que pretende utilizar las herramientas más avanzadas de la biología molecular y análisis bioinformático para identificar las consecuencias de la variación genética en el ADN humano y su interacción con el microbioma sobre los procesos fisiológicos del cuerpo humano, con especial interés en el sistema inmunitario.
“El argumento subyacente del HFGP es que el sistema inmune es una diana perfecta para estudiar la variación humana y la intersección de los genes y el ambiente,” señala Ramnik Xavier, jefe de la unidad de Gastroenterología del Massachussets General Hospital y miembro del Broad Institute of MIT and Harvard y uno de los directores del proyecto.
Los primeros trabajos del HFGP se han publicado este mes en varias revistas del grupo Cell y marcan el inicio de una mejora significativa en el conocimiento de cómo los factores genéticos y los ambientales contribuyen a generar las respuestas del sistema inmunitario en humanos y cómo la variabilidad genética afecta a la salud humana.
Los tres primeros artículos abordan en una misma cohorte de 500 personas el impacto de los factores ambientales, genéticos y del microbioma sobre la producción de las citoquinas, principales moléculas señalizadoras del sistema inmune. “Sabemos que algunas personas son más susceptibles a las infecciones que otras; algunas desarrollan enfermedades autoinmunes mientras que la mayoría no lo hacen,” manifiesta Ramnik. “En estos estudios queríamos ver cómo los genes afectan al sistema inmunitario, cómo los factores ambientales afectan a la susceptibilidad y en esta investigación si y cómo el microbioma intestinal influye en la respuesta del sistema inmunitario a diferentes patógenos.”
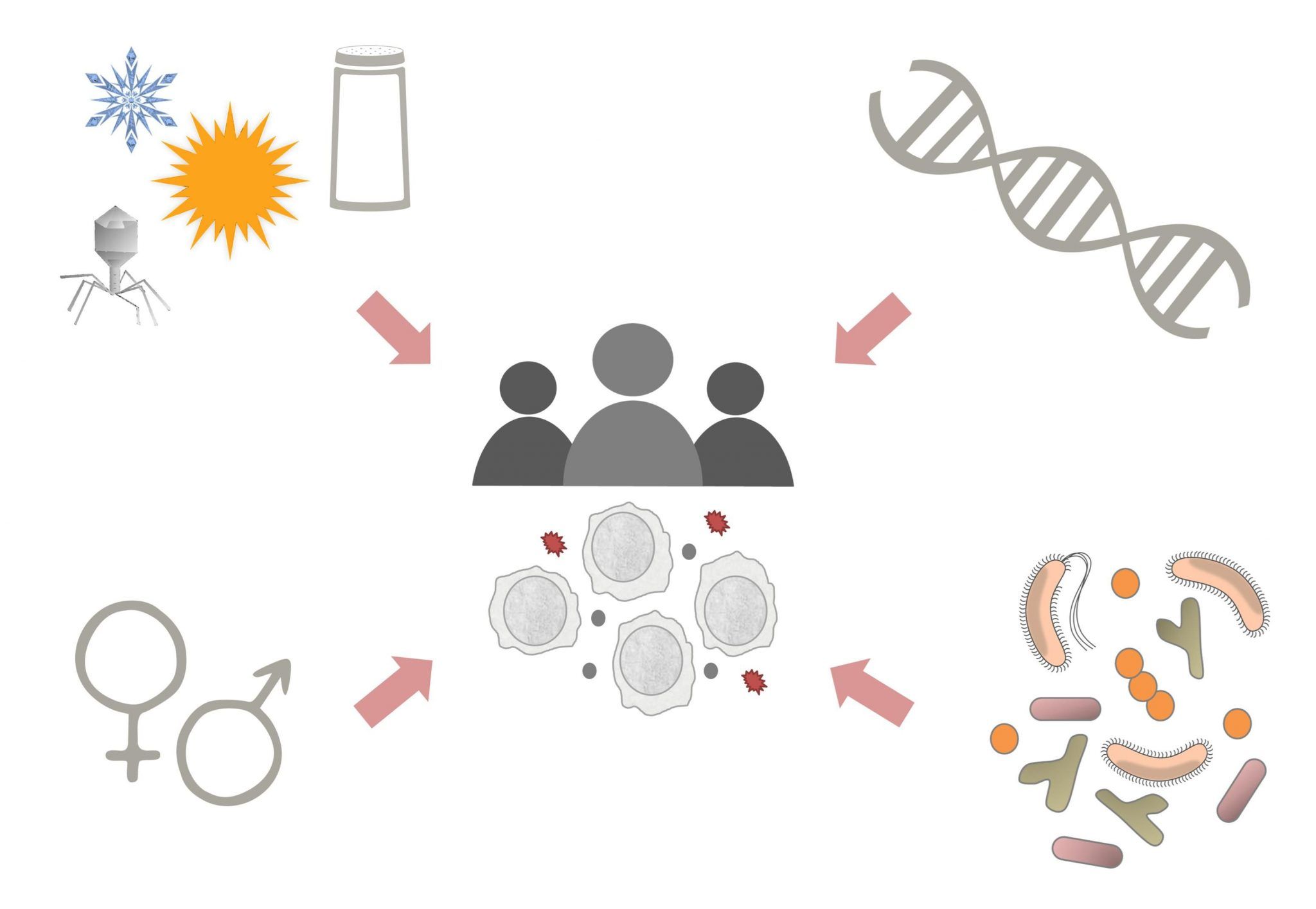
En el primer artículo, Rob ter Horst y colaboradores analizan el efecto de los factores ambientales y factores no genéticos propios del hospedador, como la edad o el sexo, en la producción de citoquinas. Los resultados del trabajo muestran un efecto estacional importante en la producción de citoquinas, lo que podría explicar en parte el hecho de que las enfermedades inflamatorias se ven afectadas por la estación del año. Además encuentran un importante efecto de la edad y sexo de la persona sobre la producción de citoquinas. En el caso de la edad, observaron que aunque en general el sistema inmunitario no se deteriora con el envejecimiento, componentes específicos del mismo, sí se ven afectados. Respecto a las diferencias encontradas en la producción de citoquinas entre hombres y mujeres, los investigadores señalan que podrían ser debidas a las citoquinas que se producen por las células del tejido graso, cuya proporción es muy diferente entre ambos sexos.
En el segundo artículo Li y colaboradores analizan el efecto de la variación genética sobre la producción de citoquinas en tres sistemas celulares distintos, tras el estímulo con diferentes patógenos. En este caso, los investigadores demuestran que los factores genéticos tienen un peso importante en la capacidad de producción de citoquinas. Entre los genes reguladores de las citoquinas, el equipo reconoce dos grupos formados por aquellos que intervienen en la respuesta innata y aquellos necesarios para el procesamiento de los antígenos en el retículo endoplásmático. Además, los investigadores detectaron un patrón importante en la respuesta inmunitaria: la capacidad para producir citoquinas dependía del tipo de estímulo, si era de origen bacteriano, fúngico o viral.
En un tercer artículo Schirmer y colaboradores demuestran el impacto de la variación del microbioma, el conjunto de microorganismos residentes en nuestro cuerpo, sobre la producción de citoquinas. En este caso, los investigadores encuentran que en respuesta a patógenos concretos, algunas bacterias de la flora intestinal influyen en la producción de ciertas citoquinas. A través de diferentes experimentos, el equipo plantea que la variación en la microbiota intestinal modifica la producción de metabolitos que educan o influyen en las células inmunitarias, y esto es lo que lleva a diferentes resultados cuando estás células son expuestas a infecciones. Si bien el peso del microbioma encontrado es menor al de los factores genéticos (sólo explica un 10% de la variabilidad frente a los valores de 25-50% de los factores genéticos sobre algunas citoquinas), los investigadores resaltan su importancia y recuerdan que recientes estudios muestran que los factores genéticos también influyen en la composición de la microbiota. “Nuestro estudio, que muestra que el microbioma puede interaccionar de forma específica de patógeno tiene potencial para la inmunoterapia,” señala Ramnik Xavier. “Por ejemplo, la dieta, los antibióticos o los trasplantes de comunidades microbianas residentes en el intestino podrían influir potencialmente en la producción de citoquinas.”
La aportación de los tres artículos sobre los factores que influyen en la producción de citoquinas tiene relevancia, no sólo en este aspecto concreto de la generación de respuestas inmunitarias, sino también porque proporciona un marco de trabajo para futuros estudios que evalúen otros procesos biológicos.
En paralelo a los trabajos mencionados, Raúl Aguirre Gamboa y colaboradores estiman cómo influyen los factores genéticos y ambientales en las poblaciones de células inmunitarias y en la concentración de inmunoglobinas. Los resultados de su trabajo muestran que las variaciones en los linfocitos T están más influidas por factores genéticos, mientras que la variabilidad en el número de linfocitos B se debe principalmente a factores no genéticos, como la estación del año o el sexo.
Por último, Marije Oosting y colaboradores analizan la arquitectura funcional y genómica de la respuesta inmunitaria frente a un tipo de infección concreta, la inducida por la bacteria Borrelia burgdorferi, principal agente responsable de la enfermedad de Lyme (transmitida por las garrapatas). Los resultados del equipo señalan, una vez más, la influencia de factores genéticos y no genéticos sobre las respuestas generadas en monocitos y linfocitos T y destacan un papel importante de la glucólisis mediada por HIF-1α en la respuesta a la infección por Borrelia.
El Proyecto de Genómica Funcional Humana continúa. Para las siguientes fases, los investigadores ya preparan estudios similares a los ya publicados en los que incluirán otras poblaciones humanas y se enfocarán en enfermedades específicas. Por ejemplo, estudiarán el microbioma en niños para ver si su composición puede influir en el riesgo a las enfermedades autoinmunes, especialmente la diabetes tipo I. “Comprendiendo cómo todos estos mecanismos complejos –genética, microbioma y ambiente –dirigen las variaciones en la respuesta inmunitaria, podríamos ser capaces de identificar factores responsables de las susceptibilidades individuales de los pacientes, así como terapias dirigidas mejores,” concluye Ramnik.
Referencias:
ter Host R, et al. Host and environmental factors influencing individual human cytokine responses. Cell. 2016. DOI: 10.1016/j.cell.2016.10.018
Li Y, et al. A functional genomics approach to understand variation in cytokine production in humans. Cell. 2016. DOI: 10.1016/j.cell.2016.10.017
Schirmer M, et al. Linking the gut microbiome to inflammatory cytokine production capacity. Cell. 2016. DOI: 10.1016/j.cell.2016.10.020
Oosting M, et al. Functional and genomic architecture of Borrelia burgdorferi-induced cytokine responses in humans. Cell Host & Microbe. 2016. DOI: 10.1016/j.chom.2016.10.006
Aguirre-Gamboa R, et al. Differential effects of environmental and genetic factors on T and B cell immune traits. Cell Reports. 2016. DOI: 10.1016/j.celrep.2016.10.053
Pappalardo JL y Hafler DA. The Human Functional Genomics Project: Understanding Generation of Diversity. Cell. 2016. Doi: 10.1016/j.cell.2016.10.040
Fuentes:
Deciphering the drivers of immune system variability. https://www.broadinstitute.org/blog/deciphering-drivers-immune-system-variability
Study links intestinal microbial population to production of inflammatory proteins. http://www.massgeneral.org/about/pressrelease.aspx?id=2009
Why every immune system is different. http://www.alphagalileo.org/ViewItem.aspx?ItemId=169529&CultureCode=en

