Las variantes genéticas causantes de enfermedad en los pacientes con cardiomiopatías determinan qué procesos biológicos concretos llevan a la enfermedad en cada paciente, revela un estudio internacional publicado recientemente en Science, destacando la importancia de la genética en cardiomiopatías. Los resultados ofrecen oportunidades para el desarrollo de tratamientos personalizados.
El desarrollo de la cardiogenética y la identificación de factores genéticos que intervienen en las enfermedades vasculares han abierto nuevas oportunidades de diagnóstico y tratamiento para los diferentes trastornos que afectan al corazón y los vasos sanguíneos.
Un ejemplo del potencial de la genética en el ámbito de la cardiología son las cardiomiopatías, condiciones que afectan a la estructura o funcionamiento del corazón. En los últimos años se han identificado mutaciones en múltiples genes relacionadas con la aparición de cardiomiopatías, pero hasta el momento no se había analizado, desde una perspectiva de medicina de precisión, cómo impactaban las diferentes variantes en el desarrollo de la enfermedad, para buscar soluciones de tratamiento adaptadas a cada paciente.

Un reciente trabajo internacional, donde han participado, entre otros, el Brigham and Woman´s Hospital de Boston, la Universidad de Alberta de Canadá y el Imperial College de Londres, muestra cómo diferentes variantes genéticas patogénicas llevan a la misma entidad clínica de cardiomiopatía tanto por procesos compartidos como diferentes.
Para entender cómo actuaba cada variante, a qué rutas biológicas afectaba, y qué células estaban implicadas, los investigadores han analizado la expresión génica de más de 880 000 células del corazón individuales, obtenidas de 61 corazones de pacientes (portadores de mutaciones conocidas) y 18 donantes sanos.
Tras reconstruir célula a célula lo que ocurría en cada corazón, los investigadores han obtenido una imagen más clara del impacto de cada mutación en la función cardiaca y desarrollo de la enfermedad. “Solo este nivel de resolución nos permite ver que las cardiomiopatías no activan de forma uniforme las mismas rutas patológicas”, señala Christine Seidman, profesora de Medicina y Genética en la Escuela de Medicina de Harvard y cardióloga en el Hospital Brigham. “Más bien diferentes mutaciones producen respuestas específicas, y algunas compartidas que llevan al fallo del corazón”, señala la investigadora.
Los resultados muestran a las cardiomiopatías como entidades heterogéneas a nivel molecular y biológico y apuntan a características que podrían ser utilizadas para personalizar el tratamiento. Especialmente, si se considera que ciertas mutaciones actúan sobre rutas moleculares concretas.
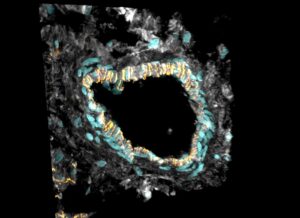
Dentro de los resultados obtenidos, los investigadores destacan, por ejemplo, que la fibrosis o crecimiento anormal de tejido conectivo en la cardiomiopatía dilatada no va acompañada de aumento en el número de fibroblastos, sino de un aumento en la actividad de los fibroblastos, que producen más matriz extracelular. Además, esta característica, se veía incrementada en pacientes con mutaciones en el gen RBM20.
Otro resultado son los cambios en la comunicación entre células observados en ciertas rutas de señalización, como el aumento en señalización a través de endotelina en los tejidos con mutaciones en LMNA o de factor de necrosis tumoral en los corazones con mutaciones en el gen PKP2.
Los datos obtenidos por los investigadores representan un atlas celular de cardiomiopatías con potencial para nuevas investigaciones. Para favorecer la utilización de la información observada en la búsqueda y desarrollo de tratamientos más precisos para los pacientes con cardiomiopatías los investigadores han hecho públicos los datos entre la comunidad científica.
Entre los objetivos a corto plazo del equipo de investigadores está repetir el estudio en pacientes durante las primeras fases de la enfermedad para detectar biomarcadadores. “Tenemos ganas de ver qué cambios descubrimos en estadios más tempranos de la enfermedad, basados por ejemplo en biopsias de endomiocardio”, ha señalado Daniel Reichart, primer autor del trabajo e Investigador de la Escuela de Medicina de Harvard, el Brigham and Women´s Hospital y la Universidad de Munich.
Referencia: Reichart D, et al. Pathogenic variants damage cell composition and single cell transcription in cardiomyopathies. Science. 2022. DOI: https://doi.org/10.1126/science.abo1984
Fuente: How pathogenic gene variants lead to heart failure. https://www.mdc-berlin.de/news/press/how-pathogenic-gene-variants-lead-heart-failure
Si te ha gustado esta noticia y quieres aprender más sobre Genética en Medicina, te interesan nuestros cursos y formación universitaria, como el “Máster de Medicina de Precisión y Genética Clínica”.




