Rubén Megía González, Genotipia
Tradicionalmente, se ha pensado que el material genético transmitido por los padres es el único factor hereditario que determina el estado de salud de la descendencia. Hoy en día se sabe que la herencia es mucho más compleja. Es cierto que la mayoría de la variación fenotípica en una población puede explicarse gracias a la herencia genética. Sin embargo, actualmente conocemos otras formas de herencia que influyen en la salud de la descendencia y que no implican de forma directa a la secuencia de ADN. Es el caso de la herencia epigenética.
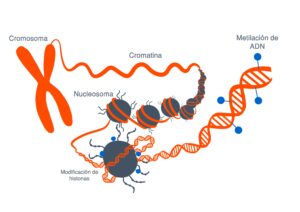
La herencia epigenética es aquella mediada por mecanismos epigenéticos, como la modificación de histonas, el ARN no codificante o la metilación del ADN. Se ha comprobado que estos mecanismos pueden ser alterados por diferentes factores ambientales, como el consumo de ciertas sustancias, el estrés o la dieta. No obstante, todavía se desconoce cómo algunos de estos factores ambientales intervienen en la transmisión a la descendencia de diferentes aspectos de la salud.
Dos recientes estudios han identificado algunos de los factores ambientales que influyen en la herencia epigenética. El primero de ellos, publicado en la revista Developmental Cell el pasado 8 de marzo, ha determinado que la dieta paterna produce cambios epigenéticos en las proteínas espermáticas que pueden afectar al desarrollo de la descendencia. El segundo, publicado en PNAS el pasado 23 de marzo, ha encontrado que ciertos factores, como la edad materna o el consumo de alcohol, pueden alterar la impronta genética de los ovocitos maternos antes de la concepción.
La dieta paterna influye en la salud de la descendencia
El primero de los estudios, publicado el pasado 8 de marzo, es resultado de 15 años de trabajo de un grupo de investigadores de la Universidad McGill. Los autores han observado, en modelos de ratón, que la falta de folato en la dieta paterna produce ciertos cambios epigenéticos en los espermatozoides. El equipo ha determinado que estos cambios influyen en la salud de la descendencia.
El folato es un tipo de vitamina B que se encuentra, de forma natural, en muchos alimentos, como las legumbres, los frutos secos o los cereales. Esta vitamina es importante para el correcto funcionamiento del organismo, pues está estrechamente relacionada con la síntesis de ácidos nucleicos y la división celular.
En el estudio, los autores alimentaron a ratones macho con una dieta deficiente en folato y analizaron la metilación de las histonas en sus espermatozoides. Los investigadores determinaron que, en ratones alimentados con una dieta carente de folato presentan alteraciones en la metilación de la lisina 4 en la histona H3 (H3K4me3) en ciertos genes relacionados con el desarrollo.
Para comprobar si los cambios epigenéticos causados por la carencia de folato en los padres provocan alteraciones en la descendencia, el equipo fecundó óvulos de hembras sanas con espermatozoides de ratones alimentados con una dieta carente de folato. Los autores determinaron que algunas de las alteraciones epigenéticas en H3K4me3 presentes en los espermatozoides prevalecían en el embrión antes de la implantación e incluso se mantenían durante el desarrollo. Además, el equipo asoció estos cambios epigenéticos con diferentes defectos esqueléticos en la descendencia.
“El gran avance de este estudio es que ha identificado un medio no basado en el ADN mediante el cual los espermatozoides recuerdan el entorno del padre y transmiten esa información al embrión”, explica la Dra. Sarah Kimmins, autora del estudio e investigadora en el Departamento de Farmacología y Terapéutica de la Facultad de Medicina de La Universidad McGill. Tal y como explica la Dra. Kimmins, este estudio sugiere que la clave para comprender y prevenir ciertas enfermedades puede involucrar cambios epigenéticos en las proteínas de los espermatozoides paternos.
El siguiente paso de los autores será determinar si los cambios heredables en las histonas producidos por la ausencia de folato pueden ser revertidos. “Tenemos un emocionante trabajo nuevo que sugiere que esto es así”, indica la Dra. Kimmins.
La edad y el consumo de alcohol antes del embarazo, dos factores que influyen en la impronta genética de la descendencia
Por otra parte, el segundo trabajo, realizado por investigadores del Instituto Van Andel y de la Universidad Stellenbosch, se ha centrado en el gen nc886, uno de los genes improntados que se transmiten de madres a hijos. Los autores han estudiado este gen porque es el único conocido que presenta una impronta genética polimórfica en la población.
La impronta genética es un proceso biológico que “etiqueta” químicamente ciertos genes durante la formación de los gametos. Estas marcas epigenéticas tienen un papel crucial en la expresión de estos genes en la descendencia, pues regulan su actividad.
Para este estudio, los autores utilizaron datos del genoma de más de 1.100 parejas de madres e hijos del sur del continente africano. En ellos, estudiaron la impronta genética del gen nc886 y analizaron cómo es influida por diferentes factores ambientales maternos, como el consumo del alcohol o de tabaco antes del embarazo. Los resultados mostraron que la impronta de nc886 está influida por la edad de la madre y su consumo de alcohol un año antes de la concepción, pero no por el consumo de tabaco.
Los investigadores no han detallado más consecuencias de los cambios en la impronta materna influidos por la edad y el consumo de tabaco. “Si bien el resultado del cambio no está claro, nuestros hallazgos nos brindan una visión valiosa de cómo los factores ambientales afectan la regulación genética a través de la epigenética y la impronta.”, explica el Dr. Peter A. Jones, director científico del Instituto Van Andel y autor del estudio.
Estudios anteriores del equipo del Dr. Jones habían demostrado que los fallos de impronta del gen nc886 están asociados con una mayor masa corporal en niños de 5 años. Otros estudios han relacionado los fallos en la impronta de este gen con una mayor supervivencia en pacientes con leucemia mieloide aguda y con una baja respuesta a ciertos fármacos para la diabetes.
Un gran paso para la investigación de la herencia epigenética
Ambos estudios suponen una mejora en el conocimiento de los factores ambientales que influyen en la herencia epigenética, a la vez que abren las puertas a nuevas investigaciones relacionadas con este tipo de herencia. “Una mejor comprensión de estos complejos procesos aumenta nuestra comprensión de la salud y la enfermedad y, algún día, puede ser la base de nuevas medidas de prevención de enfermedades «, explica el Dr. Jones.
Artículos originales:
Carpenter BL, et al. Oocyte age and preconceptual alcohol use are highly correlated with epigenetic imprinting of a noncoding RNA (nc886). Proc Natl Acad Sci U S A. 2021 Mar 23;118(12):e2026580118. doi: 10.1073/pnas.2026580118
Lismer A, et al. Histone H3 lysine 4 trimethylation in sperm is transmitted to the embryo and associated with diet-induced phenotypes in the offspring. Dev Cell. 2021 Mar 8;56(5):671-686.e6. doi: 10.1016/j.devcel.2021.01.014
Fuentes:
Study explores how environmental exposures before conception may impact fetal development. Van Andel Institute: https://www.vai.org/jones-pnas-nc886/
How sperm remember. McGill University:https://www.mcgill.ca/newsroom/channels/news/how-sperm-remember-329649
Si te ha gustado esta noticia y quieres aprender más sobre Genética en Medicina, te interesan nuestros cursos y formación universitaria, así como nuestro canal audiovisual, Genotipia TV.



