Irene González1 y Rubén Artero2,3,4
1 Facultad de Ciencias Biológicas, Universidad de Valencia
2 Grupo de Genómica Traslacional, INCLIVA Instituto de Investigación Sanitaria
3 Departamento de Genética y Estructura de Recerca Interdisciplinar en Biotecnología y Biomedicina (ERI BIOTECMED), Universidad de Valencia
4 Unidad mixta INCLIVA-CIPF
Los oligonucleótidos antisentido (ASOs) son pequeños fragmentos de ácidos nucleicos de entre 8 y 20 nucleótidos, diseñados para silenciar RNAs mensajeros o RNAs no codificantes con un fin terapéutico (Fig.1). Actualmente se estudia la posibilidad de tratamientos basados en oligonucleótidos antisentido para diferentes enfermedades, pero en algunos casos se ha encontrado que estos producen toxicidad debido a su acumulación en el riñón, lo que parece estar relacionado con la química de los ASOs y la carga renal de estos fármacos. La nefrotoxicidad se ha podido observar en ensayos clínicos incluso en sujetos sanos, por lo que es necesario buscar una forma de que se pueda conseguir la efectividad de los ASOs sin que se produzca acumulación renal.
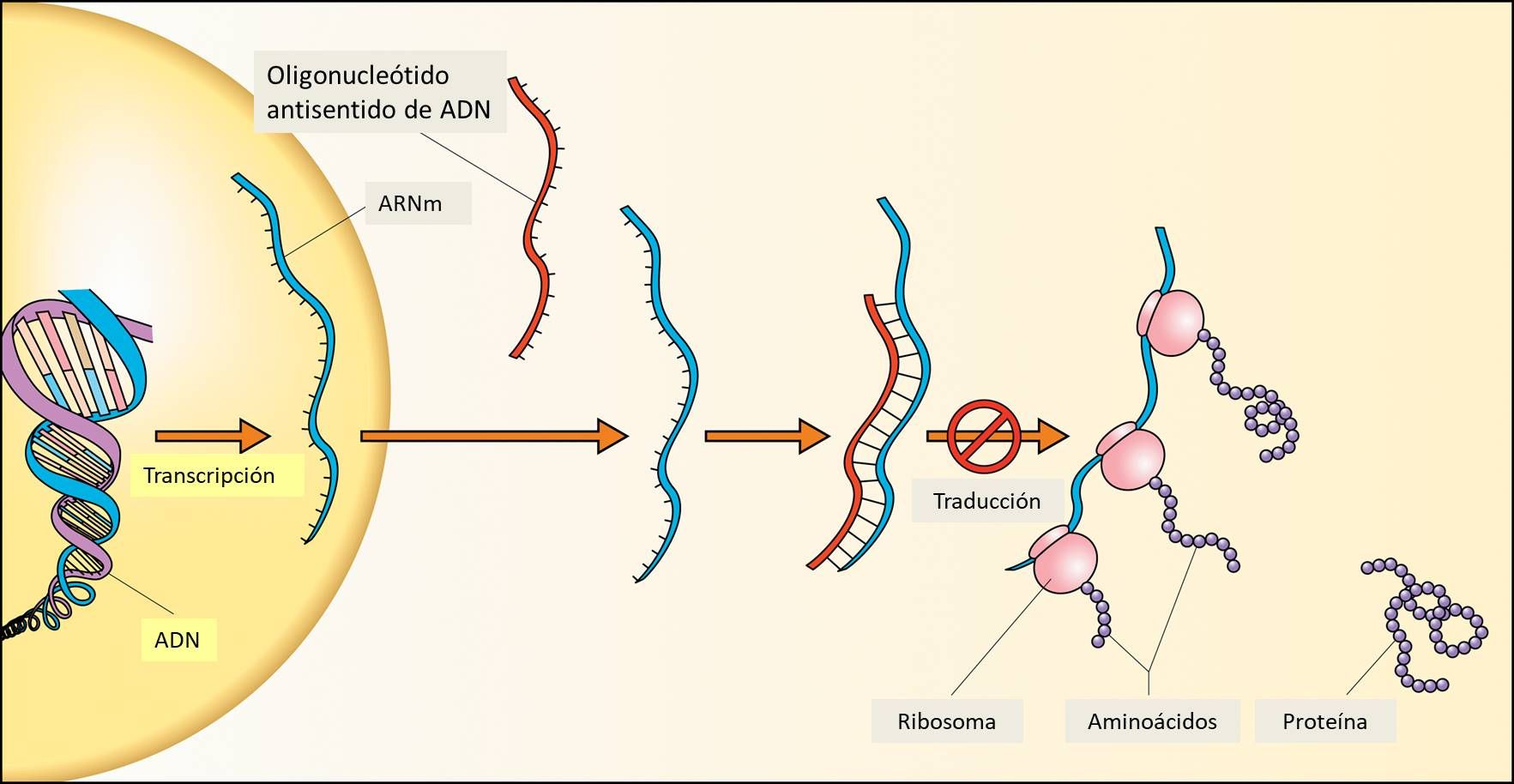
Un grupo de investigadores japoneses, especializados en enfermedades hepáticas, ha propuesto una nueva estrategia en el diseño de oligonucleótidos que cambia su farmacocinética, ya que la nefrotoxicidad está relacionada con la dosis administrada. Esta estrategia consiste en conjugar determinadas moléculas a los ASOs que sean capaces de disminuir su acumulación renal, sin afectar a su capacidad de silenciamiento génico, por lo que se propusieron como posibles ligandos el colesterol y la N-acetilgalactosamina (GalNAc).
Previamente a este estudio, se había comprobado por otros grupos investigadores que la modificación internucleotídica de los ASOs con fosforotioato (PS) incrementaba notablemente su actuación en el riñón, ya que estos oligonucleótidos interactuaban más fuertemente con proteínas del suero y eran absorbidos por los hepatocitos a través de los receptores de estabilina; mientras que en el caso de la conjugación de ASOs a colesterol, estos interactúan tanto con proteínas séricas como con lipoproteínas, permitiendo así su entrada en el hepatocito tanto por vías mediadas por receptores como por no mediadas por estos. Además, los ASOs conjugados a colesterol presentan una vida media en sangre superior, lo que puede ayudar a reducir la cantidad que se acumula en los riñones. En este estudio, se tomó como diana terapéutica el mRNA de la apolipoproteína B (apo B), buscando así una diana terapéutica para un tipo de hipercolesterolemia familiar. La tendencia de los ASOs conjugados a colesterol es a acumularse en las células no parenquimatosas (NPC) sobre los hepatocitos, donde su acción es menor, por lo que había que buscar que estos oligonucleótidos fuesen más específicos con respecto a sus células diana, los hepatocitos. Por ello, se planteó como segundo ligando GalNac, ya que actúa como ligando específico para el receptor de la asialoglicoproteína (ASGPR), una proteína que se expresa en los hepatocitos, impidiendo así que los ASOs se acumulasen en otras células.

A la vista de que estos dos ligandos podrían resolver el problema de la nefrotoxicidad ligada a ASOs, por una parte aumentando el tiempo que estos se encuentran en la circulación sanguínea, en el caso del colesterol, y por otra aumentando su especificidad por las células hepáticas, en el caso de GalNAc, se diseñó una serie de ASOs híbridos que presentaban conjugación tanto a colesterol como a GalNAc, obteniendo finalmente 4 ASOs diferentes (No conjugado, Conjugado a GalNAc (5GN) y dos dobles conjugados (5GN-3Chol/5Chol-5GN, en este último caso los ligandos estaban unidos por un conector de trietilenglicol). En todos los casos estas moléculas se diseñaron contra el mRNA de la apo B, como diana terapéutica para una variante de hipercolesterolemia familiar. Previamente al estudio, se comprobó que la conjugación directa a colesterol en el extremo 3’ ralentizaba la liberación metabólica del ASO en el tejido diana, por lo que en estas moléculas se utilizó un espaciador de 4 nucleótidos entre el extremo del ASO y el colesterol. Este cambio permitió ver que no había diferencias entre ASOs conjugados a colesterol y ASOs no conjugados ni en el tiempo de liberación ni en el silenciamiento génico que producían.
Tras la administración de estos diferentes ASOs híbridos en ratones machos de la cepa C57BL/6J, se comprobó que la doble conjugación con colesterol y GalNAc tenía un mayor efecto silenciador que la conjugación únicamente con colesterol y su acumulación renal era menor (Fig. 2A). En cuanto a los ASOs no conjugados, su acumulación en los hepatocitos (células diana) era similar a la de los ASOs conjugados, pero su efecto silenciador era mucho menor y menos específico en éstas células. Sin embargo, cuando se medía la acumulación renal (% dosis), la acumulación del ASO doblemente conjugado era prácticamente indetectable, mientras que en el caso del ASO no conjugado, esta acumulación era cincuenta veces mayor.
A la vista de estos resultados, la doble conjugación de los ASOs con colesterol y GalNAc supone una buena solución al problema de la acumulación renal en diferentes tratamientos basados en estas moléculas, a la vez que puede ayudar en diversos estudios que se han visto paralizados por la aparición de nefrotoxicidad. Sin embargo, como concluyen los investigadores, es necesario testar esta nueva estrategia en modelos preclínicos que permitan observar los efectos en el riñón de forma más detallada.
Investigación original: Wada F, et al. Cholesterol-GalNAc Dual Conjugation Strategy for Reducing Renal Distribution of Antisense Oligonucleotides. Nucleic Acid Ther. 2018 Jan; 28 (1): 50-57. doi: http://dx.doi.org/10.1089/nat.2017.0698
Referencia: Robinson, R. RNAi Therapeutics: How Likely, How Soon?. PLoS Biol, 2004 Jan; 2(1): e28. doi:10.1371/journal.pbio.0020028

