Investigadores de la Universidad de Harvard y el Instituto Broad analizan en un reciente estudio, en el que emplean organoides cerebrales, cómo distintas mutaciones en genes relacionados con el trastorno del espectro autista dan lugar a defectos similares en el neurodesarrollo.
Conocer la causa genética de una condición es un primer paso hacia comprender los mecanismos que intervienen en ella, y con ello, identificar dianas de acción terapéutica.
En los últimos años, diferentes estudios han revelado a los trastornos del espectro autista como un desorden del desarrollo complejo y heterogéneo que puede ser causado por mutaciones en diferentes genes. Así, se han identificado más de 100 genes cuya alteración, normalmente mutaciones de novo en heterocigosis (en una de las dos copias del gen afectado), está asociada al autismo.
La función individual de estos genes se conoce en muchos casos. No obstante, no está claro cómo su alteración durante el desarrollo embrionario puede derivar en el abanico de síntomas que muestran las personas con trastorno de espectro autista. Ni cómo influye el perfil genético de cada persona en la manifestación de este trastorno psiquiátrico. Investigadores de la Universidad de Harvard y el Instituto Broad aportan nuevas claves a estas preguntas en un reciente trabajo publicado en Nature.
Como modelo de estudio los investigadores han utilizado organoides cerebrales, un sistema celular tridimensional que reproduce, en laboratorio, y hasta cierto punto, el desarrollo del cerebro, en este caso la corteza cerebral humana. La obtención de organoides parte de cultivos de células madre pluripotentes inducidas, que pueden obtenerse de pacientes y modificarse mediante técnicas de edición del genoma como CRISPR para incluir mutaciones concretas.
Los investigadores generaron organoides cerebrales con características genéticas concretas para estudiar dos cuestiones. Por una parte, el equipo quería saber el efecto de la alteración de tres genes de riesgo en el desarrollo cerebral. Por otra, los investigadores buscaban conocer cómo influye el perfil genético de cada paciente en los mecanismos patológicos.
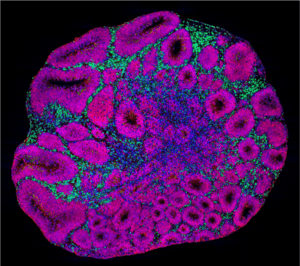
Fallos en la sincronización del desarrollo de los diferentes tipos celulares
Como prueba de concepto, los investigadores eligieron tres genes de riesgo para el autismo: SUV420H1, ARID1B y CHD8. Para determinar el efecto de las mutaciones en estos genes en el desarrollo neuronal, los investigadores obtuvieron organoides cuyas células tenían una copia alterada de SUV420H1, ARID1B o CHD8 y analizaron su progreso en cultivo en las siguientes semanas.
A partir de diferentes aproximaciones ómicas que analizaron la expresión, la regulación génica y el proteoma de las diferentes células y poblaciones de los organoides, los investigadores encontraron que la alteración de SUV420H1, ARID1B o CHD8 deriva en un retraso o una aceleración en el desarrollo de ciertos tipos de neuronas. La alteración de SUV420H1 o ARID1B induce una maduración acelerada y expansión prematura de las neuronas inhibidoras gabaérgicas, así como un desarrollo no sincronizado de las neuronas de proyección. La alteración de CHD8 en heterocigosis induce también una aceleración en el desarrollo de la población de células gabaérgicas y aumenta su proporción en los organoides.
Los cambios observados pueden derivar, en el contexto del desarrollo cerebral humano, en alteraciones en las conexiones nerviosas. “La corteza cerebral se genera de una forma muy orquestada: cada tipo de neurona aparece en un momento específico y empiezan a conectar muy tempranamente”, destaca Martina Pigoni, coautora del trabajo y antigua investigadora postdoctoral en el grupo de la Universidad de Harvard que ha dirigido el proyecto. “Si tienes algunas células que se forman demasiado pronto o demasiado tarde en comparación a cuando se supone que tienen que hacerlo se podría cambiar la forma en la que se conectan los circuitos”, señala la investigadora.
Los fallos en la sincronización del desarrollo nervioso que se producen cuando SUV420H1, ARID1B o CHD8 están alterados no se originan exactamente igual. Los cambios de expresión que se observan en cada uno de los tres tipos de organoides sugiere que, aunque el efecto final es compartido a nivel de rutas de proteínas implicadas, la alteración de cada gen actúa sobre diferentes conjuntos de genes.
El perfil genético de cada persona también influye
Además de investigar el efecto de cada mutación sobre el desarrollo neuronal, los investigadores generaron organoides de células de diferentes donantes y estudiaron cómo influye su perfil genómico diferente en la manifestación de los defectos causados por cada gene.
En general, el efecto de las mutaciones sobre la diferenciación neuronal se mantenía, aunque con diferencias en cuanto a cada perfil genómico. Este resultado es muy interesante ya que muchas mutaciones relacionadas con el trastorno del espectro autista derivan en diferente manifestación clínica en las personas portadoras. Así, estudios futuros deberán abordar no solo el impacto de cada mutación relacionada con el autismo sino también el efecto modulador del resto del genoma.
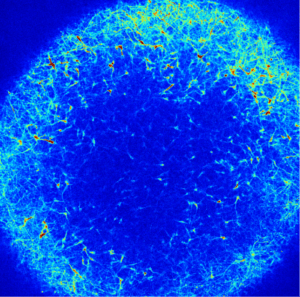
Relevancia terapéutica
Los resultados obtenidos para los diferentes organoides cerebrales sugieren que los síntomas clínicos derivan de procesos compartidos relacionados con la diferenciación celular y el establecimiento de conexiones entre circuitos nerviosos.
“Nuestros datos muestran que múltiples mutaciones relacionadas con la enfermedad convergen de hecho en efectos sobre las mismas células y procesos del desarrollo, pero a través de mecanismos diferentes”, señala Paola Arlotta, profesora de Biología Regenerativa y Células Madre en la Universidad de Harvard e investigadora en el Centro Stanley de Investigación Psiquiátrica en el Instituto Broad, así como una de los directores del trabajo. “Estos resultados impulsan la investigación futura de aproximaciones terapéuticas dirigidas a modular propiedades de los circuitos disfuncionales compartidas, así como rutas moleculares compartidas”, concluyen los investigadores en el estudio.
Referencia: Paulsen, B., Velasco, S., Kedaigle, A.J. et al. Autism genes converge on asynchronous development of shared neuron classes. Nature 602, 268–273 (2022). https://doi.org/10.1038/s41586-021-04358-6
Fuente: Different autism risk genes, same effects on brain development. https://hscrb.harvard.edu/news/autism-risk-genes-brain-development-organoids/
Si te ha gustado esta noticia y quieres aprender más sobre Genética en Medicina, te interesan nuestros cursos y formación universitaria, como el “Máster de Medicina de Precisión y Genética Clínica”.




