Amparo Tolosa, Genotipia

Genotipia, Rosario García.
Investigadores del Instituto Broad del MIT y la Universidad de Harvard han desarrollado una nueva tecnología de edición del genoma que combina elementos del sistema CRISPR-Cas9 con una transcriptasa reversa para introducir modificaciones en células humanas con precisión y eficacia.
El sistema, denominado prime editing, mejora algunas de las características de los métodos de edición previos y destaca en cuanto a la versatilidad que ofrece. Además, los investigadores estiman tiene el potencial de utilizarse en cerca del 90% de las variantes genéticas humanas que causan patologías, lo que supone una ampliación considerable respecto a las herramientas disponibles en la actualidad. “Una de las mayores aspiraciones en ciencias de la vida es la capacidad para realizar con precisión cualquier cambio en cualquier posición del genoma”, señala David Liu, director del Instituto Merkin de Tecnologías Transformativas en Cuidado de la Salud del Instituto Broad del MIT y la Universidad de Harvard y director del trabajo. “No conocemos ninguna otra tecnología de edición del genoma en células de mamífero que ofrezca este nivel de versatilidad y precisión con tan pocos productos”.
Prime editing consta de tres elementos. En primer lugar incluye una enzima, ampliamente utilizada en el sistema CRISPR clásico: Cas9. En este caso la nucleasa ha sido modificada para cortar únicamente una de las dos cadenas de ADN, en lugar de introducir un corte limpio que deje dos extremos libres en la hebra de ADN, como hace en el sistema CRISPR. El segundo elemento es una transcriptasa reversa, una enzima que se caracteriza por generar una secuencia de ADN utilizando como molde ARN. El tercer elemento es un fragmento de ARN, denominado pegRNA (de prime editing guide RNA), que tiene dos funciones principales. Por una parte pegRNA posiciona a Cas9 a una posición concreta del ADN. Por otra, actúa como molde para la síntesis de ADN por la transcriptasa reversa. Es decir, el pegRNA incluye la información con el cambio que se desea realizar en el genoma.
Prime editing funciona en dos etapas, en las cuales se modifica cada una de las dos hebras de la molécula de ADN. En un primer paso el pegRNA, que forma un complejo con Cas9 y la transcriptasa reversa, se une por uno de sus extremos a una región específica del genoma por complementariedad de secuencia. Una vez posicionada, la nucleasa Cas9 introduce un corte en la cadena de ADN que es aprovechado por la transcriptasa reversa, que utiliza el otro extremo del propio pegRNA como molde para sintetizar ADN. El fragmento original de ADN que queda expuesto tras sintetizar la nueva cadena es eliminado por endonucleasas propias de la célula, de forma que el resultado de esta primera etapa es una molécula de ADN con una posición desapareada entre sus cadenas, ya que una hebra es la original y la otra tiene una modificación. Para resolver esta situación, en una segunda etapa se utiliza un ARN guía que dirige de nuevo a la enzima Cas 9 a la cadena del ADN no modificada. Cas9 introduce un corte en esta cadena que alerta a los mecanismos de reparación de la célula, que utilizarán la cadena modificada como molde para reparar el ADN.
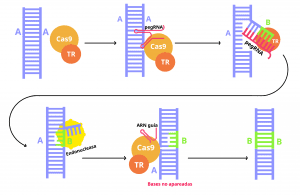
A diferencia del sistema CRISPR tradicional, la nueva herramienta de edición del genoma no necesita un ADN molde para introducir el cambio deseado, sino que esa información está incorporada en el propio pegRNA. La utilización de este ARN con función dual hace que la tecnología prime editing sea más precisa y se reduzca la posibilidad de que se introduzcan otros cambios no deseados en el genoma. Una limitación, sin embargo, es que no permite introducir grandes inserciones o deleciones, debido a que los cambios a introducir en el genoma se encuentran en el pegRNA y el tamaño de este componente debe estar dentro de unos límites para no ser degradado o eliminado por la célula.
Como prueba de concepto de la nueva estrategia, que ya ha sido definida como “algo totalmente distinto, imaginativo y sorprendente” por el investigador Lluis Montoliu, los investigadores han corregido con éxito mutaciones responsables de diversas enfermedades en diferentes tipos de células humanas en cultivo. “La belleza de este sistema es que hay pocas restricciones a la secuencia editada”, destaca Liu. “Puesto que los nucleótidos añadidos están especificados por el pegRNA pueden ser secuencias que difieran de la cadena original en solo una letra, tener más o menos letras o ser una combinación de estos cambios”. En este sentido, prime editing supone una mejora respecto a los editores de bases que permitían modificar el ADN sin cortar el ADN, pero cuyas modificaciones posibles estaban limitadas a únicamente algunos cambios concretos.
El equipo de David Liu planea mejorar la tecnología prime editing y optimizar su rendimiento en los diferentes tipos de células, así como evaluar su funcionamiento en el contexto de modelos animales de enfermedades (hasta el momento la técnica ha sido utilizada únicamente en células). Además, los investigadores destacan la importancia de desarrollar y maximizar los métodos para hacer llegar las herramientas moleculares al núcleo de las células, donde se lleva a cabo la modificación del genoma. Disponer de métodos adecuados adaptados a cada tejido o tipo celular a tratar es un paso imprescindible para cualquier terapia génica o de edición genómica.
Por último, como es habitual en los investigadores del Instituto Broad, el equipo de Liu compartirá los vectores utilizados en el estudio con la comunidad académica y científica, a través de la plataforma Addgene.
Referencia: Anzalone AV, et al. Search-and-replace genome editing without double-strand breaks or donor DNA. Nature. 2019. Doi: https://doi.org/10.1038/s41586-019-1711-4
Fuentes: New CRISPR genome editing system offers a wide range of versatility in human cells. https://www.broadinstitute.org/news/new-crispr-genome-editing-system-offers-wide-range-versatility-human-cells
Ledford H. Super-precise new CRISPR tool could tackle a plethora of genetic diseases. Nature. 2019. doi: http://dx.doi.org/10.1038/d41586-019-03164-5
Si te ha gustado esta noticia y quieres aprender más sobre Genética en Medicina, te interesan nuestros cursos. Tienes más información aquí.