Amparo Tolosa, Genética Médica News

Un equipo de investigadores del Instituto Salk de Estudios Biológicos, dirigido por Juan Carlos Izpisúa Belmonte, ha conseguido revertir las marcas del envejecimiento en células humanas y en ratones mediante la expresión intermitente de un conjunto de genes característicos de las células madre embrionarias.
El envejecimiento es uno de los principales factores de riesgo para el desarrollo de enfermedades como el cáncer, la diabetes, condiciones neurodegenerativas o diversas enfermedades cardiovasculares. Conforme envejecemos los mecanismos responsables de mantener la maquinaria molecular de nuestras células, tejidos y órganos se deterioran, lo que afecta a las diferentes funciones del organismo y repercute gravemente en el estado de salud.
Estudios previos habían demostrado que algunas características celulares típicas del envejecimiento pueden mejorarse durante la reprogramación celular in vitro, proceso que permite desdiferenciar células adultas en células pluripotenciales con capacidad para convertirse en otros tipos celulares. Sin embargo, se desconocía si se podía inducir el mismo efecto in vivo, en un organismo completo.
La reprogramación celular de células diferenciadas a un estado similar al de las células madre embrionarias se lleva a cabo mediante la expresión forzada de cuatro genes, Oct4, Sox2, Klf4, y c-Myc, conocidos como los factores Yamanaka. El conjunto de estos cuatro factores de transcripción induce los cambios de expresión génica y la remodelación epigenética necesarios para revertir el proceso de diferenciación y devolver la célula a un estado pluripotencial.
Para determinar si la reprogramación in vivo tiene un efecto sobre el envejecimiento de un organismo completo, los investigadores utilizaron un modelo animal con el que ya habían trabajado previamente: un modelo en ratón de síndrome de Hutchinson-Gilford, una enfermedad de envejecimiento prematuro. La primera cuestión a la que se enfrentaron fue cómo trasladar un proceso que funciona en células individuales a un animal completo. La reprogramación celular funciona en cultivo en laboratorio pero expresar los factores Yamanaka y modificar de forma continua todas las células de un animal adulto a un estado embrionario en los animales podía tener efectos catastróficos, como por ejemplo, la aparición de cáncer debido a la elevada capacidad proliferativa de las células reprogramadas.
Por esta razón, los investigadores decidieron inducir la expresión de los factores Yamanaka durante un corto periodo de tiempo concreto. En primer lugar, utilizaron la aproximación en células reprogramadas a partir de fibroblastos de los ratones modelo y observaron que la expresión de los cuatro factores durante un corto tiempo mejoraba los rasgos celulares asociados al envejecimiento prematuro, como el daño en el ADN, los defectos de la membrana nuclear o la alteración de mecanismos epigenéticos.
A continuación, el equipo utilizó la aproximación in vivo, en los ratones modelo. Tras optimizar las dosis y el protocolo de expresión de los factores Yamanaka para evitar la aparición de cáncer y otras complicaciones, los investigadores observaron que la reprogramación celular parcial permitía mejorar el fenotipo de envejecimiento prematuro de los ratones. Al comparar con los ratones enfermos no tratados, aquellos en los que se había inducido la expresión de los factores Yamanaka de forma cíclica durante un corto periodo de tiempo parecían más jóvenes, sus órganos funcionaban mejor y vivían un treinta por ciento más.
El siguiente paso del equipo fue investigar si la expresión temporal de los factores Yamanaka también revierte el envejecimiento en células normales. La inducción a corto tiempo de los cuatro genes consiguió mejorar el fenotipo de células humanas y de ratón envejecidas, lo que demostraba la efectividad de la reprogramación en células que habían envejecido fisiológicamente de forma natural y no como consecuencia de una patología.
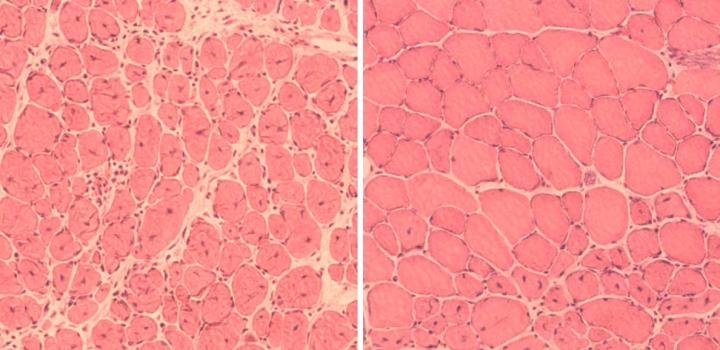
Por último, el equipo estudió el potencial de la reprogramación en ratones normales. De este modo observaron que la inducción temporal de los factores Yamanaka en ratones envejecidos de forma natural mejoraba tanto la capacidad regenerativa del músculo tras un daño, como la del páncreas.
A nivel molecular, los investigadores resaltan la importancia de la remodelación epigenética producida durante la reprogramación celular para la mejora de los rasgos asociados al envejecimiento. “Es difícil decir específicamente por qué el animal vive más,” señala Paloma Martínez Redondo, investigadora del equipo. “Pero sabemos que la expresión de estos factores induce cambios en el epigenoma y que estos llevan a beneficios a nivel celular y del organismo.”

Los resultados del trabajo ofrecen una nueva visión del envejecimiento y procesos asociados, además de plantear aproximaciones dirigidas a retrasar su aparición. «Este trabajo muestra que los cambios epigenéticos dirigen, al menos parcialmente, el envejecimiento,” indica Martínez Redondo. “Nos ofrece un conocimiento emocionante sobre qué rutas podrían utilizarse como diana para retrasar el envejecimiento celular.”
En una sociedad en la que la esperanza de vida es elevada, la posibilidad de disponer de mecanismos para retrasar la aparición de enfermedades asociadas al envejecimiento es muy atractiva. El salto de ratones a humanos es muy grande. No obstante, los resultados obtenidos por el equipo son muy prometedores y abren el camino al desarrollo de nuevas formas para frenar el envejecimiento en humanos. Especialmente interesantes son aquellas basadas en la inducción de cambios epigenéticos epigenéticos por medio de compuestos químicos o moléculas pequeñas. Conviene tener en cuenta, recuerdan los investigadores, que debido a la complejidad del envejecimiento, es posible que todavía queden unos años hasta que cualquier terapia llegue a la fase de ensayos clínicos.
“Obviamente, los ratones no son humanos y sabemos que será mucho más complejo rejuvenecer a una persona,” indica Juan Carlos Izpisúa. “Pero este estudio muestra que el envejecimiento es un proceso muy dinámico y plástico, y por tanto será más susceptible a intervenciones terapéuticas de lo que pensábamos.”

Referencia: Ocampo A, et al. In Vivo Amelioration of Age-Associated Hallmarks by Partial Reprogramming. Cell. 2016. Doi: http://dx.doi.org/10.1016/j.cell.2016.11.052
Fuentes:
Turning back time: Salk scientists reverse signs of aging. http://www.salk.edu/news-release/turning-back-time-salk-scientists-reverse-signs-aging/
Cellular reprogramming slows aging in mice. https://www.eurekalert.org/pub_releases/2016-12/cp-crs120816.php
