La variante APOE4, conocida por aumentar el riesgo a desarrollar enfermedad de Alzheimer, altera el equilibrio del colesterol en las células productoras de mielina y compromete la producción de esta sustancia necesaria para la correcta transmisión de impulsos nerviosos, señala un reciente estudio dirigido por investigadores del Instituto Tecnológico de Massachusetts y publicado en Nature.
La variante APOE4 es el principal factor de riesgo genético conocido para la enfermedad de Alzheimer. Las personas portadoras de una copia de esta variante del gen APOE tienen un riesgo de desarrollar la enfermedad tres veces superior al de las no portadoras, y, en aquellas que tienen dos copias, el riesgo es 12 veces mayor.
APOE codifica para un transportador de lípidos y colesterol, la apolipoproteína E. Hasta el momento se sabía que la variante APOE4, que difiere de la variante más frecuente en un único aminoácido, interfiere con la capacidad del transportador para movilizar los lípidos. También se había relacionado APOE4 con la formación de placas de proteína beta amiloide y la acumulación de proteína tau. No obstante, todavía se desconocían los mecanismos exactos de cómo APOE4 aumenta la susceptibilidad de una persona a desarrollar alzhéimer.
Un reciente estudio internacional, dirigido por investigadores del Instituto de Tecnología de Massachusetts (MIT) aporta nueva información sobre el papel de APOE4 en la predisposición al alzheimer. A partir del análisis de lípidos y expresión génica en cerebros postmortem y diversos modelos experimentales, los investigadores han encontrado que APOE4 interfiere con el equilibrio de lípidos y la producción de mielina por parte de los oligodendrocitos. Los resultados del trabajo ofrecen, además, posibles vías de desarrollo de tratamientos, basados en recuperar la correcta movilización de los lípidos.
Un mapa celular cerebral del impacto de APOE4
En primer lugar, los investigadores analizaron la expresión génica en células individuales del córtex prefrontal de cerebros post mortem de 32 personas, 20 de ellas con enfermedad de Alzheimer. Además, en el grupo se incluían tanto portadores de APOE4 (con 1 o 2 copias) como no portadores (con la variante APOE3).
El análisis de actividad génica de más de 160 000 células individuales reveló que la presencia de APOE4 estaba relacionada con cambios en la expresión de diferentes tipos celulares e identificó rutas moleculares afectadas, entre las que se encuentra el estrés celular y el metabolismo energético. Algunas de estas rutas ya eran conocidas por su relación con la enfermedad. Además, el análisis de expresión dentro de los diferentes tipos de células reveló nuevas rutas de interés.
Li-Huei Tsai, investigadora del Departamento de Ciencias Cognitivas y del Cerebro del MIT y directora del trabajo, destaca que el análisis de expresión de células individuales muestra que APOE4 influye de forma muy diferente en los distintos tipos de células cerebrales. “Vemos convergencia de que el metabolismo de los lípidos está alterado, pero cuando se mira en detalle el tipo de rutas lipídicas que están alteradas en los diferentes tipos de células cerebrales son todas diferentes”, señala la investigadora.
APOE4 influye en la formación de mielina
Al enfocar su atención en las alteraciones relacionadas con el metabolismo de lípidos, el equipo detectó que APOE4 altera el equilibrio del colesterol en los oligodendrocitos e interfiere con la producción de mielina.
Los oligodendrocitos son células gliales especializadas conocidas principalmente por su función de producción y mantenimiento de la mielina, sustancia que recubre los axones nerviosos y facilita la transmisión de las señales. La mielina está formada por la proteína básica de la mielina, colesterol (que los oligodendrocitos obtienen a partir de su propia síntesis o de la importación desde el exterior) y otros componentes.
A través de modelos celulares y en ratón, los investigadores encontraron que en presencia de APOE4 se produce una acumulación mayor de colesterol en el retículo endoplásmico de los oligodendrocitos. Además, el equipo ha detectado que el desequilibrio en el colesterol desencadena una situación de estrés intracelular que deriva en una disminución en la producción de la proteína básica de la mielina, otro componente esencial de la mielina. Como consecuencia final, la producción de mielina es menor, lo que implica una reducción en el grosor de las vainas de mielina que recubren las prolongaciones nerviosas.
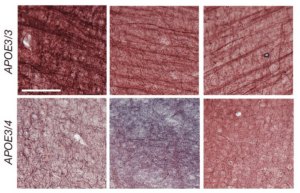
Las diferencias en el proceso de mielinización también se detectan en los cerebros post mortem analizados: los investigadores encontraron una menor expresión de genes relacionados con producción de mielina y observaron que en las personas portadoras de APOE4 la capa de mielina de los axones analizados era más fina que la de las personas portadoras de APOE3. Interesantemente, estas características también se detectaron en personas portadoras de APOE4 que no habían mostrado síntomas de enfermedad de Alzheimer. Esta circunstancia sugiere que los mecanismos que condicionan una mayor vulnerabilidad a la enfermedad están presentes de forma temprana.
Recuperar el transporte de colesterol revierte el efecto de APOE4 sobre la mielinización
Por último, los investigadores se plantearon si sería posible revertir el efecto de APOE4 sobre la producción de mielina recuperando el equilibrio en el transporte de lípidos.
Tras probar con diferentes fármacos que influyen en la síntesis o en el transporte del colesterol en cultivos celulares y un modelo en ratón, el equipo encontró que el tratamiento con ciclodextrina reduce la acumulación de colesterol y mejora la mielinización. Además, en el caso de los ratones con APOE4, el tratamiento con este fármaco mejoró su rendimiento en dos pruebas diferentes de memoria, lo que sugiere una relación entre el incremento de mielinización en estos animales y sus habilidades cognitivas.
Nuevas perspectivas sobre los mecanismos que intervienen en el alzhéimer y desarrollo de tratamiento
Los investigadores plantean que la conexión establecida entre la alteración en el equilibrio del colesterol y la formación de mielina en las personas portadoras de APOE4 puede influir en la susceptibilidad a la enfermedad de Alzheimer o en su gravedad. Estos resultados apuntan, por lo tanto, a un papel relevante de los oligodendrocitos en el desarrollo y progresión del Alzheimer a través de su función como células productoras de mielina.
El equipo también señala que los defectos en la producción de mielina podrían influir en la edad de inicio de la enfermedad aumentando la vulnerabilidad a los signos patológicos que se van acumulando con el envejecimiento progresivo.
Además de ofrecer un mecanismo por el que APOE4 puede facilitar el desarrollo de Alzhéimer, los resultados del trabajo apuntan hacia una vía de tratamiento para recuperar la mielinización: facilitar el transporte de colesterol. De momento, el tratamiento con ciclodextrina ofrece resultados positivos in vitro y en modelos animales a través de su acción sobre los oligodendrocitos. No obstante, queda por determinar cómo pueden influir otros tipos celulares sobre la función de los oligodendrocitos y cómo afectaría a estas células y su función el tratamiento.
Por último, más allá de identificar el papel de los oligodendrocitos y la mielinización como elementos centrales del papel de APOE4 en el alzheimer, el estudio ofrece una herramienta de valor para el estudio del alzheimer: un mapa de expresión en córtex prefrontal de células individuales de personas con diferente genotipo para APOE y pacientes y controles para el alzheimer. Los datos están disponibles en
Artículo científico: Blanchard, J.W., Akay, L.A., Davila-Velderrain, J. et al. APOE4 impairs myelination via cholesterol dysregulation in oligodendrocytes. Nature 611, 769–779 (2022). https://doi.org/10.1038/s41586-022-05439-w
Fuentes:
Alzheimer’s risk gene undermines insulation of brain’s “wiring”. https://news.mit.edu/2022/alzheimers-risk-gene-undermines-insulation-of-brain-wiring-1122
Dolgin E. This is how an Alzheimer’s gene ravages the brain. Nature News. 2022. DOI: https://doi.org/10.1038/d41586-022-03724-2
Carlström K y Castelo-Branco G. Alzheimer’s risk variant APOE4 linked to myelin-assembly malfunction. News and Views. Nature. 2022. DOI: https://doi.org/10.1038/d41586-022-03371-7
Si te ha gustado esta noticia y quieres aprender más sobre Genética en Medicina, te interesan nuestros cursos y formación universitaria.