Paula Ortiz-Romero 1,2, Victoria Campuzano1,2,3
1Departament de Ciències Experimentals i de la Salut, Universitat Pompeu Fabra, Barcelona, España.
2Institut Hospital del Mar d’Investigacions Mèdiques (IMIM), Barcelona, España.
3Centro de Investigación Biomédica en Red de Enfermedades Raras (CIBERER), ISCIII, Barcelona, España.
El síndrome de Williams-Beuren (SWB) es un trastorno del neurodesarrollo causado por la deleción heterocigota de 26-28 genes contiguos (1.55-1.83Mb) en el cromosoma 7q11.23 que afecta a 1/7500-1/20000 recién nacidos. Los pacientes afectados presentan discapacidad intelectual leve-moderada, hipersociabilidad, ansiedad, descoordinación motora y déficits de integración visuoespacial.
En la región delecionada se encuentra, entre otros, el gen de la elastina (ELN, OMIN: 130160). Debido a la deficiencia de esta proteína los pacientes presentan una arteriopatía generalizada, con estructuras lamelares desorganizadas y fibras elásticas fragmentadas. Las complicaciones cardiovasculares son la causa más común de problemas de salud e incluso muerte en estos pacientes, que tienen un riesgo de muerte súbita 25-100 veces mayor que la población general en la misma franja de edad.
El modelo murino de la deleción (CD) recopila varios rasgos comportamentales y cardiovasculares que se observan en los pacientes con el SWB (Segura-Puimedon M, et al. 2014), por lo que se trata de un buen modelo para el estudio del fenotipo de la enfermedad así como de los efectos de distintos tratamientos.
La epigalocatequina-3-galato (EGCG) es la catequina más abundante del té verde, y su consumo se ha asociado a potenciales efectos terapéuticos en cáncer, enfermedades cardiovasculares, inflamatorias y neurológicas. Sus efectos beneficiosos se han atribuido principalmente a sus potentes efectos antioxidantes y captadores de radicales libres, además de su interacción con un amplio rango de vías de señalización celular. Por este motivo, hemos realizado un tratamiento con EGCG en los ratones CD para evaluar sus efectos sobre el fenotipo de WBS, tanto a nivel cardiovascular como neurocognitivo.
Fenotipo cardiovascular
Los ratones CD presentan un fenotipo cardiovascular caracterizado por hipertensión e hipertrofia cardíaca debida a un aumento de la medida de los cardiomiocitos.
El análisis de los niveles de estrés oxidativo mediante tinción con DHE muestra un ligero aumento (sobre el 20%) en los ratones CD en comparación con los ratones WT. En este modelo de ratón, la vía relacionada con NOX2 no se encuentra alterada. Estudios anteriores sugieren que los efectos antioxidantes de la EGCG se relacionan con la vía de NRF2, ya que la catequina aumenta la translocación de NRF2 al núcleo, potenciando así la transcripción de antioxidantes endógenos.
Los resultados de este estudio muestran una reducción significativa de los niveles nucleares de NRF2 en cardiomiocitos CD que se correlaciona con una menor expresión del mRNA de genes regulados como Nqo1 por esta vía. El tratamiento con EGCG resulta ser efectivo para recuperar los niveles nucleares normales de NRF2 y la expresión de sus genes diana.
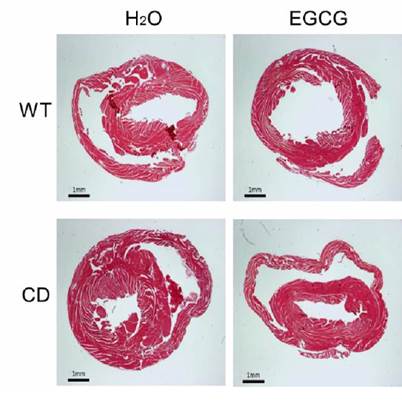
También se ha observado que tras el tratamiento con EGCG no se observa hipertrofia cardíaca en los ratones CD ya que se recupera la medida normal de los cardiomiocitos.
Por tanto, la mejora de la hipertrofia cardíaca después del tratamiento con EGCG en los ratones CD podría deberse a cambios en la regulación del estrés oxidativo mediante NRF2 que protegerían contra la hipertrofia.
Fenotipo neurocognitivo
Los ratones CD presentan un fenotipo neurocognitivo caracterizado por hipersociabilidad, descoordinación motora, ansiedad, problemas en la memoria a corto plazo y en la memoria de trabajo. A nivel neuroanatómico se observa una reducción en el número de espinas dendríticas y una desorganización de los axones.
Estudios recientes muestran que la administración de EGCG en diferentes modelos murinos de síndrome de Down consigue recuperar el déficit de aprendizaje dependiente de hipocampo. En nuestro estudio los efectos beneficiosos del tratamiento con EGCG a nivel neurocognitivo se restringen a mejoras en la memoria a corto plazo, sin efectos en la memoria de trabajo espacial, la ansiedad o la sociabilidad.
Numerosos estudios han apoyado el papel de la EGCG en la expresión de BDNF. Nuestros resultados muestran que los animales CD tratados con EGCG presentan niveles de expresión de Bdnf normalizados aunque sin ningún efecto en la remodelación neuroanatómica.
Homeostasis del calcio
Con frecuencia se han descrito anormalidades en la homeostasis del calcio en el SWB. Tanto la funcionalidad neuronal como la de los cardiomiocitos son procesos que requieren cascadas de señalización muy controladas, la mayoría de las cuales dependen del calcio intracelular.
En cultivos primarios de hipocampo hemos observado que las células CD tienen un flujo intracelular de calcio alterado. Además, estudios previos demuestran que para que BDNF pueda mediar en la generación y remodelación dendrítica es necesaria la funcionalidad de los canales RyR3, encargados de la liberación de calcio del retículo endoplásmico. Hemos observado que la expresión de RyR3 en el hipocampo de los ratones CD está significativamente aumentada en comparación con los ratones WT. Así pues, aunque el tratamiento con EGCG consigue normalizar la expresión de BDNF, este problema en la regulación del calcio podría estar impidiendo la acción de BDNF y por tanto los efectos de recuperación que esperábamos.
A nivel cardiovascular, los ratones CD también presentan niveles altos de RyR2, la principal molécula responsable de la contracción de los miofilamentos dependiente de calcio. La sobreexpresión de RyR2 puede alterar la estequiometria del canal con consecuencias negativas para la función de los cardiomiocitos e incrementar la sensibilidad al calcio de estas células.
En estudios previos se ha comprobado que la EGCG disminuye la sensibilidad al calcio en miofilamentos cardíacos, y que puede inhibir totalmente la hipertrofia cardíaca y mejorar la funcionalidad cardíaca en ratas con hipertensión. Así pues, y todavía en proceso de estudio, disminuir la sensibilidad al calcio mediante la regulación de RyR2 podría tener un efecto cardioprotector.

Sugerimos que la alteración de la homeostasis del calcio en los pacientes con SWB, sin ser la causa principal, juega un papel relevante en los fenotipos cardiovascular y cognitivo de estos pacientes. Esta alteración podría deberse a la desregulación de los receptores RyR2/3 y al incremento de sensibilidad al calcio, tanto en neuronas como en cardiomiocitos.
Por este motivo, la EGCG podría ser un agente terapéutico prometedor para los pacientes con SWB gracias a, entre otros mecanismos, el aumento de expresión de genes dependientes de NRF2, el aumento de los niveles de BDNF y la disminución de la sensibilidad al calcio.
Referencia: Ortiz-Romero P, Borralleras C, et al. Epigallocatechin-3-gallate improves cardiac hypertrophy and short-term memory deficits in a Williams-Beuren syndrome mouse model. PLoS ONE. 2018; 13(3):e0194476. https://doi.org/10.1371/journal.pone.0194476
Referencias: Segura-Puimedon M, Sahún I, et al. Heterozygous deletion of the Williams-Beuren syndrome critical interval in mice recapitulates most features of the human disorder. Hum Mol Genet. 2014;23: 6481–6494. doi:10.1093/hmg/ddu368

