Genética Médica News
Identificado un gen humano clave para la síntesis de los plasmalógenos, un tipo de fosfolípidos relacionados con la enfermedad de Alzheimer y el cáncer
- noviembre 21, 2019
Montserrat Elías Arnanz, Universidad de Murcia
- El hallazgo, llevado a cabo por investigadores del Área de Génetica de la Universidad de Murcia y del Instituto de Química Física “Rocasolano” del CSIC en Madrid, se publica en la revista Science.
- Los científicos logran identificar el gen humano investigando con una bacteria que sintetiza plasmalógenos y los utiliza para responder a la luz.
- El estudio proporciona una diana directa para estudiar el papel de estos lípidos en varias patologías humanas.
El grupo de investigación dirigido por Montserrat Elías Arnanz, Catedrática de Génetica de la Universidad de Murcia, ha descubierto que el gen denominado TMEM189 es fundamental para la síntesis de una clase de lípidos denominados plasmalógenos. Los otros investigadores del grupo implicados en el trabajo son Aránzazu Gallego, Antonio Monera, Elena Pajares, Eva Bastida, Ricardo Pérez, Antonio Iniesta y Marta Fontes. Además, ha participado como codirector del trabajo Subramanian Padmanabhan, Profesor de Investigación del Instituto de Química-Física “Rocasolano” del CSIC.
Los plasmalógenos son un tipo particular de fosfolípidos presentes casi exclusivamente en las membranas celulares de los animales y de muy pocas bacterias. La seña de identidad de los plasmalógenos es que uno de los ácidos grasos del fosfolípido se encuentra unido mediante un enlace vinil-éter, en lugar del típico enlace éster. La presencia del enlace vinil-éter confiere propiedades especiales a estos lípidos, tales como la capacidad de modular la estructura y la dinámica de las membranas, así como un posible papel antioxidante y señalizador.
En el ser humano, los plasmalógenos abundan en el cerebro y el corazón. Se ha descrito que la cantidad de plasmalógenos aumenta rápidamente en edades tempranas, durante la fase de mielinización intensa, y comienza a disminuir a partir de la mediana edad. Diversas patologías neurodegenerativas comunes como la enfermedad de Alzheimer, y algunas más raras como el síndrome de Zellweger, correlacionan con una disminución significativa en los niveles de plasmalógenos. Varios tipos de cáncer cursan con cambios notables de la cantidad de plasmalógenos, lo que ha llevado a proponer su uso como marcadores tempranos del proceso tumoral.
Desde hace casi 50 años, una de las incógnitas en la biosíntesis de los plasmalógenos ha sido la identidad de la enzima con actividad desaturasa que genera el enlace vinil-éter a partir del fosfolípido precursor con enlace éter. Esta enzima estaba clasificada como huérfana porque se desconocía el gen que la determinaba.
“El logro más llamativo de este trabajo es que hemos descubierto el gen correspondiente, que se ha mostrado esquivo durante décadas” señala la Dra. Elías Arnanz. “Además, un aspecto fascinante de nuestro estudio es que hemos conseguido desenmascarar el gen humano de una manera muy inusual, la del estudio de una bacteria”.
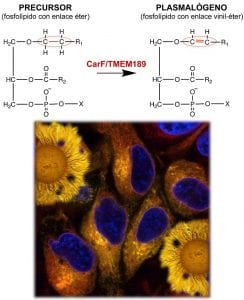
Desde hace años, el grupo de investigación está interesado en entender cómo una bacteria que vive en el suelo, Myxococcus xanthus, es capaz de distinguir entre la luz y la oscuridad. Cuando se expone a la luz, la bacteria sintetiza unos pigmentos protectores que la defienden de los daños oxidativos provocados por la luz solar. “Nuestro empeño por descubrir el papel de un gen clave para que la bacteria perciba la luz, el gen carF, ha sido lo que nos ha conducido a identificar el gen humano”. A diferencia de la gran mayoría de bacterias, M. xanthus sí puede sintetizar plasmalógenos, como los seres humanos y los animales. Esto ha permitido demostrar que los plasmalógenos son esenciales para que la bacteria perciba que se encuentra expuesta a la luz. Esta función de los plasmalógenos, la de permitir que una bacteria vea la luz, es muy novedosa.
Hace tiempo, los investigadores advirtieron que los animales, incluido el ser humano, contenían un gen cuyo producto proteico, de función desconocida, era muy similar a la proteína CarF de la bacteria. En el trabajo, se ha podido comprobar que las proteínas correspondientes a CarF en humanos y en varios animales como el ratón, el pez cebra, el gusano y la mosca funcionan en la bacteria igual que la suya propia. También se ha demostrado que la inactivación del gen en células humanas, usando la tecnología CRISPR-Cas, provoca la desaparición de los plasmalógenos. Por lo tanto, se concluye que la proteína de humanos y la de la bacteria comparten la misma función, a pesar de la enorme distancia evolutiva entre ambos organismos.
Hasta ahora, la función atribuida a los plasmalógenos en humanos se ha basado en el estudio del efecto de mutaciones en genes que participan en pasos anteriores de la ruta de biosíntesis. Esto tiene el inconveniente de que, además de los plasmalógenos, desaparecen los lípidos precursores con enlace éter, que también podrían desempeñar alguna función celular. El descubrimiento de que TMEM189 es el gen que determina la enzima responsable para la síntesis de los plasmalógenos permitirá un análisis directo del papel de los plasmalógenos y su relación con diversas patologías. Mediante mutación del gen TMEM189 ahora es posible generar animales modelo que carezcan de plasmalógenos, pero mantengan los fosfolípidos precursores, para discernir cuáles son las funciones de estos lípidos tan enigmáticos.
Además, el trabajo proporciona una plataforma sencilla y rápida para estudiar el impacto funcional de posibles mutaciones que se encuentren en un futuro en el gen humano; bastaría con introducir la versión mutada en la bacteria y analizar si el cambio afecta o no a la respuesta a la luz, como se ha hecho en este trabajo para la versión normal del gen humano.
Referencia:
Aránzazu Gallego-García, Antonio J. Monera-Girona, Elena Pajares-Martínez, Eva Bastida-Martínez, Ricardo Pérez-Castaño, Antonio A. Iniesta, Marta Fontes, S. Padmanabhan y Montserrat Elías-Arnanz. A bacterial light response reveals an orphan desaturase for human plasmalogen synthesis. Science 366: 128-132, 4 Oct. 2019. DOI: http://dx.doi.org/10.1126/science.aay1436
Si te ha gustado esta noticia y quieres aprender más sobre Genética en Medicina, te interesan nuestros cursos. Tienes más información aquí.
Categorías
- Actualidad
- Congresos
- Coronavirus
- CRISPR
- Debates
- Diagnóstico Genético
- Enfermedades Raras
- Entrevistas
- Envejecimiento y longevidad
- Epigenética
- Farmacogenética
- Formación
- Genética del cáncer
- Genética en Cardiología
- Medicina Reproductiva
- Microbiología molecular
- Neurociencia
- Noticias de Genotipia
- Noticias de investigación
- Noticias patrocinadas
- Proyectos
- Reseñas de libros
- Terapia Génica
- Tratamientos
Cursos relacionados
Contacto
¿Quieres publicar con nosotros? ¿Tienes dudas?
Contacta con nosotros de la manera que prefieras y te responderemos a la mayor brevedad.