Amparo Tolosa, Genética Médica News
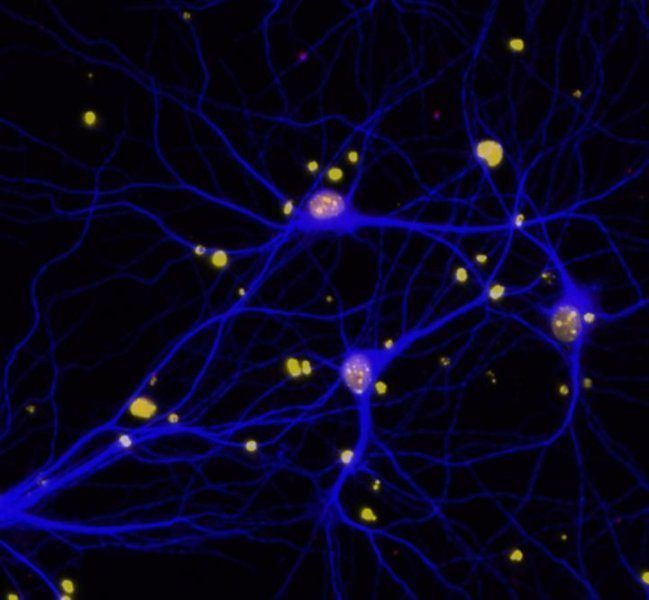
El gen BRCA1 es conocido principalmente por su relación con el cáncer. Algunas mutaciones en este gen aumentan el riesgo de cáncer de mama y ovario y representan un porcentaje importante de las formas hereditarias de ambos tipos de cáncer. Además, las mutaciones en el gen son frecuentes en otros tumores. BRCA1 codifica para una proteína que interviene en la reparación de daños en el material hereditario. Concretamente, BRCA1 se une a roturas producidas en la doble cadena del ADN y recluta a otros factores de reparación para evitar la degradación enzimática del ADN y promover su reparación.
Además de su importante papel como gen supresor de tumores, un reciente estudio acaba de revelar que BRCA1 es regulado por la actividad neuronal y se encarga de proteger el genoma de las células nerviosas. El trabajo muestra también que los niveles de BRCA1 están disminuidos en los pacientes con enfermedad de Alzhéimer, relacionando por primera vez el gen y su producto con un desorden neurológico.
El equipo de investigadores, dirigido por Lennart Mucke, director del Instituto Gladstone de Enfermedades Neurológicas en San Francisco, EE.UU., había encontrado previamente que el aumento de actividad cerebral aumenta transitoriamente el número de roturas en el ADN sin que esto cause la muerte de las neuronas. Basándose en estos resultados, el equipo especuló que los ciclos de daño y reparación del ADN que se producen en las células nerviosas facilitan el aprendizaje y la memoria. Así, si los mecanismos de reparación del ADN no funcionan correctamente y el equilibrio entre el daño y reparación del ADN se desplaza hacia la acumulación de daños, las neuronas se ven afectadas y se producen déficits en las habilidades cognitivas.
Con el objetivo de profundizar en esta idea, los investigadores analizaron los niveles de los diferentes componentes de la maquinaria de reparación de las roturas de doble cadena en el ADN en ratones modelo para Alzhéimer y ratones control. De este modo, encontraron una reducción selectiva de BRCA1 en diversas regiones cerebrales, respecto al resto de componentes que intervienen en la reparación del ADN. La misma reducción generalizada fue observada en muestras de pacientes con Alzhéimer.
A continuación, el equipo bloqueó la expresión de BRCA1 en el modelo en ratón, encontrando un aumento en el número de roturas en el ADN en las neuronas de las regiones cerebrales analizadas. La reducción de BRCA1 reduce el tamaño de las células nerviosas y la densidad del árbol dendrítico – las prolongaciones que utilizan para recibir estímulos -, aumenta su excitabilidad y disminuye su capacidad de respuesta o plasticidad. Esto, unido al aumento en la inestabilidad genómica derivada de la incapacidad de BRCA1 para reparar el ADN, provoca déficits en la memoria y aprendizaje en los ratones modelo.
“BRCA1 ha sido hasta ahora estudiado principalmente en células en división, multiplicándose y en cáncer, que se caracteriza por el aumento anormal del número de células,” indica Elsa Suberbielle, primera autora del trabajo. “Por esta razón nos sorprendió encontrar que también juega un papel importante en neuronas, las cuales no se dividen y en un desorden neurodegenerativo caracterizado por la pérdida de estas células cerebrales.”
Por último, los investigadores demostraron que la acumulación de proteína beta amiloide en el cerebro de los ratones modelo – característica frecuente en los pacientes con Alzhéimer – reduce los niveles de BRCA1, lo que contribuye a las alteraciones cognitivas que se producen en la enfermedad.
Los resultados del trabajo no sólo revelan un nuevo marco de actuación para BRCA1, sino que también plantean nuevas preguntas sobre los mecanismos por los que actúa esta proteína supresora de tumores en las células nerviosas. Por ejemplo, se desconoce a través de qué ruta de reparación del ADN repara las roturas del ADN en las neuronas maduras, que a diferencia de las células tumorales no se dividen.
Además, proporcionan una nueva aproximación para el tratamiento del Alzhéimer. “La manipulación terapéutica de los factores de reparación como BRCA1 podría ser utilizada para prevenir los daños neuronales y el deterioro cognitivo en los pacientes con Alzhéimer o las personas en riesgo a desarrollar la enfermedad,” manifiesta Lennart Mucke. “Normalizando los niveles o la función de BRCA1, podría proteger a las neuronas del daño en el ADN excesivo y prevenir los procesos nocivos que esto inicia.”
Referencia: Suberbielle E, et al. DNA repair factor BRCA1 depletion occurs in Alzheimer brains and impairs cognitive function in mice. Nat Commun. 2015 Nov 30;6:8897. doi: 10.1038/ncomms9897.
Fuente: DNA Repair Protein BRCA1 Implicated in Cognitive Function and Dementia. https://gladstone.org/about-us/press-releases/dna-repair-protein-brca1-implicated-cognitive-function-and-dementia
