Antonio Garcia-Gomez1, Tianlu Li1, Mercedes Garayoa2 & Esteban Ballestar1
1Grupo de Epigenética e Inmunidad, Instituto de Investigación contra la Leucemia Josep Carreras (IJC), 08916 Badalona, Barcelona
2Centro de Investigación del Cáncer, Instituto de Biología Molecular y Celular del Cáncer (IBMCC, Universidad de Salamanca-CSIC) y Hospital Universitario de Salamanca-IBSAL, 37007 Salamanca.
El mieloma múltiple (MM) es un tipo prevalente de cáncer de la sangre, que representa más del 10% de todos los cánceres hematológicos. Entre las principales complicaciones del MM están las relacionadas con el hueso, tales como la osteoporosis, lesiones líticas y fracturas, que tienen un gran impacto en la calidad de vida de los pacientes y, en última instancia, en su supervivencia. Por otro lado, hasta el 80% de los pacientes de MM desarrollan problemas óseos durante el curso de la enfermedad. Dada la naturaleza incurable de estas lesiones óseas, es de gran urgencia identificar nuevas dianas terapéuticas dirigidas no solo a reducir la progresión tumoral sino también a revertir las lesiones óseas asociadas.
Entre las estrategias destinadas a revertir las lesiones óseas en el MM, las únicas aprobadas hasta la fecha van dirigidas a inhibir o destruir los osteoclastos, responsables de la destrucción del hueso y con actividad exacerbada en MM.
Una posible diana celular, alternativa a los osteoclastos, lo constituyen las células mesenquimales estromales (MSCs, de las siglas en inglés), directamente relacionadas con el proceso de remodelación ósea ya que son progenitores de los osteoblastos formadores de hueso. Específicamente, en MM se produce un deterioro en la diferenciación y función de los osteoblastos a partir de los precursores mesenquimales, lo que se traduce en destrucción ósea. Las lesiones óseas persisten en muchos pacientes con mieloma incluso después de la remisión terapéutica, lo que sugiere un defecto a largo plazo en las MSCs que bloquea su capacidad para diferenciarse adecuadamente a osteoblastos funcionales.
Durante una gran parte de su carrera científica, Antonio García-Gómez y Mercedes Garayoa han investigado las alteraciones de las MSCs de la médula ósea en el MM y su relevancia en el contexto de esta enfermedad. Aparte de su papel precursor de los osteoblastos, las MSCs de la médula ósea desempeñan un papel fundamental en el apoyo a la progresión del mieloma y la resistencia a los medicamentos.
Dada la naturaleza de esta enfermedad, se sabe que las alteraciones en las MSCs son el resultado de su interacción con las células plasmáticas cancerosas. Esto coloca a las MSCs como una diana atractiva para tratar la enfermedad ósea del mieloma. Recientemente, nuestro equipo ha publicado en la revista Nature Communications (Garcia-Gomez et al., 2021) un estudio donde se describen por primera vez alteraciones epigenéticas en las MSCs de pacientes en diferentes etapas en la progresión hacia MM. Estas alteraciones epigenéticas, principalmente en la metilación del DNA, se identificaron en sitios genómicos relacionados con genes que controlan la diferenciación adecuada de las MSC a osteoblastos, como los conocidos genes HOX, así como en otros genes necesarios para la correcta función de los osteoblastos como RUNX2, SPP1 (osteopontina) o IBSP (sialoproteína ósea).
Durante los últimos años se han publicado numerosos estudios relacionados con la adquisición de alteraciones de la metilación del DNA en diferentes tipos de cáncer. Las alteraciones en la metilación del DNA suelen tener un impacto directo en la expresión de los genes a los que afecta. En el estudio que hemos publicado recientemente, demostramos que las células de mieloma son capaces de influir en el perfil de metilación de las MSCs, que se encuentran en el microentorno tumoral, aunque no son propiamente cancerosas. En los últimos años se ha evidenciado el papel fundamental del microambiente tumoral como mediador de la progresión tumoral y la inmunosupresión en varios tipos de cáncer. La interacción recíproca entre las células neoplásicas y las no tumorales está mediada por el contacto directo de célula a célula, factores solubles y exosomas que dan como resultado patrones de expresión génica diferencial que son impulsados por mecanismos epigenéticos (Garcia-Gomez, Rodríguez-Ubreva and Ballestar, 2018).
Dado que las alteraciones epigenéticas son farmacológicamente reversibles, en nuestro estudio investigamos si revertir las alteraciones de la metilación del DNA en las MSCs de mieloma podría restaurar su fenotipo a osteoblastos sanos.
Durante el curso del proyecto utilizamos una molécula, CM-272, con capacidad de inhibición dual tanto de DNA metiltransferasas (DNMTs) como de la histona metiltransferasa G9a, desarrollada por el equipo de Felipe Prósper y previamente publicada en Nature Communications por su actividad en otras neoplasias hematológicas (José-Enériz et al., 2017). También se ha demostrado que este doble inhibidor es capaz de desencadenar la represión inmune en el cáncer de vejiga (Segovia et al., 2019).
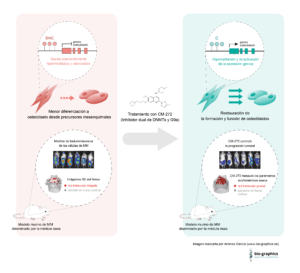
En el contexto del MM, observamos que el tratamiento de MSCs de pacientes con CM-272 revierte su fenotipo aberrante y ayuda a la correcta diferenciación de las MSCs a osteoblastos formadores de hueso (Figura 1). Este es un resultado directo de la reversión de la metilación del DNA aberrante en estas células por la acción del inhibidor. Además, el tratamiento con CM-272 pudo reducir tanto la carga tumoral como mejorar la pérdida ósea asociada al MM en un modelo de ratón de MM diseminado en la médula ósea (Figura 1), empleado previamente por el equipo de Mercedes Garayoa (Garcia-Gomez et al., 2014).
De manera interesante, otro trabajo reciente ha demostrado que la reducción simultánea de G9a y DNMT1 estimula la expresión osteogénica y la mineralización de la matriz ósea en un modelo de rata destinado al estudio de la pérdida ósea en condiciones de ingravidez (Bing et al., 2021).
Nuestro trabajo proporciona evidencia de un gran potencial para el tratamiento de la epigenética alterada en pacientes con MM, para tratar la enfermedad ósea asociada a esta enfermedad.
Artículo original: Garcia-Gomez, A. et al. Targeting aberrant DNA methylation in mesenchymal stromal cells as a treatment for myeloma bone disease. Nat Commun. 2021. 12(1), p. 421. doi: http://dx.doi.org/10.1038/s41467-020-20715-x
Bibliografía
Bing, L. et al. Crosstalk between histone and DNA methylation mediates bone loss in hind limb unloading. Journal of Bone and Mineral Research. 2021. doi: 10.1002/jbmr.4253.
Garcia-Gomez, A. et al. Preclinical activity of the oral proteasome inhibitor mln9708 in myeloma bone disease. Clinical Cancer Research. 2014, 20(6), pp. 1542–1554. doi: 10.1158/1078-0432.CCR-13-1657.
Garcia-Gomez, A., Rodríguez-Ubreva, J. y Ballestar, E. Epigenetic interplay between immune, stromal and cancer cells in the tumor microenvironment. Clinical Immunology. 2018. 196, pp. 64–71. doi: 10.1016/j.clim.2018.02.013.
José-Enériz, E. S. et al. ‘Discovery of first-in-class reversible dual small molecule inhibitors against G9a and DNMTs in hematological malignancies. Nat Comm. 2017. doi: 10.1038/ncomms15424.
Segovia, C. et al. Inhibition of a G9a/DNMT network triggers immune-mediated bladder cancer regression. Nat Medicine. 2019, 25(7), pp. 1073–1081. doi: 10.1038/s41591-019-0499-y.
Si te ha gustado esta noticia y quieres aprender más sobre Genética en Medicina, te interesan nuestros cursos y formación universitaria, así como nuestro canal audiovisual, Genotipia TV.



