Una terapia experimental basada en ARN mensajero logra restaurar la producción de espermatozoides en ratones estériles debido a un defecto genético.
Los animales tratados produjeron crías sanas mediante técnicas de reproducción asistida, lo que sugiere una posible vía futura para tratar ciertos casos de infertilidad masculina.
La infertilidad afecta aproximadamente al 10 % de las parejas en todo el mundo. En cerca de la mitad de los casos, está relacionada con factores masculinos, como por ejemplo, defectos genéticos que alteran la producción de espermatozoides.
Cuando la espermatogénesis se detiene antes de producir gametos con la dotación cromosómica adecuada, las técnicas habituales de reproducción asistida no siempre son útiles. Durante las últimas décadas, se han explorado diferentes estrategias para tratar este tipo de infertilidad genética. Una posibilidad es utilizar terapia génica para introducir copias normales de genes defectuosos relacionados con la formación de gametos. Sin embargo, la posibilidad de que el ADN introducido se integre en el genoma de forma permanente ha limitado su desarrollo clínico. En este contexto, el ARN mensajero podría ser una alternativa más segura, ya que permite la producción temporal de proteínas sin modificar permanentemente el genoma celular.
Un estudio liderado por investigadores de la Universidad de Kioto ha evaluado esta posibilidad en un modelo experimental de infertilidad masculina en ratón. Los resultados, publicados en Stem Cell Reports, muestran que la administración dirigida de ARN mensajero en el testículo puede restaurar la producción de espermatozoides y permitir el nacimiento de descendencia sana.
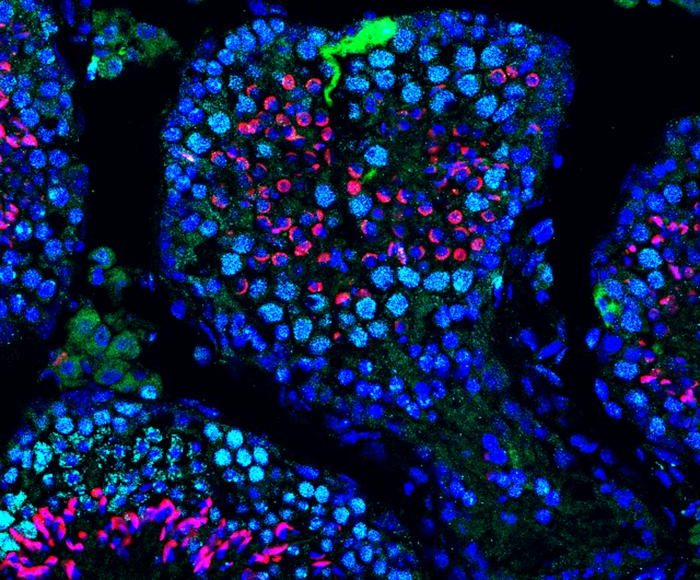
Una terapia con ARN mensajero dirigida a las células de Sertoli
Para evaluar si una terapia basada en ARN mensajero podría restaurar la producción de células germinales los investigadores enfocaron su trabajo en la infertilidad masculina asociada a alteraciones en las células de Sertoli. Estas células, presentes en los túbulos seminíferos, proporcionan soporte a las células germinales y regulan el entorno donde se desarrolla la espermatogénesis.
Los investigadores partieron de un modelo de ratón con alteraciones en el gen Cldn11. Este gen codifica la proteína CLDN11, un componente de las uniones estrechas que forman la barrera hematotesticular, una estructura creada por las células de Sertoli y esencial para la espermatogénesis. En ratones, la ausencia de CLDN11 provoca un bloqueo de la producción de espermatozoides. Alteraciones en CLDN11 también se han asociado a infertilidad masculina y otros trastornos testiculares en humanos, lo que convierte a este gen en un modelo relevante para estudiar posibles estrategias terapéuticas.
Para intentar revertir la ausencia de CLDN11, el equipo introdujo ARN mensajero que codifica la proteína directamente en los testículos mediante microinyección en el conducto eferente. Esta vía de administración permitía que el ARNm llegara a los túbulos seminíferos y fuese captado principalmente por las células de Sertoli donde se expresa el gen.
Aunque la expresión del ARNm fue temporal, el tratamiento permitió reactivar la espermatogénesis en parte de los túbulos seminíferos. Dos meses después del tratamiento se detectaron espermátidas haploides (espermatozoides inmaduros), que posteriormente pudieron utilizarse para generar embriones y crías viables mediante microinyección en ovocitos.
Implicaciones clínicas de la terapia con ARN mensajero para la infertilidad
En conjunto, los resultados del trabajo apuntan a que las terapias basadas en ARNm podrían convertirse en una herramienta para tratar algunos tipos de infertilidad masculina de origen genético. A diferencia de la terapia génica basada en ADN, el ARNm no se integra en el genoma y tiene una vida media corta, lo que reduce el riesgo de alteraciones genéticas permanentes. Esta misma estrategia, con un gen diferente, mostró resultados similares hace unos meses, lo que refuerza su potencial.
El trabajo también resalta el papel de las células de Sertoli como diana terapéutica potencial. Sin embargo, la aplicación clínica de la estrategia todavía requiere de estudios adicionales. La investigación se ha realizado en ratones y será necesario evaluar su eficacia y seguridad en otros modelos.
Otra cuestión es que el tratamiento no permitió la producción de suficientes espermatozoides como para lograr una fecundación natural. La obtención de descendencia requirió técnicas de reproducción asistida, concretamente la microinyección de espermátidas en ovocitos. Los autores también señalan que la expresión del ARNm fue limitada y heterogénea dentro del testículo, por lo que habría que mejorar los sistemas de administración para aumentar la eficacia del tratamiento. También será necesario evaluar los posibles efectos a largo plazo.
En cualquier caso, como concluyen los investigadores, la administración de ARNm tiene el potencial de convertirse en una opción viable para el tratamiento de la infertilidad humana.
Artículo científico
Kanatsu-Shinohara M, et al. Messenger RNA delivery into Sertoli cells restores fertility to congenitally infertile male mice. Stem Cell Reports. 2026 Mar 5:102829. doi: https://doi.org/10.1016/j.stemcr.2026.102829
Fuente
Mashiko D, et al. Sperm and offspring production in a nonobstructive azoospermia mouse model via testicular mRNA delivery using lipid nanoparticles. Proc Natl Acad Sci U S A. 2025 Oct 21;122(42):e2516573122. doi: https://doi.org/10.1073/pnas.2516573122