Un nuevo estudio de la Universidad de Cambridge sugiere que algunas pruebas de cribado genético en embriones generados para fecundación in vitro pueden sobreestimar el riesgo de anomalías cromosómicas.
Los investigadores observaron errores mitóticos en etapas tardías del embrión que podrían no afectar al desarrollo fetal.
El desarrollo de la Fecundación In Vitro (FIV) hace ya más de 45 años, supuso un importante avance para la medicina reproductiva y la reproducción asistida. En los últimos años se han incorporado mejoras significativas en las técnicas y protocolos. Sin embargo, las tasas de éxito siguen siendo bajas debido a que una parte importante de los embriones obtenidos en laboratorio no se implanta o no se desarrolla adecuadamente.
Obtener embriones sanos y adecuados para su transferencia es uno de los retos principales de la reproducción asistida. Con este objetivo, una de las herramientas utilizadas en muchas clínicas de reproducción es el cribado genético preimplantacional de aneuploidías (PGT-A). Esta aproximación permite identificar alteraciones en el número de cromosomas mediante el análisis de células extraídas del trofoectodermo, la capa externa que rodea al embrión en sus primeros días de desarrollo y que será la encargada de formar la placenta.
Cuando se detectan aneuploidías en el trofoectodermo, el embrión suele considerarse inviable debido a que la presencia de este tipo de alteración cromosómica en el embrión es una de las principales causas de aborto espontáneo.
Aunque el cribado genético preimplantacional de aneuploidías (PGT-A) se ha generalizado en muchas clínicas de fertilidad, su eficacia real y utilidad clínica siguen siendo objeto de un intenso debate científico y ético, especialmente en los últimos años. Por una parte, los estudios clínicos no han demostrado de forma concluyente que esta estrategia aumenta la tasa de nacidos vivos. Por otra parte, no hay garantía de que las células analizadas reflejen fielmente el estado o viabilidad del resto del embrión. Una reciente investigación de la Universidad de Cambridge aborda precisamente esta cuestión. Gracias a una nueva técnica de imagen en 3D capaz de observar el desarrollo de embriones humanos en tiempo real, los investigadores han encontrado que algunas de las alteraciones que se detectan en los cribados podrían no afectar al desarrollo del embrión ni comprometer su viabilidad. Los resultados se han publicado en Nature Biotechnology.
Análisis en tiempo real del desarrollo embrionario
Para superar las limitaciones de los métodos existentes, que no son adecuados para estudiar embriones humanos en etapas preimplantacionales avanzadas, el equipo de la Universidad de Cambridge desarrolló un nuevo sistema de captura de imagen con el que pudieron observar las células vivas a alta resolución y mínima fototoxicidad durante periodos prolongados.
En primer lugar, el equipo optimizó la técnica de electroporación (que utiliza pulsos eléctricos breves con el objetivo de facilitar la entrada del material genético en las células) para introducir un ARN mensajero concreto en las células embrionarias. Este ARNm codifica una proteína fluorescente (H2B-mCherry), que al expresarse se localiza en el núcleo celular y permite visualizar el ADN.
Una vez marcado el núcleo, los embriones fueron observados mediante microscopía de lámina de luz, una técnica que permite generar imágenes tridimensionales de alta resolución durante periodos prolongados, minimizando el daño por exposición a la luz.
Mediante el nuevo sistema de imagan, los investigadores pudieron monitorizar más de 220 divisiones celulares en 13 embriones humanos en fase de blastocisto, el estadio previo a la implantación. Los embriones habían sido donados por parejas tras tratamientos de fertilidad exitosos.
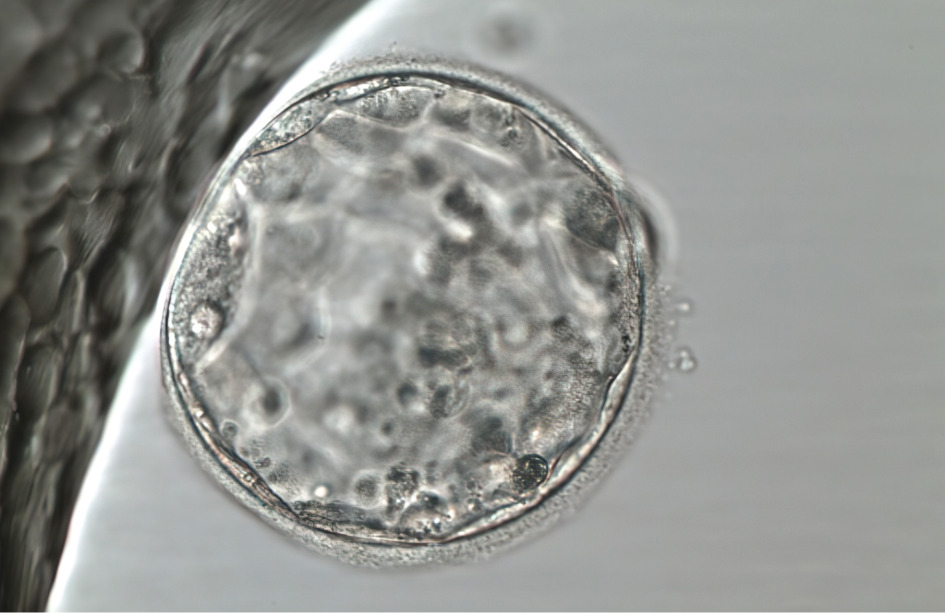
Resultados que motivan una revisión de la selección de embriones mediante cribado preimplantacional
Hasta el momento, se pensaba que las aneuploidías detectadas en el trofectodermo se originaban a partir de errores en la formación de los gametos o en las primeras divisiones del embrión que afectaban a todo el embrión. Sin embargo, el estudio demuestra que pueden ocurrir errores en las divisiones celulares en las fases tardías del desarrollo embrionario.
“Nos sorprendió enormemente descubrir que pueden producirse divisiones celulares anormales desde cero en una fase muy tardía del desarrollo humano”, ha señalado Kathy Niakan, directora del Centro Loke para la Investigación del Trofoblasto, de la Universidad de Cambridge. “Solo gracias al uso de una nueva técnica de imagen fue posible observar este fenómeno”
Los investigadores encontraron que alrededor del 10 % de las células observadas durante la división celular (correspondientes mayoritariamente a la capa externa del blastocisto, que dará lugar a la placenta) presentaban errores en la segregación cromosómica. No obstante, a pesar de estas alteraciones, las células no mostraron signos de inviabilidad y continuaron dividiéndose normalmente, lo que sugiere que estos errores pueden ser tolerados por el embrión sin comprometer su desarrollo.
Estos resultados plantean una revisión a la práctica de descartar embriones basándose únicamente en la presencia de aneuploidías en el trofoectodermo, ya que podrían tratarse de errores mitóticos tardíos, de origen espontáneo, y no de alteraciones heredadas en la fertilización.
Las alteraciones genéticas que se detectan en el cribado genético preimplantacional podrían estar confinadas a la futura placenta y no afectar a la masa celular interna, que da lugar al embrión propiamente dicho. Como consecuencia, embriones viables podrían estar siendo descartados innecesariamente. Esto es especialmente relevante porque cuando el embrión se descarta es necesario repetir el proceso de reproducción asistida, con el consecuente impacto físico, emocional y económico para los pacientes.
Además, los autores destacan que el cultivo prolongado de embriones in vitro puede estar relacionado con un aumento del riesgo de errores cromosómicos. En estas circunstancias plantean que también deberían reevaluarse los tiempos y condiciones del cultivo embrionario en clínicas de reproducción asistida.
Próximos pasos para investigar el desarrollo embrionario
Los resultados del trabajo podrían contribuir a redefinir los criterios utilizados para la selección embrionaria, promoviendo una medicina reproductiva más basada en la evidencia y menos dependiente de herramientas diagnósticas cuyo valor predictivo real puede estar sobreestimado.
En cuanto a conocimiento básico, el estudio ha permitido saber con mayor precisión cuándo y dónde se originan las anomalías cromosómicas que se detectan en el trofoectodermo. La siguiente cuestión será si realmente las células detectadas en una biopsia del trofoectodermo reflejan con precisión la composición genética de las células internas (la masa celular interna), que se convertirán en el feto. En futuros trabajos, los investigadores planean centrarse además en la masa celular interna para determinar si también pueden surgir errores mitóticos tardíos en las células que darán lugar al embrión.
La responsable del trabajo, Kathy Niakan, remarca la necesidad de impulsar más investigación básica para comprender mejor los mecanismos del desarrollo temprano y la tolerancia a la aneuploidía: “Se necesita mucha más investigación básica para informar la práctica clínica futura y mejorar las tasas de concepción asistida”.
Artículo científico
Abdelbaki, A et al. Live imaging of late-stage preimplantation human embryos reveals de novo mitotic errors. Nat Biotech; 23 Oct 2025; DOI: 10.1038/s41587-025-02851-1
Fuente
Widely-used technique for assessing IVF embryos may be flawed, study suggests. https://www.cam.ac.uk/research/news/widely-used-technique-for-assessing-ivf-embryos-may-be-flawed-study-suggests