María Sánchez Osuna y Victor J. Yuste
Universitat Autònoma de Barcelona
Centro de Investigación Biomédica en Red sobre Enfermedades Neurodegenerativas (CIBERNED-ISCIII)
Investigadores de la Universidad Autónoma de Barcelona, en colaboración con el Hospital Universitario de Bellvitge/Instituto de Investigación Biomédica de Bellvitge, la Universidad de Barcelona y el Instituto Catalán de Oncología han identificado un marcador bioquímico común en las células de glioblastoma, que consiste en una ausencia de degradación de su contenido genómico durante la apoptosis.
Los gliomas o tumores que afectan a las células de la glía, representan el 80% de los tumores cerebrales primarios malignos. Por desgracia, dentro de los gliomas, el glioblastoma o glioma de grado IV es el más común. Debido a su alta capacidad invasiva y su elevada tasa de crecimiento descontrolado, el glioblastoma es un tumor muy difícil de tratar. De hecho, aunque la combinación de la cirugía, la radioterapia y la quimioterapia ha conseguido alargar la esperanza de vida de los pacientes hasta los 2 años aproximadamente, los tratamientos actuales son incapaces de proporcionar una cura definitiva para estos pacientes.
En el estudio, los investigadores analizaron cómo células provenientes de 11 pacientes diferentes reaccionaban a estímulos citotóxicos. Independientemente de las mutaciones particulares que exhibían las células analizadas, todas las células de glioblastoma resultaron incapaces de degradar su ADN durante la apoptosis. La apoptosis es el tipo mas conocido de muerte celular programada y, además, constituye la vía principal a través de la cual, tanto la radiación como los fármacos anticancerígenos destruyen las células tumorales. Durante la apoptosis, la correcta activación de las caspasas permite que el contenido celular sea integrado en los denominados cuerpos apoptóticos para su posterior eliminación por parte de las células del sistema inmune o de células vecinas. Para ello, el material genético necesita ser degradado en fragmentos de bajo peso molecular y empaquetarse correctamente, una tarea que depende de la acción de la enzima con actividad endonucleásica DFF40/CAD (del inglés, DNA Fragmentation Factor 40 KDa subunit / Caspase-Activated DNase). Los investigadores vieron que, a pesar de que la mayoría de las células de glioblastoma eran capaces de activar correctamente las caspasas después de ser expuestas a estímulos citotóxicos, la actividad de la endonucleasa DFF40/CAD en las células tumorales era limitada. Esto se debía no sólo a que la enzima estuviera extrañamente localizada en el núcleo y no en el citoplasma ya antes del tratamiento, sino también porque sus niveles de expresión eran muy bajos. Así, la expresión forzada de DFF40/CAD, la cual incrementaba la cantidad de proteína disponible en el citoplasma, el compartimento subcelular donde tiene lugar la activación de las caspasas, provocó que las células recuperasen su capacidad de degradar el ADN durante la apoptosis.
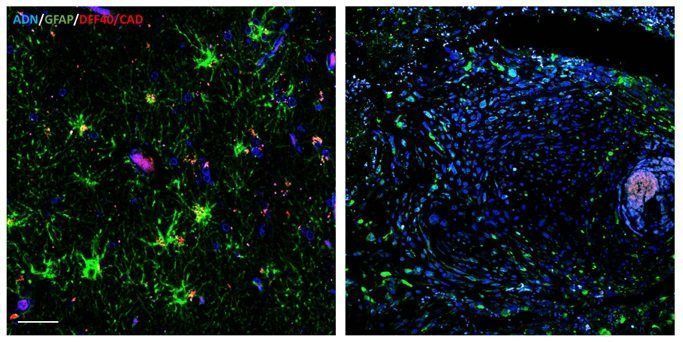
Una vez obtenidos estos resultados, los investigadores realizaron un estudio histológico mediante inmunohistoquímica. Después de analizar la expresión de DFF40/CAD en diferentes muestras de gliomas concluyeron que los niveles de expresión de la endonucleasa en los gliomas son inferiores a los observados en tejido cerebral de personas sanas. De hecho, estos resultados también se observaron al comparar los niveles de expresión de la proteína en tejido tumoral y no tumoral dentro de un mismo paciente, lo cual parecería indicar que la bajada de expresión de DFF40/CAD podría estar relacionada con el proceso de gliomagénesis.
A pesar de los esfuerzos realizados durante la ultima década, hasta ahora no se había encontrado ningún defecto genético ni bioquímico común en el glioblastoma. Los bajos niveles de expresión de la endonucleasa DFF40/CAD y la ausencia de degradación apoptótica del ADN, en fragmentos oligonucleosomales o de bajo peso molecular, constituyen, respectivamente, el primer marcador molecular y bioquímico de este tumor, lo que hace pensar en su posible relevancia de cara a entender su agresividad. Aunque este estudio es algo preliminar, los investigadores se encuentran esperanzados y confían que estos resultados sienten las bases de tratamientos más eficaces en el futuro.
Referencia: Sánchez-Osuna M, et al. An intrinsic DFF40/CAD endonuclease deficiency impairs oligonucleosomal DNA hydrolysis during caspase-dependent cell death: a common trait in human glioblastoma cells. Neuro Oncol. 2016. Doi: 10.1093/neuonc/nov315 http://dx.doi.org/10.1093/neuonc/nov315

