Un estudio publicado recientemente en el New England Journal of Medicine presenta resultados prometedores a largo plazo para una terapia génica para la anemia falciforme en pacientes.
La terapia, probada en 35 pacientes adultos de diferentes centros médicos estadounidenses, forma parte de un programa clínico de la empresa bluebird bio y consiste en un trasplante de células del propio paciente modificadas para incluir una versión del gen beta globina que reduce la proporción de proteína hemoglobina anómala característica de los pacientes.
Con una única dosis de terapia lovo-cel (también conocida como lovotibeglogene autotemcel), que compacta una versión modificada del gen beta-globina en un vector lentiviral, los investigadores observaron una reducción significativa de los eventos clínicos adversos que caracterizan a la enfermedad.
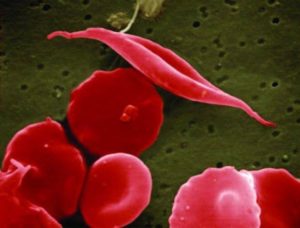
La anemia falciforme, un problema clínico a resolver
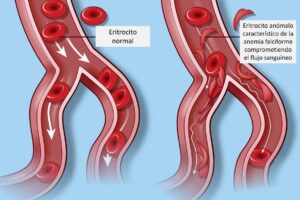
Como trastorno hereditario sanguíneo más frecuente la anemia falciforme es una de las enfermedades más estudiadas. Su origen se encuentra en la presencia de ciertas mutaciones en el gen HBB, que codifica para la proteína beta globina, una de las subunidades de la hemoglobina. Estas mutaciones llevan a la producción de una forma anómala de beta globina que compromete la formación de la hemoglobina y deriva en unos eritrocitos frágiles y de conformación anómala que mueren de forma prematura causando anemia y pueden provocar otras complicaciones por su dificultad para circular en los vasos sanguíneos más pequeños.
La anemia falciforme puede ser tratada mediante un trasplante de médula ósea. Sin embargo, este tratamiento depende de la existencia de un donante compatible, por lo que no es una opción viable en la mayoría de los pacientes. Su causa genética tan concreta y definida ha llevado a que durante los últimos años, se hayan planteado diferentes aproximaciones de terapia génica para la enfermedad que buscan introducir copias normales del gen o recuperar la expresión de la hemoglobina fetal (en la que no interviene HBB) en las células precursoras de la sangre del propio paciente.
Resultados a largo plazo
En el reciente estudio, los investigadores evaluaron la efectividad y seguridad de la terapia lovo-cel en 35 pacientes adultos. Con única infusión de células modificadas se observó que esta población de células se mantenía hasta 36 meses después del tratamiento. Además, la hemoglobina derivada de la terapia, HbAT87Q , representaba al menos un 40% del total de hemoglobina de los pacientes a partir del sexto mes tras el tratamiento, lo que representa una mejora para los pacientes.
Respecto a las consecuencias clínicas de la terapia, los investigadores encontraron evidencias bioquímicas de una reducción en la hemolisis o muerte prematura de eritrocitos, proceso que está aumentado en los pacientes de anemia falciforme y deriva en anemia hemolítica.
Además, los investigadores destacan que no se produjo ningún evento vaso oclusivo grave en los 25 pacientes en los que se pudo hacer un seguimiento de esta característica durante al menos 6 meses. Los eventos vaso oclusivos consisten en episodios de dolor agudo que se producen como consecuencia de la agrupación de eritrocitos anómalos y bloqueo de vasos sanguíneos. Estos eventos influyen en la calidad de vida de los pacientes ya que pueden afectar a diferentes tejidos y órganos y frecuentemente resultan en consultas en urgencias o hospitalizaciones. En los 24 meses previos a la terapia, los pacientes habían mostrado entre un mínimo de 2 y un máximo de 13.5 eventos vaso oclusivos.
Una terapia para la anemia falciforme que utiliza las propias células de los pacientes
La terapia lovotibeglogene autotemcel modifica y utiliza las propias células de los pacientes como tratamiento, lo que reduce el riesgo de rechazo, como ocurre con otros tipos de trasplantes. Para ello, los investigadores extraen células madre de la sangre y utilizan vectores lentivirales para introducir en ellas una versión modificada del gen HBB, denominada βA-T87Q. Posteriormente, estas células modificadas, de las que pueden derivar diferentes tipos de células sanguíneas, entre ellas los eritrocitos, son introducidas de nuevo en los pacientes.
Como resultado de la terapia, los eritrocitos de los pacientes pueden incluir la versión de beta globina βA-T87Q en la síntesis de hemoglobina y se reduce la proporción de hemoglobina anómala que produce la enfermedad.
Aspectos por mejorar de la terapia para la anemia falciforme
Los resultados del trabajo resultan muy prometedores. No obstante, existen diferentes limitaciones y aspectos que pueden ser mejorados.
Por una parte, los investigadores señalan que 12 de los pacientes sufrieron algún efecto adverso grave asociado al tratamiento, como dolor abdominal, nauseas o vómitos. En tres de los pacientes estos efectos se asociaron a la infusión de tratamiento.
Otra limitación del tratamiento es que, para favorecer la adaptación y mantenimiento de las células modificadas en los pacientes éstos deben recibir una dosis elevada de quimioterapia, que elimine las células madre a reemplazar. Este tratamiento puede resultar tóxico y está asociado a un riesgo aumentado a desarrollar cáncer. De hecho, dos pacientes de la cohorte inicial de pacientes tratados con lovo-cel desarrollaron leucemia mieloide.
De momento, ninguno de los 35 pacientes tratados en la fase más avanzada del estudio ha desarrollado ningún tipo de cáncer y los investigadores no han identificado ninguna evidencia de que pueda producirse una inserción del vector o el gen HBB en una región no deseada relacionada con el cáncer.
En este contexto, los investigadores sospechan que los dos casos de leucemia podrían estar asociados a la quimioterapia y están trabajando en aproximaciones menos tóxicas para preparar al organismo para la terapia. “El objetivo será utilizar este tratamiento tan pronto como sea posible, antes de que los pacientes desarrollen daños en los órganos y otras complicaciones asociadas a la anemia falciforme”, destaca Markus Y. Mapara, profesor en la Universidad de Columbia y uno de los autores del trabajo. “sin embargo antes de que podamos hacer esto necesitamos encontrar una alternativa segura a la quimioterapia para las estrategias de condicionamiento, como por ejemplo anticuerpos”.
La terapia lovo-cel ha sido designada como medicamento huérfano por la Administración de Alimentos y Fármacos de EE. UU. No obstante, es un tratamiento en investigación que no ha sido aprobado todavía en ningún país.
La empresa bluebird bio planea continuar los ensayos clínicos con lovo-cel en adultos. De momento, el programa clínico en menores de 18 años ha sido detenido temporalmente por la FDA hasta aclarar lo ocurrido con un paciente adolescente, que había manifestado una anemia persistente tras el tratamiento. El paciente se encuentra bien y no hay evidencias de ningún proceso tumoral.
Bluebird bio cuenta con una terapia similar ya aprobada para otra enfermedad causada por mutaciones en el gen HBB, la beta-thalasemia.
Referencia: Kanter J, et al. Biologic and Clinical Efficacy of LentiGlobin for Sickle Cell Disease. NEJM. 2021. DOI: http://dx.doi.org/10.1056/NEJMoa2117175
Fuentes: Experimental Gene Therapy Reverses Sickle Cell Disease for Years. https://www.cuimc.columbia.edu/news/experimental-gene-therapy-reverses-sickle-cell-disease-years
bluebird bio Announces Partial Clinical Hold for Patients Under 18 in Sickle Cell Gene Therapy Clinical Program. https://investor.bluebirdbio.com/news-releases/news-release-details/bluebird-bio-announces-partial-clinical-hold-patients-under-18
New and Updated Data Demonstrating Sustained Treatment Response in Patients Treated in Largest Sickle Cell Gene Therapy Program To-Date Presented at ASH21 and Published in NEJM. https://investor.bluebirdbio.com/news-releases/news-release-details/new-and-updated-data-demonstrating-sustained-treatment-response
Si te ha gustado esta noticia y quieres aprender más sobre Genética en Medicina, te interesa nuestra formación, como el “Máster de Medicina de Precisión y Genética Clínica“, o el “Experto Universitario en Enfermedades Raras y Genética Clínica“.



