El sarcoma de Ewing es un tipo de cáncer de las células redondas. Está catalogado como enfermedad rara y se manifiesta mayoritariamente en niños y adolescentes. Los tumores se encuentran principalmente en huesos y tejidos blandos. Su agresividad, elevada tasa de recaídas y mortalidad, evidencian la urgencia para desarrollar nuevas terapias. Las estrategias terapéuticas de que disponemos hoy en día (quimioterapia) son poco efectivas y presentan un alto número de efectos secundarios indeseados y seriamente perjudiciales para la salud del paciente.
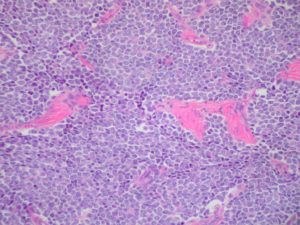
Las doctoras Scotlandi y Caré, del Instituto Ortopédico de Rizzoli (IRCCS) e Instituto superior de Sanidad de Roma, han liderado una investigación basada en la biología básica del Sarcoma de Ewing que aporta nuevos conocimientos y apunta hacia otras estrategias clínicas.
La proteína de membrana CD99 está altamente expresada en células tumorales del sarcoma de Ewing (EWS). De ella depende el mantenimiento y la agresividad del tumor ya que participa en procesos biológicos esenciales como la diferenciación, migración y muerte celular entre otros. Las células EWS tienen la capacidad de liberar y transportar CD99 hacia otras células mediante los exosomas (EXOs). Estos últimos son vesículas extracelulares especializadas que juegan un papel principal en la comunicación celular. Pueden cargar y transferir distintos tipos de moléculas como proteínas, ARNs mensajeros y micro-ARNs necesarios para la puesta en marcha de mecanismos oncogénicos en las células receptoras.
Los investigadores utilizan dos líneas celulares estables de EWS que no expresan CD99 para producir y purificar exosomas que no contienen CD99 (EXOs CD99neg). Posteriormente incuban células EWS con EXOs CD99neg y las comparan con EWS incubadas con exosomas que sí contienen CD99 (EXOs CD99pos).
Los resultados indican que las EWS que absorben EXOs CD99neg presentan un crecimiento celular más bajo y una reducción en proliferación celular, pero no una inducción de muerte celular. Además, células EWS con EXOs CD99neg, presentan mayor grado de diferenciación neuronal. Estas características fenotípicas de EWS con EXOs CD99neg reproducen el fenotipo que se asocia a un silenciamiento estable de CD99. Los investigadores concluyen que los EXOs CD99neg poseen capacidades antioncogénicas y de diferenciación celular.
Tras realizar un perfil de expresión génica, el estudio demuestra que los CD99neg EXOs modulan la expresión de genes en células EWS receptoras después de 24h de incubación con CD99neg EXOs. Los resultados (comprobados con ensayos de actividad con luciferasa) apuntan hacia una disminución de la expresión de c-fos y de la proteína activadora-1 (AP-1) así como de algunas de sus dianas: CCND1, MMP9 y MMP1 .
Otros procesos afectados son la neurogénesis, diferenciación neuronal y guía axonal. Estos resultados confirman que el efecto antineoplásico y de diferenciación neuronal en células EWS con EXOs CD99neg son debidos, en parte, a la alteración de la expresión génica.
Para finalizar, los autores utilizan microarrays para analizar el contenido de micro-ARN en EXOs de las líneas celulares CD99pos EXOs y CD99neg EXOs. Además de caracterizar el contenido de micro-ARN de las distintas líneas, los investigadores identifican el miR-199a-3p como el más abundante en los EXOs CD99neg.Tras confirmar la acumulación de este micro-ARN con PCR cuantitativa, incuban células TC-71 e IOR/CAR con miR-199a-3p y observan el mismo fenotipo que en las células EXOs CD99neg: un efecto antioneoplásico y una inducción de la diferenciación celular neuronal. También identifican (a través de análisis in-silico) a c-Fos como diana de miR-199a-3p, así como una inhibición de la actividad de AP-1 y una reducción de los niveles de c-Fos.
Los investigadores proponen que el miR-199a-3p identificado en EXOs CD99neg funciona como un nuevo supresor de tumores en células EWS. Para validar su hipótesis, generan una línea de EXOs CD99neg que expresa el miR-199a-3p (CD99pos EXOs [miR-199a-3p]). Las células infectadas con CD99pos EXOs [miR-199a-3p] presentan el mismo fenotipo que las células infectadas directamente con el miR-199a-3p, validando así sus observaciones.
El equipo de Scotlandi y Caré, llevan sus observaciones a la clínica y comprueban sus hipótesis en muestras de pacientes con EWS. Cuantifican los niveles de expresión de miR-199a-3p en tumores localizados, primarios y sin tratar (n=62) y los comparan con lesiones metastásicas (n= 51). Observan una expresión significantemente más baja de miR-199a-3p en los procesos metastásicos, sugiriendo una contribución notable de este micro-ARN a la agresividad de EWS.
En primer lugar, de este artículo podemos deducir la necesidad de entender la biología básica subyacente en las patologías y poderlas relacionar con casos clínicos. La investigación demuestra que, la alteración del contenido de las vesículas de transporte, en este caso un micro-ARN, puede ejercer efectos antineoplásicos en las células receptoras. En segundo lugar, aporta información muy valiosa para el desarrollo y la investigación en nanotransportadores «naturales» (exosomas) que gozan, actualmente, de un creciente interés como estrategia terapéutica oncológica.
Además, este trabajo proporciona bases moleculares para la ingeniería de dichos nanotransportadores y ofrece una nueva oportunidad terapéutica para controlar tanto tumores primarios como metástasis. Finalmente, este artículo abre un nuevo campo de investigación muy necesario sobre el agresivo sarcoma de Ewing y establece nuevas bases para poder superar las limitaciones de las terapias convencionales.
Referencia: De Feo et al. Exosomes from CD99-deprived Ewing sarcoma cells reverse tumor malignancy by inhibiting cell migration and promoting neural differentiation. Cell Death and Disease. 2019. https://doi.org/10.1038/s41419-019-1675-1
Si te ha gustado esta noticia y quieres aprender más sobre Genética y Cáncer, quizás te interese nuestro curso “Medicina Genómica en Oncología y sus aplicaciones clínicas”. Tienes más información sobre el curso aquí.


